Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Medicina Geral e Familiar
versão impressa ISSN 2182-5173
Rev Port Med Geral Fam vol.33 no.2 Lisboa abr. 2017
REVISÕES
Ácido acetilsalicílico na prevenção da pré-eclâmpsia: uma revisão baseada na evidência
Aspirin in pregnancy for the prevention of preeclampsia: an evidence-based review
Sara Santos Ferreira,1-2 Ana Carolina Martins,1,3 Ana Cláudia Magalhães,1,4 Hélder Martins5-6
1. Médica Interna de Medicina Geral e Familiar
2. USF Infesta, Unidade Local de Saúde de Matosinhos
3. USF Fiães, ACeS Feira Arouca
4. UCSP Moimenta da Beira, ACeS Douro Sul
5. Médico Especialista em Medicina Geral e Familiar
6. USF Maresia, Unidade Local de Saúde de Matosinhos
Endereço para correspondência | Dirección para correspondencia | Correspondence
RESUMO
Objetivo: Rever a evidência atual sobre o efeito do ácido acetilsalicílico (AAS) na prevenção da pré-eclâmpsia.
Fontes de dados: MEDLINE e sítios de medicina baseada na evidência.
Métodos de revisão: Pesquisa de normas de orientação clínica (NOC), ensaios clínicos aleatorizados e controlados (ECAC), revisões sistemáticas (RS) e meta-análises (MA), publicados entre 13/11/2005 e 13/11/2015, utilizando os termos MESH ‘pre-eclampsia’ e ‘aspirin’ e os termos DeCS ‘pre-eclâmpsia’ e ‘aspirina’. Para atribuição do nível de evidência (NE) e força de recomendação (FR) foi utilizada a Strenght of Recommendation Taxonomy, da American Academy of Family Physicians.
Resultados: Foram selecionados 14 de entre 296 artigos encontrados: sete MA, três RS, três NOC e um ECAC. Globalmente, as RS e MA demonstram o benefício do AAS na prevenção da pré-eclâmpsia, principalmente em mulheres de alto risco. Apenas uma RS com NE 2 não encontrou evidência para suportar o uso desta profilaxia nas mulheres em risco de pré-eclâmpsia. Os estudos que analisam separadamente as mulheres de baixo risco na população-alvo verificaram uma ausência de benefício do AAS neste grupo de mulheres. As NOC recomendam o uso de AAS na prevenção da pré-eclâmpsia em mulheres de alto risco, desaconselhando o seu uso nas mulheres de baixo risco. O ECAC faz a mesma recomendação relativamente às mulheres de alto risco.
Conclusões: A evidência disponível indica que o AAS em baixa dose tem benefício quando usado como medicação preventiva nas mulheres em risco de pré-eclâmpsia, com evidência clara do seu benefício nas mulheres de alto risco (FR A), sendo desaconselhado o seu uso em mulheres de baixo risco (FR A). Existe ainda necessidade de mais estudos de elevada qualidade, de metodologia homogénea e amostras relevantes que suportem esta evidência.
Palavras-chave: Pre-eclâmpsia; Aspirina.
ABSTRACT
Objectives: To review the current evidence for the effectiveness of aspirin in preventing preeclampsia.
Data sources: MEDLINE and evidence-based medicine websites.
Methods: We searched for clinical practice guidelines (CPG), randomized controlled trials (RCT), systematic reviews (SR) and meta-analyzes (MA), published between 13/11/2005 and 13/11/2015, using the MESH terms ‘pre-eclampsia’ and ‘aspirin’ and the Portuguese DeCS terms ‘pre-eclâmpsia’ and ‘aspirina’. The Strength of Recommendation Taxonomy (SORT) of American Academy of Family Physicians was used for the assignment of levels of evidence (LE) and the strength of recommendations (SOR).
Results: A total of 14 articles were selected for this review out of 296 articles found. These included seven MA, three SR, three CPG and one RCT. The SR and MA found benefits for aspirin in the prevention of preeclampsia, particularly in women at high-risk. One SR with LE 2 found no evidence to support the use of aspirin prophylaxis in women at risk for preeclampsia. Studies that analyzed women at low-risk separately found no benefit from the use of aspirin in this group of women. The CPG recommend the use of aspirin in the prevention of preeclampsia in high-risk women and discouraged its use in low-risk women. The RCT supported the same recommendation for high-risk women.
Conclusions: The available evidence suggests that low-dose aspirin is effective for the prevention of preeclampsia in women at risk. There is clear evidence of its benefit in high-risk women (SOR A) and its use is discouraged in low-risk women (SOR A). There is still a need for more high quality studies with similar methods conducted in relevant populations to support these recommendations.
Keywords: Pre-eclampsia; Aspirin.
Introdução
A pré-eclâmpsia é uma das patologias obstétricas mais graves, sendo uma das principais causas de morbimortalidade materna e fetal.1 Habitualmente manifesta-se na segunda metade da gravidez, complicando 2 a 8% das gestações2 e contribuindo para mais de 100.000 mortes maternas por ano a nível global.3 Segundo a International Society for the Study of Hypertension in Pregnancy (ISSHP), a pré-eclâmpsia é definida pelo início de hipertensão após as 20 semanas de gestação, combinada com proteinúria (>300mg/dia) ou outras disfunções de órgão-alvo, como disfunção renal ou hepática, complicações neurológicas ou hematológicas, disfunção útero-placentária ou restrição de crescimento intrauterino (RCIU).4 A pré-eclâmpsia está ainda associada a parto pré-termo, quer espontâneo quer iatrogénico, e a nascimento de recém-nascidos pequenos para a idade gestacional (RN-PIG).5 Adicionalmente, as crianças nascidas de mães com pré-eclâmpsia têm maior risco de displasia broncopulmonar e paralisia cerebral associadas ao parto pré-termo.5 De um modo geral, a pré-eclâmpsia diminui a qualidade de vida relacionada com a saúde e aumenta o risco de depressão pós-parto.5
Apesar da causa da pré-eclâmpsia permanecer desconhecida, parece estar relacionada com alterações ao nível da formação e organização da placenta, com consequentes defeitos na perfusão útero-placentária e indução de um estado de hipercoagulabilidade.6 Este último aspeto parece estar relacionado com uma deficiência relativa da produção de prostaciclina (um vasodilatador) e produção excessiva de tromboxano (uma prostaglandina vasoconstritora sintetizada durante a agregação plaquetária).1 Tem sido proposto que a terapêutica com ácido acetilsalicílico (AAS) em baixa dose inibe a produção de tromboxano, reduzindo a vasoconstrição e a hipercoagulabilidade da placenta,7 hipótese que motivou a realização de vários ensaios clínicos a avaliar o uso de agentes antiplaquetários, como o AAS na prevenção da pré-eclâmpsia.1 Adicionalmente tem sido sugerido que a eficácia do AAS pode estar relacionada com a idade gestacional em que é iniciada a terapêutica.8 A normal formação e estruturação da placenta compreende a invasão das artérias espirais do endométrio pelas células do trofoblasto, processo que ocorre a partir da oitava semana de gestação, acreditando-se estar completa entre as 16 e as 20 semanas de gestação. Pelo exposto, alguns autores defendem haver maior benefício na introdução do AAS numa fase precoce da gravidez.9
O médico de família, sendo a base do sistema de saúde, é o primeiro profissional a providenciar cuidados obstétricos à população, tendo um papel importante no rastreio e abordagem inicial das mulheres com risco ou diagnóstico de pré-eclâmpsia. Neste sentido, os autores pretendem rever a evidência mais recente sobre a eficácia do AAS na prevenção da pré-eclâmpsia.
Métodos
Foi realizada uma pesquisa de normas de orientação clínica (NOC), ensaios clínicos aleatorizados e controlados (ECAC), revisões sistemáticas (RS) e meta-análises (MA), publicados entre 13 de novembro de 2005 e 13 de novembro de 2015, nas línguas portuguesa e inglesa, indexados nas bases de dados da National Guideline Clearinghouse, National Institute for Health and Care Excellence (NICE) Guidelines Finder, Canadian Medical Association Practice Guidelines Infobase, The Cochrane Library, Database of Abstracts of Reviews of Effectiveness (DARE), Bandolier, Evidence Based Medicine Online e MEDLINE, utilizando os termos MESH ‘pre-eclampsia’ e ‘aspirin’ e os termos DeCS ‘pre-eclâmpsia’ e ‘aspirina’.
Os critérios utilizados para a inclusão dos artigos consistiram em: população-alvo constituída por mulheres grávidas sem pré-eclâmpsia na gravidez atual; intervenção terapêutica com AAS (sem restrições de dosagem; isolado ou em associação com outros agentes antiagregantes plaquetários); em comparação com placebo ou nenhum tratamento e outcome relacionado com a ocorrência de pré-eclâmpsia.
Foram utilizados como critérios de exclusão: estudos não-randomizados, artigos duplicados, artigos de opinião, artigos de revisão clássica de tema, sumários de sítios na Internet e artigos discordantes do objetivo da revisão. Foram também excluídos ensaios clínicos incluídos em RS ou MA selecionadas.
Para estratificar o nível de evidência (NE) dos estudos e a força de recomendação (FR) foi utilizada a Strenght of Recommendation Taxonomy (SORT),7 da American Academy of Family Physicians.
A seleção dos artigos para revisão foi feita em duplicado pelos dois primeiros autores que, perante dúvidas, discutiram em conjunto a inclusão/exclusão do artigo com uma taxa de concordância final de 100%. A leitura integral foi realizada e a avaliação da qualidade e NE dos artigos incluídos discutida por todos os autores.
Resultados
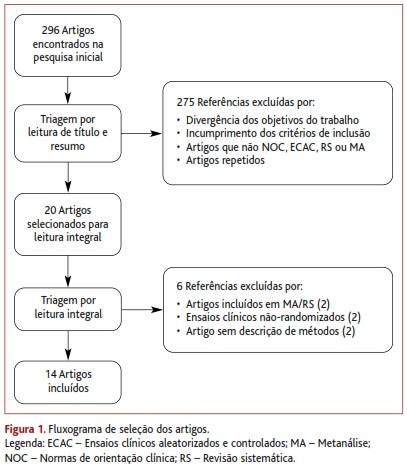
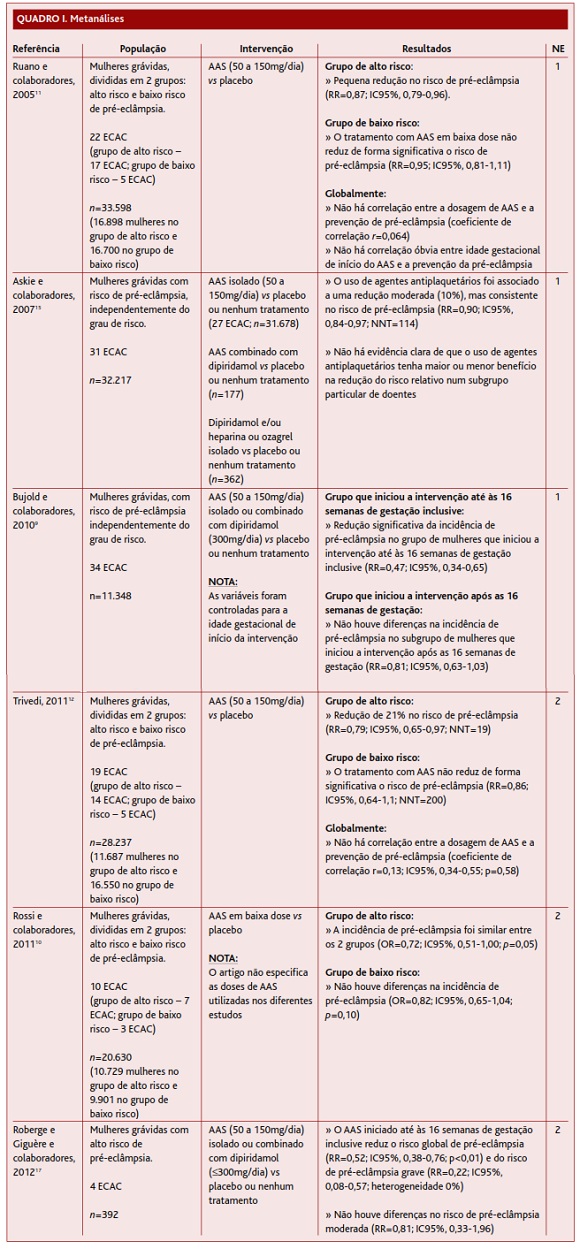
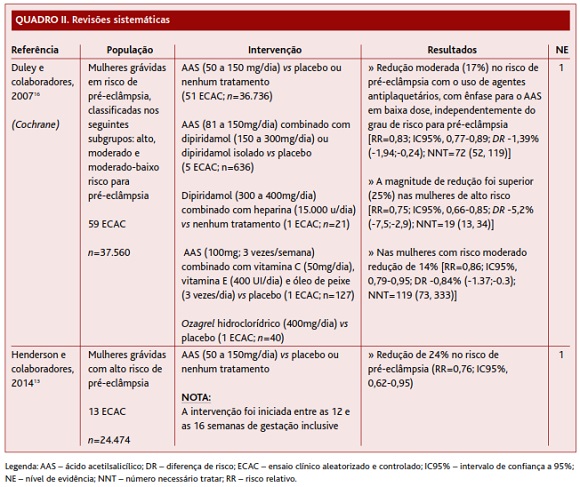
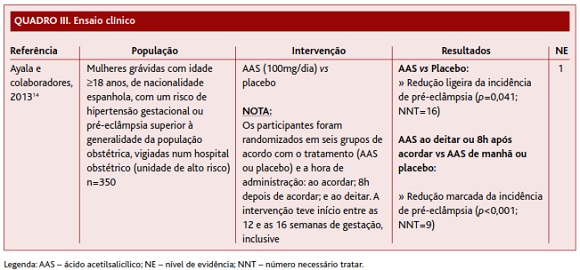
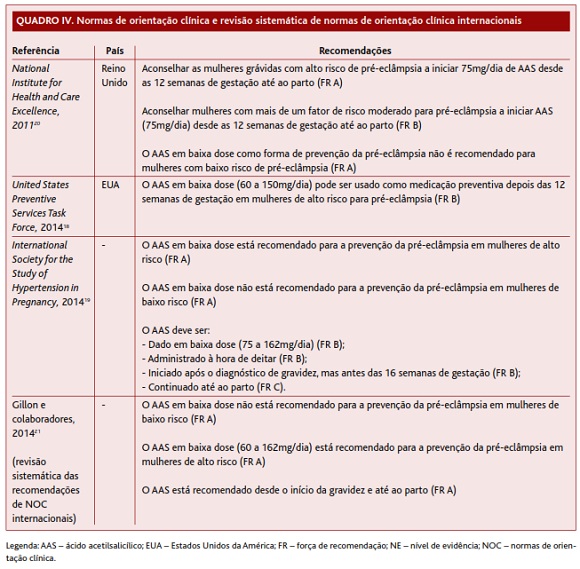
Da pesquisa efetuada resultou um total de 296 artigos, dos quais 14 cumpriam todos os critérios de inclusão: sete MA, três RS, três NOC e um ECAC. A Figura 1 representa o fluxograma de seleção dos estudos. Os Quadros I, II e III resumem as características dos estudos selecionados para revisão.
Mulheres de alto risco versus mulheres de baixo risco
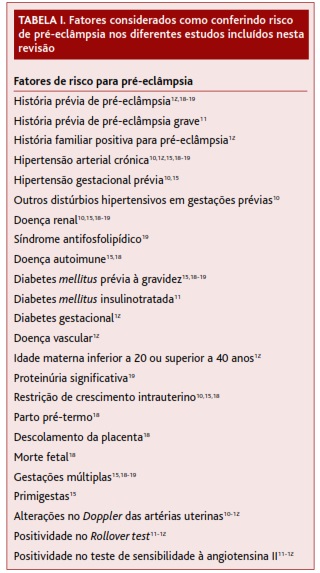
Dos estudos incluídos, três MA10-12 avaliaram o efeito do AAS na prevenção da pré-eclâmpsia, estratificando as mulheres de acordo com o seu grau de risco. Para tal selecionaram ECAC cuja intervenção consistia no uso de AAS vs placebo em mulheres grávidas divididas em dois subgrupos: alto e baixo risco para pré-eclâmpsia. Os fatores que permitiram a estratificação das mulheres em grupos de risco encontram-se listados na Tabela I. Ruano e colaboradores11 e Trivedi12 concluem que o AAS em baixa dose tem um pequeno efeito na prevenção da pré-eclâmpsia nas mulheres de alto risco (RR=0,87 com IC95%, 0,79-0,9611 e RR=0,79 com IC95%, 0,65-0,97,12 respetivamente), não apresentando, contudo, um efeito significativo na redução de risco nas mulheres de baixo risco (RR=0,95 com IC95%, 0,81-1,1111 e RR=0,86 com IC95%, 0,64-1,1,12 respetivamente). Apesar de chegarem às mesmas conclusões, a qualidade da evidência não é igual nos dois trabalhos. A MA de Ruano e colaboradores11 incluiu apenas ECAC de boa qualidade, apresentando uma boa descrição da metodologia utilizada, justificando a atribuição de NE 1. Já Trivedi,12 apesar de ter selecionado apenas ensaios clínicos prospetivos, randomizados e duplamente cegos, por parca informação não é possível aferir a consistência e qualidade dos estudos incluídos, pelo que foi atribuído a este trabalho NE 2. Rossi e colaboradores10 chegam a uma conclusão diferente. Os autores não conseguem encontrar diferenças significativas entre o grupo tratado com AAS e o tratado com placebo, quer para as mulheres de alto risco (OR=0,72; IC95%, 0,51-1,00; p=0,05) quer para as de baixo risco (OR=0,82; IC95%, 0,65-1,04; p=0,10), concluindo não haver evidência que suporte a administração de AAS em baixa dose para a prevenção da pré-eclâmpsia. Contudo, o artigo não especifica as dosagens de AAS utilizadas nos diferentes estudos, nem aquilo que os autores consideram como baixa dose de AAS. Por este motivo e por não especificar com clareza os critérios de seleção dos estudos incluídos foi atribuído a este trabalho NE 2.
Henderson e colaboradores13 conduziram uma RS com o objetivo de avaliar o efeito do AAS na prevenção da pré-eclâmpsia apenas em mulheres de alto risco. Para tal selecionaram ECAC cuja intervenção consistia na toma de AAS em baixa dose comparado com placebo ou nenhum tratamento na população supracitada. Após análise, os autores concluem haver benefício no uso de AAS em baixa dose para prevenção da pré-eclâmpsia em mulheres de alto risco (RR=0,76 com IC95%, 0,62-0,95). À semelhança de Henderson e colaboradores,13 também Ayala e colaboradores14 procuraram avaliar o efeito do AAS na prevenção da pré-eclâmpsia em mulheres de alto risco, verificando uma redução ligeira na incidência de pré-eclâmpsia com a intervenção (p=0,04 com número necessário tratar (NNT)=16). Ambos os trabalhos cumprem critérios de boa qualidade, pelo que lhes foi atribuído NE 1.
Askie e colaboradores,15 numa MA publicada na Lancet, e Duley e colaboradores,16 numa RS da Cochrane, tiveram como objetivo avaliar o efeito, não só do AAS, mas também de outros agentes antiagregantes plaquetários (dipiridamol, heparina e ozagrel) na prevenção da pré-eclâmpsia. Ambos os estudos incluíram mulheres grávidas em risco de pré-eclâmpsia, independentemente do grau de risco, e verificaram uma redução moderada, mas significativa, do risco de pré-eclâmpsia (10%15 e 17%,16 respetivamente) com o uso de agentes antiagregantes plaquetários. No entanto, a RS da Cochrane refere ainda que a magnitude da redução foi superior nas mulheres de alto risco (25%; NNT=19) face às de moderado risco (14%; NNT=119).16 Já a MA publicada na Lancet refere não haver evidência clara de que a intervenção tenha maior ou menor benefício na redução do risco relativo num subgrupo particular de doentes (NNT global=114).15 Apesar de a análise avaliar a ação de vários agentes antiagregantes plaquetários na prevenção da pré-eclâmpsia, Duley e colaboradores16 salientam que a maior parte da evidência (51 de 59 ECAC) se refere ao AAS em baixa dose, pelo que deve ser este o agente de escolha. Por sua vez, Askie e colaboradores15 não especificam nenhum agente antiagregante plaquetário em particular, embora o AAS também tenha sido o agente mais utilizado na intervenção (27 de 31 ECAC). Ambos os trabalhos cumprem critérios de boa qualidade dos ECAC selecionados, pelo que foi atribuído a ambos NE 1.
Roberge e Giguère e colaboradores17 conduziram uma MA com o objetivo de avaliar o benefício do AAS em baixa dose, iniciado até às 16 semanas de gestação, na prevenção de pré-eclâmpsia grave e de pré-eclâmpsia moderada em mulheres de alto risco para pré-eclâmpsia. Para tal selecionaram ECAC cuja intervenção consistia no uso de AAS em baixa dose, isoladamente ou em associação com dipiridamol, iniciado até à idade gestacional supracitada, controlado com placebo ou nenhum tratamento. Os autores concluem que o início de AAS em baixa dose até às 16 semanas de gestação, inclusive, se associa a uma diminuição do risco global de pré-eclâmpsia em mulheres de alto risco (RR=0,52; IC95%, 0,38-0,76; p<0,01). Analisando separadamente os resultados para o risco de pré-eclâmpsia grave e moderada, os autores verificaram que essa redução de risco é sobretudo para a pré-eclâmpsia grave, em que a redução do risco relativo se aproxima dos 90%, não havendo diferenças para a pré-eclâmpsia moderada (RR=0,81; IC95%, 0,33-1,96). O facto de esta RS ter incluído um pequeno número de estudos com um número reduzido de participantes pode ter conduzido a vieses significativos, pelo que foi atribuído a este trabalho NE 2.
A United States Preventive Services Task Force (USPSTF) publicou, em 2014, uma NOC relativa ao uso de AAS em baixa dose na prevenção da morbimortalidade por pré-eclâmpsia.18 Esta entidade concluiu com moderada certeza haver evidência substancial do benefício do AAS em baixa dose na redução do risco de pré-eclâmpsia em mulheres de alto risco. Neste sentido, recomenda o uso de AAS em baixa dose em mulheres grávidas de alto risco para pré-eclâmpsia (FR B).
A ISSHP emitiu, em 2014, uma NOC para a abordagem das doenças hipertensivas na gravidez, de entre as quais se salienta a pré-eclâmpsia.19 Esta entidade conclui haver boa evidência para recomendar o uso de AAS em baixa dose para prevenção da pré-eclâmpsia em mulheres de alto risco (FR A), não havendo evidência suficiente para fazer esta recomendação em mulheres de baixo risco (FR A).
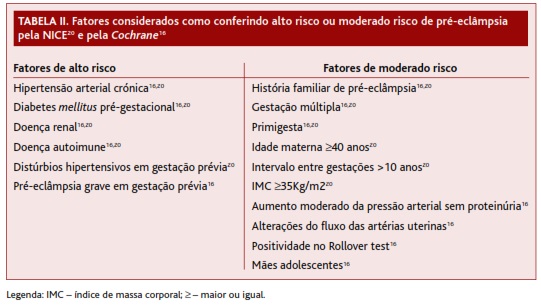
O National Institute for Health and Care Excellence (NICE) publicou, em 2011, uma NOC sobre a abordagem das doenças hipertensivas na gravidez, elaborada pelo Royal College of Obstetricians and Gynaecologists em colaboração com o National Collaborating Centre for Women’s and Children’s Health.20 Estas entidades concluem existir evidência suficiente para recomendar AAS em baixa dose na prevenção da pré-eclâmpsia, sendo que o risco-benefício do seu uso é dependente do risco de desenvolver pré-eclâmpsia. Assim, existe uma clara indicação em aconselhar AAS em baixa dose para profilaxia da pré-eclâmpsia em mulheres de alto risco (FR A), contrariamente ao que se verifica para as mulheres de baixo risco (FR A). Embora admitam que os estudos não são consensuais relativamente aos critérios para classificação de mulheres de moderado risco, estas entidades recomendam também o uso de AAS em baixa dose na presença de pelo menos dois fatores de risco moderado para a doença (FR B). Os fatores considerados pela NICE para estratificação das mulheres em alto e moderado risco para pré-eclâmpsia encontram-se listados na Tabela II.
Gillon e colaboradores21 realizaram uma RS das recomendações de NOC internacionais sobre a abordagem de doenças hipertensivas na gravidez, onde se inclui a pré-eclâmpsia. Os autores recomendam o uso de AAS em baixa dose para a prevenção da pré-eclâmpsia em mulheres de alto risco (FR A); o mesmo não é recomendado em mulheres de baixo risco (FR A).
Uma limitação importante, referida pelos autores da maior parte dos estudos incluídos nesta revisão, reside na disparidade de critérios para definir mulheres grávidas de alto e de baixo risco para pré-eclâmpsia, o que leva os autores a sugerir a realização de mais estudos para perceber concretamente quais os fatores que conferem maior risco para esta doença.11,13,16,20 Alguns trabalhos definem com clareza quais os fatores de risco que motivaram a inclusão dos diferentes estudos, definindo como mulheres de alto risco aquelas com, pelo menos, um fator de risco para pré-eclâmpsia e mulheres de baixo risco aquelas que não apresentam nenhum desses fatores.11-12 A NICE, na sua NOC de 2011,20 e a Cochrane, na sua RS de 2007,16 fazem uma divisão diferente dos fatores de risco, considerando fatores de alto risco e fatores de risco moderado para pré-eclâmpsia. As Tabelas I e II apresentam todos os fatores de risco para pré-eclâmpsia considerados nos estudos incluídos nesta revisão.
Dose de AAS
Ruano e colaboradores11 e Trivedi12 analisaram, nas suas MA, a correlação entre as dosagens de AAS utilizadas nos diferentes estudos incluídos e a prevenção da pré-eclâmpsia, não havendo correlação em nenhum dos trabalhos. Os autores não conseguem, assim, tirar conclusões acerca da melhor dose de AAS para prevenção da pré-eclâmpsia, recomendando de forma genérica AAS em baixa-dose, sem especificar a dose. Da mesma forma, Henderson e colaboradores13 não foram capazes de demonstrar qual a dose ótima de AAS a administrar. Por sua vez, o ECAC de Ayala e colaboradores14 utilizou na sua intervenção 100mg de AAS por dia, concluindo que esta será a dose mínima recomendada para a prevenção da pré-eclâmpsia em mulheres de alto risco.
A USPSTF18 e a ISSHP19 são consensuais em recomendar o uso de AAS em baixa dose para a prevenção da pré-eclâmpsia em mulheres de alto risco. A USPSTF18 conclui com moderada certeza haver evidência substancial para recomendar o uso de AAS na dose de 60 a 150mg/dia (FR B), enquanto a ISSHP19 conclui haver razoável evidência para recomendar o uso de AAS na dose de 75 a 162mg/dia (FR B). Gillon e colaboradores21 na sua RS das recomendações de NOC internacionais recomendam o uso de AAS na dose de 60 a 162mg/dia (FR A). Por sua vez, a NICE20 considera que a dose mínima recomendada de AAS deverá ser 75mg/dia, tendo em conta o perfil de segurança demonstrado do AAS nesta dose e a magnitude de redução do risco de pré-eclâmpsia (FR A). Por apurar fica o eventual benefício de doses mais elevadas de AAS em mulheres de alto risco.
Idade gestacional de início do AAS
Para além de analisar a correlação entre a dosagem de AAS e a prevenção da pré-eclâmpsia, Ruano e colaboradores11 procuram também analisar a correlação entre as idades gestacionais de início do tratamento com AAS e a prevenção da pré-eclâmpsia, não encontrando qualquer tipo de correlação. Os autores não conseguem, assim, concluir acerca da melhor altura para iniciar o tratamento com AAS. Da mesma forma, Henderson e colaboradores13 e Trivedi12 não conseguiram avaliar a influência da idade gestacional de início da intervenção no outcome final. Por sua vez, o ECAC de Ayala e colaboradores14 iniciou a sua intervenção até às 16 semanas de gestação inclusive, concluindo que o AAS deve ser iniciado no máximo até esta idade gestacional. Da mesma forma, Roberge e Giguère e colaboradores17 incluíram, na sua MA, ECAC cuja intervenção era iniciada até às 16 semanas de gestação, concluindo que o AAS deve ser iniciado até às 16 semanas de gestação, inclusive, para prevenção da pré-eclâmpsia em mulheres de alto risco.
Bujold e colaboradores9 realizaram uma MA com o objetivo de avaliar especificamente a influência da idade gestacional de início do AAS na incidência de pré-eclâmpsia. Para tal selecionaram ensaios clínicos prospetivos, controlados e randomizados, cuja intervenção consistia no uso de AAS em baixa dose, isoladamente ou em associação com dipiridamol, controlado com placebo ou nenhum tratamento, numa amostra de mulheres de alto risco para pré-eclâmpsia. Para atingir os objetivos propostos, os autores estratificaram os resultados de acordo com a idade gestacional de início da intervenção: até às 16 semanas inclusive ou após as 16 semanas de gestação. Os autores concluem haver uma redução significativa da incidência de pré-eclâmpsia quando o AAS é iniciado até às 16 semanas de gestação inclusive (RR=0,47; IC95%, 0,34-0,65), não havendo diferenças na incidência de pré-eclâmpsia no subgrupo de mulheres que iniciou a intervenção após as 16 semanas de gestação (RR=0,81; IC95%, 0,63-1,03). Ficou ainda por demonstrar se existe uma idade gestacional a partir da qual não existe benefício em iniciar AAS. Para diminuir vieses, os autores excluíram artigos quasi-randomizados, falhas na dupla ocultação e perdas de follow-up superiores a 20%. Neste contexto foi atribuído ao estudo NE 1.
Roberge e Villa e colaboradores8 conduziram uma MA com o objetivo de avaliar o benefício do AAS em baixa dose, iniciado também até às 16 semanas de gestação, no risco de desenvolvimento de pré-eclâmpsia pré-termo e de pré-eclâmpsia de termo. Os autores definem pré-eclâmpsia pré-termo como aquela que se associa a parto até às 37 semanas completas de gestação e pré-eclâmpsia de termo aquela que se associa a parto após as 37 semanas de gestação. Para atingir os objetivos propostos, os autores incluíram ECAC cuja intervenção consistia no uso de AAS em baixa dose, com ou sem dipiridamol, controlado com placebo ou nenhum tratamento, em mulheres grávidas com risco de pré-eclâmpsia (independentemente do grau de risco) e com a idade gestacional supracitada. Os autores verificaram que o início de AAS em baixa dose até às 16 semanas de gestação, inclusive, resultou numa diminuição de 89% no risco de pré-eclâmpsia pré-termo (RR=0,11 com IC95%, 0,04-0,33; p<0,01), não havendo diferenças no risco de pré-eclâmpsia de termo (RR=0,98 com IC95%, 0,42-2,33; p=0,97). Os autores justificam os resultados obtidos com a grande heterogeneidade (54%) entre os estudos que avaliaram o risco de pré-eclâmpsia de termo, colocando ainda a hipótese de a terapêutica com AAS diminuir o risco de pré-eclâmpsia grave, ou seja, aquela que se associa a parto pré-termo, não reduzindo o risco de pré-eclâmpsia moderada, ou seja, aquela que permite partos de termo. Esta MA cumpre critérios de boa qualidade, pelo que lhe foi atribuído NE 1.
A USPSTF18 conclui com moderada certeza haver evidência substancial para recomendar o início de AAS após as 12 semanas de gestação em mulheres grávidas de alto risco para pré-eclâmpsia (FR B), não se manifestando sobre a idade gestacional até à qual deve ser mantida a terapêutica com AAS. Da mesma forma, a NICE20 considera importante o início do AAS às 12 semanas de gestação em mulheres de alto risco para pré-eclâmpsia, referindo ter sido esta a idade gestacional mais precoce para a qual foi identificado benefício do uso de AAS (FR A). Relativamente à descontinuação do tratamento, a NICE20 refere não existir evidência de qual será a idade gestacional ótima. A ISSHP19 refere haver razoável evidência para recomendar que o AAS seja iniciado logo após o diagnóstico de gravidez e antes das 16 semanas de gestação (FR B) e evidência inconsistente para recomendar a manutenção da terapêutica com AAS até ao parto (FR C). Gillon e colaboradores,21 na sua RS das recomendações de NOC internacionais, recomendam o início do AAS logo no início da gravidez que deve ser mantido até ao parto (FR A).
Hora de administração do AAS
Para além de avaliar o efeito do AAS na prevenção da pré-eclâmpsia em mulheres de alto risco, Ayala e colaboradores14 procuraram também perceber se esse efeito estaria dependente da hora de administração. Para tal conduziram um estudo prospetivo, randomizado e duplamente cego, tendo randomizado 350 mulheres em seis grupos, de acordo com o tratamento (AAS ou placebo) e a hora de administração (ao acordar, oito horas depois de acordar e ao deitar). Os resultados foram analisados para a comparação “AAS vs placebo” e, posteriormente, para a comparação “AAS ao deitar ou oito horas após acordar vs AAS de manhã ou placebo”. Quando comparado com o placebo, o AAS, independentemente da hora de administração, reduziu ligeiramente a incidência de pré-eclâmpsia (NNT=16). Este efeito é claramente ampliado quando a ingestão do AAS é feita à tarde ou ao deitar (NNT=9), levando os autores a recomendar a administração de AAS ao deitar, para prevenção da pré-eclâmpsia.
A ISSHP19 é a única NOC a emitir recomendações sobre a hora de administração do AAS, referindo haver evidência razoável para recomendar que a administração de AAS seja feita ao deitar (FR B).
Perfil de segurança do AAS
Uma das principais preocupações relacionadas com a terapêutica com AAS durante a gravidez é a possibilidade de um aumento de complicações hemorrágicas na grávida ou no recém-nascido.15 Estas preocupações são em parte dissipadas por alguns dos estudos incluídos nesta revisão.
A incidência de descolamento prematuro da placenta, de hemorragia anteparto e de hemorragia pós-parto com a terapêutica com AAS foram consistentemente avaliados em vários trabalhos. Rossi e colaboradores10 verificaram a ocorrência materna de descolamento da placenta e necessidade de transfusão sanguínea em dois estudos envolvendo mulheres de alto risco e em dois outros estudos envolvendo mulheres de baixo risco. Contudo, não encontraram diferenças entre as mulheres grávidas tratadas com AAS e as tratadas com placebo (AAS em baixa dose: 28/752 (3,7%) vs placebo: 26/772 (3,3%); Z=0,36; P=0,72; OR=1,10 com IC95%, 0,60-1,90), indicando que o AAS em baixa dose é seguro (NE 2). Da mesma forma, Bujold e colaboradores9 e Henderson e colaboradores13 não encontraram diferenças significativas na incidência de descolamento da placenta (RR=0,62 com IC95%, 0,08-5,039 e RR=1,17 com IC95%, 0,93-1,48,13 respetivamente). Henderson e colaboradores13 ressalvam, contudo, que as baixas taxas de eventos reportados podem ter induzido vieses importantes na interpretação deste outcome. Por este motivo e para este outcome foi atribuído a este trabalho NE 2.
Em relação à incidência de hemorragia pós-parto, Henderson e colaboradores13 e Ayala e colaboradores14 não encontraram diferenças entre os grupos tratados com AAS e os tratados com placebo (RR=1,02 com IC95%, 0,96-1,0913 e p=0,303,14 respetivamente) (NE 1), resultados corroborados por Trivedi12 na sua metanálise de 2011 (NE 2). Em relação à incidência de hemorragia anteparto, Ayala e colaboradores14 não encontraram diferenças significativas entre o AAS em baixa dose e o placebo (p=0,415) (NE 1). Rossi e colaboradores10 não conseguiram avaliar a relação entre hemorragia anteparto e pós-parto e o uso de AAS para profilaxia da pré-eclâmpsia, pelas disparidades encontradas na definição de hemorragia pós-parto entre os estudos incluídos e pela elevada subjetividade na avaliação das perdas sanguíneas.
Askie e colaboradores15 e Duley e colaboradores16 avaliaram o efeito e a segurança não só do AAS, como também de outros agentes antiplaquetários na prevenção da pré-eclâmpsia. Nenhum dos trabalhos encontrou diferenças na incidência de descolamento prematuro da placenta (RR=1,13 com IC95%, 0,87-1,4815 e RR=1,10, IC95%, 0,89-1,37,16 respetivamente). Paralelamente, Askie e colaboradores15 não encontraram diferenças na incidência de hemorragia anteparto (RR=1,02, com IC95%, 0,90-1,15) e na incidência de hemorragia pós-parto (RR=1,06 com IC95%, 1,00-1,13). Os autores sublinham, no entanto, que as conclusões relativas à incidência de hemorragia pós-parto devem ser interpretadas com cautela, pelas dificuldades na mensuração e definição de hemorragia pós-parto nos diferentes estudos incluídos. Por este motivo e para estes outcomes foi atribuído a este trabalho NE 2.
A incidência de hemorragia neonatal e a possibilidade de ocorrência de anomalias do desenvolvimento são outras das preocupações associadas à exposição ao AAS durante a gestação. Relativamente ao primeiro outcome, Trivedi12 e Duley e colaboradores16 não encontraram diferenças significativas na incidência de hemorragia neonatal (NE 2). Em relação ao segundo outcome, Henderson e colaboradores13 e Duley e colaboradores16 não relataram potenciais efeitos prejudiciais ou diferenças no desenvolvimento até aos 18 meses de idade, salvaguardando que efeitos raros ou a longo prazo não foram identificados e que mais estudos são necessários (NE 2). Da mesma forma, Askie e colaboradores15 não relatam aumento do risco de anomalias congénitas, nem problemas no desenvolvimento até cerca dos dois anos de idade (NE 2).
As NOC incluídas nesta revisão são consensuais em afirmar a segurança do AAS em baixa dose.18-20 A USPSTF18 refere que esta terapêutica não está associada à ocorrência de descolamento prematuro da placenta, hemorragia pós-parto ou danos fetais, como hemorragia intracraniana e anomalias congénitas, enquanto a ISSHP19 refere que a terapêutica com AAS não aumenta nem diminui o risco de abortamento espontâneo, não havendo evidência de teratogenicidade ou outros efeitos adversos pediátricos a curto ou a longo prazo.
Conclusões
De acordo com a evidência atual disponível, pode concluir-se que o AAS em baixa dose tem benefício quando usado como medicação preventiva nas mulheres em risco de pré-eclâmpsia, com evidência clara do seu benefício nas mulheres de alto risco (FR A). Não existe, contudo, evidência suficiente para recomendar esta profilaxia nas mulheres de baixo risco (FR A). Estas conclusões são suportadas por um elevado número de estudos, a maioria de boa qualidade, com resultados consistentes e orientados para o paciente.
Globalmente, as RS e MA de boa qualidade incluídas nesta revisão demonstraram que o uso de AAS em baixa dose conduzia a reduções significativas do risco relativo de pré-eclâmpsia em mulheres de alto risco.9,11,13,16 Apenas uma RS com NE 2 não encontrou evidência suficiente para suportar o uso desta profilaxia nas mulheres em risco de pré-eclâmpsia, independentemente do seu grau de risco.10 Os estudos que analisaram separadamente as mulheres de baixo risco na população-alvo verificaram uma ausência de benefício do AAS neste subgrupo de mulheres.10-12
Relativamente à dose de AAS a administrar, os estudos são consensuais em recomendar AAS em baixa dose (FR A).11-14 Contudo, a maior parte dos estudos inclui ECAC com disparidades importantes nas dosagens de AAS, pelo que à luz da evidência disponível não é possível determinar a dose ótima de AAS a ministrar para prevenção da pré-eclâmpsia.
No que respeita à idade gestacional de início da terapêutica profilática com AAS, não existe consenso entre os estudos, que apresentam critérios de inclusão divergentes relativamente a este parâmetro. Ruano e colaboradores11, Henderson e colaboradores13 e Trivedi12 não conseguiram determinar a idade gestacional ótima para início da profilaxia com AAS. Não obstante, a MA de Bujold e colaboradores9 e o ECAC de Ayala e colaboradores,14 dois estudos de boa qualidade com NE 1, concluem haver maior benefício no início da terapêutica com AAS até às 16 semanas de gestação inclusive, sendo esta a idade gestacional recomendada para início da profilaxia (FR A).
O ECAC de Ayala e colaboradores14 foi o único estudo a avaliar objetivamente o efeito da cronoterapia com AAS na prevenção da pré-eclâmpsia. À luz deste estudo de boa qualidade (NE 1) é possível recomendar, com uma FR B, que a profilaxia com AAS seja administrada preferencialmente ao deitar.
Alguns estudos avaliaram ainda a incidência de efeitos adversos relacionados com a terapêutica, verificando que o uso de AAS em baixa dose não esteve associado a aumento da incidência de efeitos adversos, sendo, à partida, seguro na população em estudo (FR B). De facto, os estudos não encontraram diferenças na incidência de descolamento prematuro da placenta, de hemorragia anteparto e pós-parto, nem na incidência de hemorragia neonatal ou anomalias do desenvolvimento. É de salvaguardar, contudo, a possibilidade de vieses importantes na interpretação destes outcomes, sendo necessários mais estudos a longo prazo para avaliar estes e outros potenciais efeitos adversos que, pela sua raridade, necessitam de um follow-up mais alargado.
Uma limitação importante e fonte de heterogeneidade da maior parte dos estudos incluídos nesta revisão reside na disparidade de critérios para definir mulheres grávidas de alto e de baixo risco para desenvolvimento de pré-eclâmpsia, sendo necessários mais estudos para aferir quais os fatores que conferem maior risco para esta doença.
A pré-eclâmpsia é uma das mais graves patologias obstétricas, estando associada a complicações graves e a morbimortalidade materna e fetal, devendo o médico de família estar sensibilizado para o seu rastreio e abordagem. As conclusões deste trabalho podem, assim, melhorar os cuidados às grávidas em risco de pré-eclâmpsia, reduzindo o risco de complicações e melhorando os outcomes maternos e fetais.
No entanto, subsistem ainda algumas dúvidas relativas ao uso de AAS na prevenção da pré-eclâmpsia. Assim sendo, são necessários mais estudos para esclarecer quais os fatores que conferem maior risco para esta patologia, para perceber qual a melhor altura para iniciar a profilaxia com AAS e qual a dose mais adequada. São ainda necessários estudos de boa qualidade para reafirmar a segurança do AAS na população obstétrica.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Duley L, Henderson-Smart D, Knight M, King J. Antiplatelet drugs for prevention of pre-eclampsia and its consequences: systematic review. BMJ. 2001;322(7282):329-33. [ Links ]
2. World Health Organization. Geographic variation in the incidence of hypertension in pregnancy: World Health Organization international collaborative study of hypertensive disorders of pregnancy. Am J Obstet Gynecol. 1988;158(1):80-3. [ Links ]
3. Khan KS, Wojdyla D, Say L, Gülmezoglu AM, Van Look PF. Who analysis of causes of maternal death: a systematic review. Lancet. 2006;367(9516):1066-74. [ Links ]
4. Tranquilli AL, Dekker G, Magee L, Roberts J, Sibai BM, Steyn W, et al. The classification, diagnosis and management of the hypertensive disorders of pregnancy: a revised statement from the ISSHP. Pregnancy Hypertens. 2014;4(2):97-104. [ Links ]
5. Mol BW, Roberts CT, Thangaratinam S, Magee LA, de Groot CJ, Hofmeyr GJ. Pre-eclampsia. Lancet. 2016;387(10022):999-1011. [ Links ]
6. Khong TY, De Wolf F, Robertson WB, Brosens I. Inadequate maternal vascular response to placentation in pregnancies complicated by pre-eclampsia and by small-for-gestational age infants. Br J Obstet Gynaecol. 1986;93(10):1049-59. [ Links ]
7. Schiff E, Peleg E, Goldenberg M, Rosenthal T, Ruppin E, Tamarkin M, et al. The use of aspirin to prevent pregnancy-induced hypertension and lower the ratio of thromboxane A2 to prostacyclin in relatively high risk pregnancies. N Engl J Med. 1989;321(6):351-6. [ Links ]
8. Roberge S, Villa P, Nicolaides K, Giguère Y, Vainio M, Bakthi A, et al. Early administration of low-dose aspirin for the prevention of preterm and term preeclampsia: a systematic review and meta-analysis. Fetal Diagn Ther. 2012;31(3):141-6. [ Links ]
9. Bujold E, Roberge S, Lacasse Y, Bureau M, Audibert F, Marcoux S, et al. Prevention of preeclampsia and intrauterine growth restriction with aspirin started in early pregnancy: a meta-analysis. Obstet Gynecol. 2010;116(2 Pt 1):402-14. [ Links ]
10. Rossi AC, Mullin PM. Prevention of pre-eclampsia with low-dose aspirin or vitamins C and E in women at high or low risk: a systematic review with meta-analysis. Eur J Obstet Gynecol Reprod Biol. 2011;158(1):9-16. [ Links ]
11. Ruano R, Fontes RS, Zugaib M. Prevention of preeclampsia with low-dose aspirin: a systematic review and meta-analysis of the main randomized controlled trials. Clinics (Sao Paulo). 2005;60(5):407-14. [ Links ]
12. Trivedi NA. A meta-analysis of low-dose aspirin for prevention of preeclampsia. J Postgrad Med. 2011;57(2):91-5. [ Links ]
13. Henderson JT, Whitlock EP, O'Connor E, Senger CA, Thompson JH, Rowland MG. Low-dose aspirin for the prevention of morbidity and mortality from preeclampsia: a systematic evidence review for the U.S. Preventive Services Task Force. Ann Intern Med. 2014;160(10):695-703. [ Links ]
14. Ayala DE, Ucieda R, Hermida RC. Chronotherapy with low-dose aspirin for prevention of complications in pregnancy. Chronobiol Int. 2013;30(1-2):260-79. [ Links ]
15. Askie LM, Duley L, Henderson-Smart DJ, Stewart LA. Antiplatelet agents for prevention of pre-eclampsia: a meta-analysis of individual patient data. Lancet. 2007;369(9575):1791-8. [ Links ]
16. Duley L, Henderson-Smart DJ, Meher S, King JF. Antiplatelet agents for preventing pre-eclampsia and its complications. Cochrane Database Syst Rev. 2007;(2):CD004659. [ Links ]
17. Roberge S, Giguère Y, Villa P, Nicolaides K, Vainio M, Forest JC, et al. Early administration of low-dose aspirin for the prevention of severe and mild preeclampsia: a systematic review and meta-analysis. Am J Perinatol. 2012;29(7):551-6. [ Links ]
18. LeFevre ML. Low-dose aspirin use for the prevention of morbidity and mortality from preeclampsia: U.S. Preventive Services Task Force Recommendation Statement. Ann Intern Med. 2014;161(11):819-26. [ Links ]
19. Magee LA, Pels A, Helewa M, Rey E, von Dadelszen P. Diagnosis, evaluation, and management of the hypertensive disorders of pregnancy. Pregnancy Hypertens. 2014;4(2):105-45. [ Links ]
20. National Collaborating Centre for Women’s and Children’s Health, National Institute for Health and Clinical Excellence. Hypertension in pregnancy: the management of hypertensive disorders during pregnancy (Internet). London: Royal College of Obstetricians and Gynaecologists; 2011. [ Links ] Available from: http://www.ncbi.nlm.nih.gov/books/NBK62649/?report=classic
21. Gillon TE, Pels A, von Dadelszen P, MacDonell K, Magee LA. Hypertensive disorders of pregnancy: a systematic review of international clinical practice guidelines. PLoS One. 2014;9(12):e113715. [ Links ]
Endereço para correspondência | Dirección para correspondencia | Correspondence
Sara Santos Ferreira
USF Infesta, Unidade Local de Saúde de Matosinhos
E-mail: sara_danielapk@hotmail.com
Conflitos de interesse
Os autores declaram não ter conflitos de interesse.
Financiamento do estudo
Os autores declaram que o trabalho relatado neste manuscrito não foi objeto de qualquer tipo de financiamento externo.
Conflitos de interesse
Os autores declaram não ter conflitos de interesse.
Financiamento do estudo
Os autores declaram que o trabalho relatado neste manuscrito não foi objeto de qualquer tipo de financiamento externo.
Recebido em 03-02-2016
Aceite para publicação em 22-12-2016