Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Angiologia e Cirurgia Vascular
versão impressa ISSN 1646-706X
Angiol Cir Vasc vol.13 no.2 Lisboa jun. 2017
ARTIGO REVISÃO
Anticoagulantes orais diretos: um novo paradigma no tratamento da trombose venosa profunda
Direct oral anticoagulants:a new paradigmin deep vein thrombosis treatment
Bruna Guimarãesa, Luciana Ricca Gonçalvesb, Armando Mansilhac
a Estudante do 6ºAno de Mestrado Integrado em Medicina, Faculdade de Medicinada Universidade do Porto, Porto, Portugal
b Serviço de Imunohemoterapia, Centro Hospitalar de São João, Faculdade de Medicina da Universidade do Porto, Porto, Portugal
c Serviço de Angiologia e Cirurgia Vascular, Centro Hospitalar de São João, Faculdade de Medicina da Universidade do Porto, Porto, Portugal
RESUMO
A trombose venosa profunda (TVP) é uma patologia com elevada mortalidade e morbilidade, sendo importante ser reconhecida e tratada de forma eficaz e precoce. Os anticoagulantes orais diretos (DOAC), que inibem seletivamente e de forma reversível o fator IIa (Dabigatrano) ou o fator Xa (Rivaroxabano, Apixabano e Edoxabano), tornaram-se uma alternativa atrativa à terapêutica convencional devido à sua administração oral em doses fixas, sem interações alimentares e ausência de necessidade de monitorização. O objetivo deste trabalho é o de proceder a uma revisão sobre o uso terapêutico dos DOAC e da sua relação risco/benefício comparativamente à terapêutica convencional no tratamento e prevenção da TVP. Foi efetuada uma pesquisa na base de dados Pubmed de artigos em língua inglesa que abordassem os DOAC no tratamento e prevenção secundária da TVP. Foram incluídos os principais ensaios clínicos e as mais recentes orientações para o tratamento e prevenção do Tromboembolismo Venoso (TEV). Grandes ensaios clínicos randomizados demonstraram a não-inferioridade dos DOAC no perfil de eficácia comparativamente à terapêutica convencional com a vantagem de apresentarem uma segurança superior. A melhor relação risco/ benefício dos DOAC aliada às previsíveis propriedades farmacocinéticas e ausência de necessidade de monitorização por rotina, proporciona-lhes uma melhor relação custo-eficácia. Apesar de nem todos os doentes beneficiarem desta terapêutica, que deve ser individualizada em cada caso, os DOAC tornaram o tratamento e prevenção da TVP mais prático e seguro, com um aumento da satisfação e diminuição da incidência de eventos recorrentes, iniciando um novo paradigma no tratamento e prevenção da TVP.
Palavras-chave: Anticoagulantes Orais Diretos; Trombose Venosa Profunda; Dabigatrano; Rivaroxabano; Apixabano; Edoxabano.
ABSTRACT
The deep vein thrombosis (DVT) is a high morbility pathology if not properly diagnosed and treated at its early-stage. The direct oral anticoagulants (DOACs), which selectly inhibit factor lla (dabigratan) or factor Xa (rivaroxaban, apixaban and edoxaban), have become an attractive alternative to conventional therapy due to their fixed doses, no food interactions and absence of monitoring. The aim of this work is to procced with a revision on the therapeutic use of DOACs and their risk/benefit correlation in comparison to conventional therapy in the DVT treatment and prevention. It was conducted a search on Pubmed database of English-language articles that addressed the DOACs in treatment and secondary prevention of DVT. It were also included the major clinical trials and the latest guidelines for the treatment and prevention of Venous Thromboembolism (VTE).
Large randomized studies stated the non-inferiority of DOACs in the efficiency profile in comparison to conventional therapy, with the advantage of providing a higher safety profile. The improved risk/benefit ratio of DOACs combined with predictable pharmacokinetic properties and the absence of monitoring allow a better relation cost/efficiency. Although not all patients benefit from this therapy, which should be individualized in each case, the DOACs have changed DVT treatment and prevention into a more practical and safer procedure, associated with a higher patient satisfaction and a decrease in recurrent events incidence, launching a new paradigm in DVT treatment and prevention.
Keywords: Direct oral anticoagulants; Deep vein thrombosis; Dabigatran; Rivaroxaban; Apixaban; Edoxaban
O Tromboembolismo Venoso (TEV) é a terceira principal causa de morte por doença vascular, a seguir ao enfarte agudo do miocárdio e ao acidente vascular cerebral, e apresenta como principais manifestações a trombose venosa profunda (TVP) e a embolia pulmonar (EP)1. A TVP tem uma incidência anual de 1 a 2 casos por 1000 na população geral2. A idade é um fator importante considerando que a prevalência de TVP aumenta substancialmente após os 40 anos. A presença confirmada de uma TVP sugere uma pronta instituição da terapêutica anticoagulante, com os objetivos de impedir a progressão e migração do trombo, reduzir os episódios de recorrência e a incidência de síndrome pós-trombótico3. Até recentemente, a terapêutica anticoagulante convencional era representada por um tratamento anticoagulante parentérico inicial (heparina de baixo peso molecular (HBPM), heparina não fracionada (HNF) ou fondaparinux), durante pelo menos 5 dias, sobreposto e seguido por um antagonista da vitamina K (AVK), durante pelo menos 3 meses (prevenção secundária) ou por tempo indefinido (prevenção a longo-prazo)4. A duração da terapêutica é dependente do risco de recorrência e influenciada pelo risco de hemorragia e preferência do doente 2. Os doentes com TEV no contexto de um fator de risco transitório, cirúrgico ou não, apresentam um menor risco de recorrência após interrupção da anticoagulação, comparativamente a um doente com TEV idiopático que apresenta um risco de recorrência de 30% aos 5 anos, após inter-romper a terapia anticoagulante5. O risco de recorrência deve ser analisado em conjunto com o risco hemorrágico do doente categorizado como baixo (sem fatores de risco; risco hemorragia major 0.8% ao ano), moderado (um fator de risco; risco de hemorragia major 1.6% ao ano) ou elevado (dois ou mais fatores de risco; risco de hemorragia major igual ou superior a 6.5% ao ano)5. De acordo com as recomendações da 10ª edição do American College of Chest Physician5:
- doentes com um primeiro episódio de TVP secundário a um fator de risco transitório, cirúrgico ou não, é recomendada terapêutica anticoagulante por um período de 3 meses;5
- doentes com um primeiro episódio de TVP idiopático é recomendada terapêutica anticoagulante por um período de 3 meses. Após esse período, deve ser avaliado o risco/benefício da extensão do tratamento por duração indeterminada5:
• doentes com TVP idiopática proximal com baixo ou moderado risco hemorrágico têm indicação para a extensão do tratamento, ao contrário dos doentes com TVP idiopática proximal com elevado risco hemorrágico que deverão realizar apenas 3 meses de terapia anticoagulante;5
• doentes com TVP distal deverão efetuar apenas 3 meses de terapêutica anticoagulante, independentemente da etiologia idiopática ou não.5
doentes com um episódio recorrente de TVP com baixo ou moderado risco hemorrágico têm indicação para a extensão da terapêutica anticoagulante. Se elevado risco hemorrágico que devem suspender a terapêutica anticoagulante ao fim de 3 meses.5 Apesar da eficácia comprovada da terapêutica anticoagulante convencional, a necessidade de administração parentérica, a monitorização frequente, a estreita janela terapêutica, as múltiplas interações alimentares e medicamentosas e os múltiplos polimorfismos genéticos que influenciam a resposta à varfarina são inconvenientes que limitam a sua adesão e prescrição.3 Nos últimos anos, estas limitações subjacentes à terapêutica convencional abriram uma oportunidade para o desenvolvimento de fármacos anticoagulantes alternativos — anticoagulantes orais diretos (DOAC) — para uma anticoagulação mais segura, eficaz e prática para o doente. Os DOAC, com eficácia e segurança comparável ou superior, inibem fatores específicos da cascata da coagulação: factor IIa (dabigatrano) e o factor Xa (rivaroxabano, apixabano e edoxabano)2 (Figura 1).
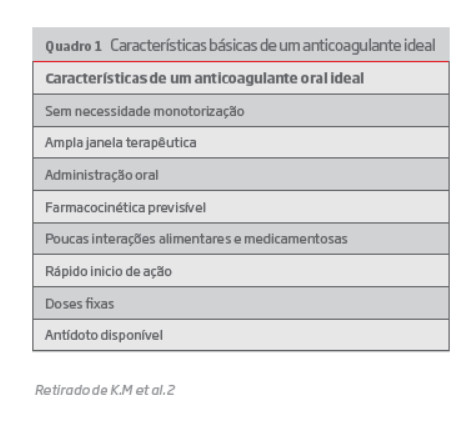
Estes fármacos, sem efeitos diretos na agregação plaquetária e em outras serinas de protéases, são administrados por via oral sem necessidade de monitorização, apresentam um curto tempo de semi-vida, poucas interações medicamentosas e ausência de interações alimentares.4 Estas vantagens face aos fármacos convencionais estão associadas a uma maior conveniência terapêutica e uma maior proximidade com as características de um anticoagulante oral ideal (quadro 1) destacando um novo paradigma para o tratamento e prevenção da TVP.
O objetivo deste trabalho é o de proceder a uma revisão sobre o uso dos anticoagulantes orais diretos: dabigatrano, rivaroxabano, apixabano e edoxabano (comparativamente com a terapêutica convencional) no tratamento e prevenção da trombose venosa profunda, particularmente no que concerne às suas características farmacológicas, eficácia, segurança e relação risco/benefício do seu uso terapêutico.
MATERIAL E MÉTODOS
Foi efetuada uma pesquisa bibliográfica na base de dados Pubmed, limitada a artigos em Língua Inglesa, de 2011 ao presente, com o termo de pesquisa “DOAC AND NOAC AND Deep Venous Thrombosis OR DVT”. Os artigos foram selecionados após leitura do respetivo abstract, tendo sido atribuída prioridade de inclusão a artigos de revisão e aos principais ensaios clínicos de avaliação da eficácia e segurança dos DOAC.
Foram ainda incluídos outros artigos não abrangidos pelos resultados de pesquisa, com relevância para o assunto em epígrafe, citados como referência de outros artigos.
Assim, na presente revisão foram incluídos 49 artigos dos quais foi retirada informação pertinente para responder aos objetivos propostos na introdução.
RESULTADOS
TERAPÊUTICA ANTICOAGULANTE CONVENCIONAL
A anticoagulação constitui a base do tratamento bem sucedido da TVP. A terapêutica anticoagulante convencional é iniciada por um fármaco anticoagulante parentérico (heparina não fraccionada (HNF) e heparinas de baixo peso molecular (HBPM) ou fondaparinux) mantido por um período mínimo de 5 dias como transição para uma anticoagulação estável de longo prazo com um antagonistas da vitaia K (AVK).4
As heparinas atuam por um mecanismo de ação indireto através da ligação à antitrombina (AT), ativando-a e potenciando a sua função no sentido de inibir os fatores de coagulação IIa (trombina) e Xa e, em menor proporção, IXa, XIa e XIIa.6
A HNF é administrada normalmente por infusão intravenosa contínua e tem um curto tempo de semi-vida (1,5 horas).
No entanto, apresenta várias limitações, nomeadamente a necessidade de frequente monitorização do efeito anticoagulante
pelo tempo de tromboplastina parcial ativado (aPTT) e um risco de 0.5 a 5% de trombocitopenia induzida
pela heparina (TIH).2
A HBPM, apesar de um mecanismo de ação similar tem uma maior ação inibitória sobre o fator Xa comparativamente ao fator IIa.
Apresenta uma melhor razão risco/benefício com um efeito anticoagulante mais consistente, uma administração subcutânea e ausência de necessidade de monitorização por rotina. Além disso, comparativamente à HNF, foi associada a uma diminuição de 5 vezes de TIH, das taxas de mortalidade, de TEV recorrente e de hemorragia major.3
O fondaparinux é um análogo sintético do pentassacarídeo ligado à AT, encontrado nas heparinas, e foi o primeiro inibidor seletivo do fator Xa a surgir. Este fármaco é administrado por via subcutânea uma vez ao dia e apresenta uma eficácia e segurança semelhante à HBPM.7
Os AVK atuam por um mecanismo de ação indireto através da ligação à vitamina K epóxido-redutase, impedindo a ativação por carboxilação dos fatores de coagulação dependentes desta vitamina: II, VII, IX e X (e também a proteína C e a proteína S). No entanto, como a semi-vida de cada um destes fatores é diferente, um estado de hipercoagulabilidade transitório, devido à redução das proteínas C e S, precede o efeito antitrombótico, sendo atingido um nível de anticoagulação estável após 36–72 horas do início da administração do fármaco, o que explica a necessidade da sobreposição terapêutica com um anticoagulante parentérico por um período mínimo de 5 dias e até que dois valores sequenciais de INR (International Normalized Ratio) com intervalo de pelo menos um dia, alcancem o intervalo terapêutico alvo (2–3).7, 8
A varfarina é o AVK mais utilizado com eficácia comprovada.
No entanto, apresenta inúmeras desvantagens (quadro 2) que limitam o seu uso e a adesão à terapêutica: inicio e fim de ação lentos, uma estreita janela terapêutica, propriedades farmacocinéticas e farmacodinâmicas que originam respostas variáveis e uma grande variabilidade de respostas inter e intra individuais, influenciada também por polimorfismos genéticos (CYP2C9 e subunidade 1 do complexo vitamina K epóxido-redutase — VKORC1) e por numerosas interações alimentares e medicamentosas. Estas características conduzem à necessidade de monitorização da terapêutica através do INR (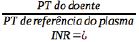 )ISI).3
)ISI).3

Uma meta-análise demonstrou que a varfarina diminui o risco de um episódio recorrente de TVP em 85% comparativamente ao placebo.8 No entanto, apresenta uma incidência de hemorragia intracraniana (HIC) de 0.1% a 0.5% e de hemorragia major de 1% a 2%2 A HIC é uma das causas mais graves de hemorragia associada à varfarina. Não obstante, o seu risco é variável e depende de uma série de fatores, incluindo a idade e intensidade da anticoagulação5.
O risco de um evento tromboembólico aumenta significativamente para valores de INR inferiores a 1.8 e a taxa de HIC aumenta exponencialmente para valores superiores a 3.5.9 Por este motivo, a dose deve ser devidamente ajustada de acordo com a monitorização laboratorial periódica a que estes doentes estão sujeitos.10 Infelizmente, no geral cerca de 60% dos valores de INR mantém-se dentro do intervalo terapêutico (TTR)4, salientando a importância da educação do doente para o sucesso da terapêutica.
Em situações de hemorragia ou necessidade de cirurgia urgente a reversão do efeito da varfarina é efetuada de duas formas: administração endovenosa de vitamina K (“antídoto”) e/ou concentrado de complexo protrombínico (CCP).10 A restauração da hemóstase com vitamina K apresenta um efeito sustentado, visto que requer a síntese de novos fatores de coagulação pelo fígado, um processo que necessita pelo menos 6 horas e mais provavelmente 12–24horas para ter um impacto significativo na redução do INR.11 O CCP está associado a uma rápida e não sustentada reversão do efeito anticoagulante em 10–20 minutos
após a sua administração.11
As heparinas, fondaparinux e os AVK apresentam diversas limitações que tiveram de ser geridas durante longos anos e que impulsionaram o desenvolvimento de fármacos anticoagulantes alternativos tendo por base a teoria de que o aumento da seletividade do fármaco é diretamente proporcional à sua eficácia e segurança.2
ANTICOAGULANTES ORAIS DIRETOS (DOAC)
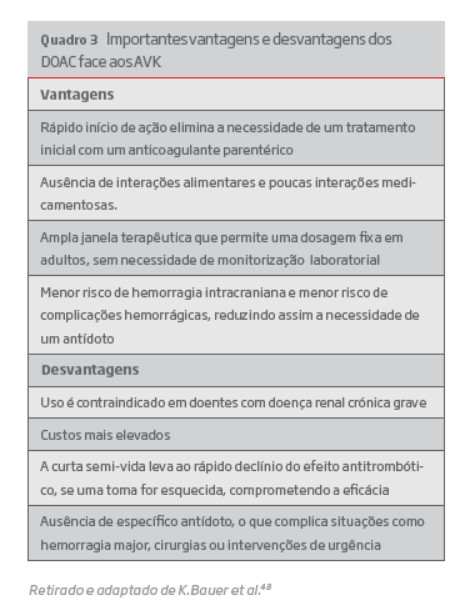
Durante a última década, os anticoagulantes orais diretos foram desenvolvidos como uma alternativa à terapêutica convencional para o tratamento e prevenção da TVP, através de um mecanismo de ação direto pela inibição seletiva do fator IIa (Dabigatrano, Pradaxa®) ou do fator Xa (Rivaroxabano, Xarelto®, Apixabano, Eliquis® ou Edoxabano, Lixiana®). (quadro 3)
De acordo com várias análises sistemáticas de ensaios clínicos randomizados que compararam o uso de DOAC com o placebo ou com a terapêutica convencional para a prevenção e tratamento da TVP, muitos autores, como exemplo Calvin H.Yeh et al.8, concluíram que, no geral, os DOAC apresentam eficácia e segurança igual ou superior, embora nem todos os grupos de doentes beneficiarão do seu uso. No entanto, não havendo estudos cegos que comparem os DOAC entre si, reconhecem que pode ser difícil apontar o mais indicado para cada doente, mas consideram importante que todo o médico se sinta capaz de usar pelo menos um deles com confiança.
INIBIDOR DIRETO DA TROMBINA (IDT)
Os IDT orais inibem diretamente e de forma reversível o Fator IIa (trombina) sem intervir noutros mecanismos pró-trombóticos. A trombina desempenha um papel fundamental na trombogénese associada à TVP. Esta protease serina, por proteólise, exibe atividades procoagulantes, pela conversão de fibrinogénio solúvel em fibrina insolúvel, e ativa outros fatores incluídos na cascata de coagulação, incluindo receptores das plaquetas ativados por protéases e o fator XIII, que, por sua vez, estabiliza o coágulo de fibrina.12 O IDT oral é uma molécula sintética univalente (liga-se ao domínio ativo da trombina) que inibe tanto a trombina livre como a ligada à fibrina e apresenta indiretamente um efeito antiplaquetário, uma vez que reduz a ativação das plaquetas mediada pela trombina. Para além disso, a atividade deste fármacos é independente da antitrombina, ao contrário das heparinas, não necessita de monitorização de rotina, tem uma baixa ligação às proteínas plasmáticas (35%) e uma resposta anticoagulante bastante mais previsível e consistente.13
Dabigatrano (Pradaxa®)
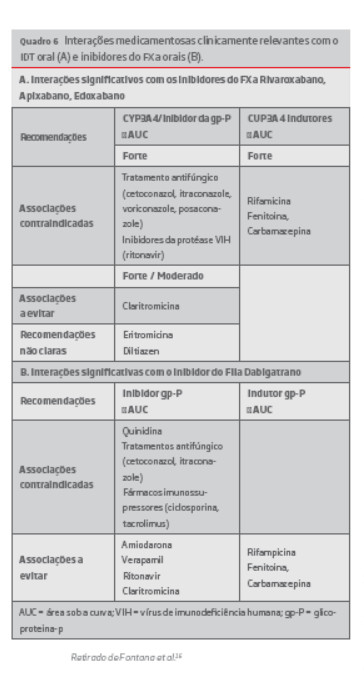
O dabigatrano etexilato é um pró-fármaco que rapidamente é convertido na sua forma ativa, dabigatrano, por esterases hepáticas e intestinais, após administração oral.14 É um inibidor competitivo, reversível, específico e univalente da trombina, administrado em doses fixas, sem necessidade de monitorização e que apresenta favoráveis propriedades farmacocinéticas e farmacodinâmicas.15 (Quadro 4) Em 2014, foi aprovado pela FDA (Food and Drug Administration) e pela EMA (European Medicines Agency) para o tratamento e prevenção secundária da TVP e EP, em adultos, na dose de 150 mg duas vezes ao dia após tratamento anticoagulante parentérico durante, pelo menos, 5 dias, com base na informação recolhida de quatro grandes estudos (RE-COVER, RE-COVER II, RE-SONATE e RE-MEDY).12 (Quadro 5) O Dabigatrano apresenta uma biodisponibilidade de apenas 6%. A concentração plasmática máxima é atingida após 2 horas e o tempo de semi-vida, em indivíduos saudáveis, varia entre 12–17 horas (Quadro 4). É excretado essencialmente por via renal (80%) e a sua semi-vida média apresenta uma relação inversa com a depuração da creatinina (ClCr); está contraindicado em doentes com ClCr inferior a 30mL/min.4, 12, 16 Apesar de um favorável perfil de interações alimentares e farmacológicas comparativamente aos AVK, o dabigatrano etexilato é um substrato da glicoproteína-P (gpP), que diminui a absorção oral de vários fármacos e/ou a sua reabsorção pelo nefrónio, funcionando como uma bomba de efluxo.14 Por este motivo, inibidores da gpP promovem fenómenos hemorrágicos, com aumento da biodisponibilidade de dabigatrano, por inibirem a sua excreção.13 Em contrapartida, indutores da gpP são responsáveis por fenómenos trombóticos dado diminuírem a biodisponibilidade de dabigatrano em 66%, por aumento da sua excreção.13 Em função desta via metabólica, fármacos que sejam fortes indutores ou inibidores da gpP não devem ser prescritos devido à interação clinicamente significativa que apresentam com o Dabigatrano. (quadro 6) De forma a avaliar a eficácia e segurança do dabigatrano na fase aguda do tratamento da TVP, foi realizado um estudo aleatorizado, multicêntrico, duplamente cego, de não-inferioridade (RE-COVER), onde 2564 doentes com TVP e/ou EP foram randomizados, após administração de um anticoagulante parentérico, durante pelo menos 5 dias, para receber terapêutica com Varfarina (em dose ajustada para atingir INR entre 2.0–3.0) ou Dabigatrano (em dose de 150mg duas vezes ao dia) durante 6 meses de tratamento (Quadro 5).14, 15 A média de idades foi de 55 anos, 58% eram homens, 95% da população do estudo era caucasiana, 90% dos doentes tinham um ClCr superior a 50mL/min e em 68% o evento trombótico índice foi a TVP15
Este estudo demonstrou a não-inferioridade do dabigatrano, 150mg duas vezes ao dia em comparação com a varfarina. O resultado primário de eficácia (recorrência de TEV sintomático ou morte relacionada) ocorreu em 2.4% dos doentes a realizarem terapia com o DOAC e em 2.1% dos doentes tratados com Varfarina.15 O risco de hemorragia major foi semelhante em ambos os grupos (1.6% e 1.9%, respectivamente). No entanto, verificou-se um menor número de hemorragias intracranianas, em doentes tratados com Dabigatrano (0) em relação à Varfarina (3), menor número de hemorragias não-major clinicamente relevantes (5.6% e 8.8%, respectivamente) e menor número de eventos totais (16.1% e 21.9%, HR 0.71; IC 95% 0.59–0.85).13 Não obstante, o grupo tratado com Dabigatrano apresentou uma maior tendência para hemorragias gastrointestinais comparativamente ao grupo tratado com Varfarina.15 Neste estudo, não houve evidência de hepatotoxicidade associada ao Dabigatrano, ao contrário do Ximelagatrano (único IDT oral aprovado para o tratamento e prevenção do TEV e que foi retirado por hepatotoxicidade).17 A dispepsia, observada em 3% dos doentes tratados com Dabigatrano, foi o único efeito adverso atribuído, o que justificou a maior taxa de descontinuação do tratamento observada (9% Dabigatrano vs. 6.8% Varfarina).6 Em função do número reduzido de eventos TEV recorrentes no RE-COVER, foi efetuado um segundo estudo (RE-COVER II), com resultados de eficácia e segurança semelhantes nos dois grupos (Dabigatrano e Varfarina), reforçando os resultados do RE-COVER. 6 Posteriormente foram realizados dois estudos de extensão, randomizados, multicêntricos, duplamente cegos, de não-inferioridade, para avaliar a eficácia e segurança do Dabigatrano na prevenção secundária do TEV. O Dabigatrano, 150mg duas vezes ao dia, foi comparado com a Varfarina, no estudo RE-MEDY, e com o placebo, no estudo RE-SONATE (Quadro 5).6 O estudo RE-MEDY teve uma duração mediana de 15.6 meses e uma aderência global >98%.13 Neste estudo, o IDT foi considerado não inferior à Varfarina na prevenção de TEV recorrente ou morte relacionada (HR 1.44; IC 95% 0.78–2.64; p<0.01 para não-inferioridade)18 e mais seguro, verificando-se um menor número de eventos hemorrágicos major (0.9% e 1.8%, respectivamente) e não-major clinicamente relevantes (5.6% e 10.2%, respectivamente)18 No estudo RE-SONATE, com uma duração mediana de
5.4 meses e uma taxa de aderência global de 96.5%, foi demonstrada a não inferioridade do Dabigatrano comparativamente ao placebo, com um resultado primário de eficácia confirmado em 0.4% dos doentes tratados com o IDT e em 5.6% do grupo controlo (HR 0.08; IC95% 0.02–0.25; p<0.001).14 No entanto, o Dabigatrano demonstrou uma segurança inferior ao placebo, apresentando um maior número de eventos hemorrágicos major (0.3% Dabigatrano vs. 0% placebo) e não-major clinicamente relevantes (5.3% Dabigatrano vs. 1.8% placebo).14 O recto, foi o local predominante de hemorragia com o Dabigatrano (2.8% e 0.8%, respectivamente). Nos restantes locais o número de eventos hemorrágicos foi semelhante em ambos os grupos, assim como os eventos adversos.18
INIBIDORES DO FACTOR XA (FXA)
Os inibidores diretos do FXa (uma enzima essencial na conversão de protrombina em trombina) ligam-se de forma direta, seletiva e reversível à parte ativa do FXa, tanto na sua forma livre como na complexada com o fator Va ou na forma ligada às plaquetas, resultando numa diminuição da atividade do complexo protrombinase com consequente diminuição da geração de trombina e do desenvolvimento do coágulo de fibrina. 6 (Figura 1) Teoricamente, a supressão de uma molécula de FXa pode resultar numa redução da atividade da trombina 100 vezes superior à conseguida pela inibição de uma molécula de FIIa3 Os inibidores diretos do FXa apresentam uma resposta anticoagulante previsível, não necessitam de monitorização laboratorial de rotina e apresentam uma alta ligação às proteínas plasmáticas, sendo por isso não dializáveis.6
Rivaroxabano (Xarelto®)
O Rivaroxabano é um inibidor direto e reversível do FXa administrado por via oral e em doses fixas.19 Em 2011, foi aprovado pela EMA no tratamento da TVP e na prevenção secundária do TEV, sem necessidade de HBPM, na dose escalonada de 15mg duas vezes ao dia durante três semanas (21 dias), seguida de 20mg uma vez ao dia na continuação do tratamento e prevenção de TVP recorrente e EP, tendo por base a informação dos estudos EINSTEIN DVT, EINSTEIN PE e EINSTEIN EXT.20 (Quadro 5) O Rivaroxabano é um anticoagulante bem tolerado e sem efeito sobre as plaquetas.17 Tal como a HBPM, tem um rápido início de ação, com uma pico de concentração plasmática máxima entre as 2–4 horas após a ingestão. Apresenta uma elevada biodisponibilidade (80%–100%), se administrado aquando da ingestão de alimentos em doses superiores a 15mg, uma elevada ligação às proteínas plasmáticas (92%) e um tempo de semi-vida entre 5–9 horas, em indivíduos jovens saudáveis e entre 11–13 horas, em indivíduos idosos saudáveis (> 60 anos).21 Após a ingestão, 2/3 da dose administrada é degradada em metabolitos inativos pelo fígado, que são eliminados pela via renal e hepatobiliar, e o restante 1/3 é excretado de forma inalterada como substância ativa por via renal21 A sua administração está contraindicada em doentes com ClCr < 15 mL/min.20 (Quadro 4)
Apesar da ausência de interações alimentares, o Rivaroxabano, tal como os outros inibidores do FXa, é metabolizado pelo CYP450 (isoforma CYP3A4) e, tal como o IDT, é substrato da gpP. Estas diferenças são importantes em termos de interações medicamentosas, embora muitos dos fármacos que afetam a função do CYP3A4 afetam também a gp-P.16,21 Por este motivo, em doentes sob terapêutica com Rivaroxabano é contraindicada a administração concomitante de fármacos que sejam potentes inibidores ou indutores do CYP3A4 e/ou gpP. (quadro 6) Para testar a eficácia e segurança do Rivaroxabano (15mg duas vezes ao dia durante os primeiros 21 dias, seguida de 20mg uma vez ao dia) na fase aguda do tratamento da TVP e EP, este fármaco foi comparado com a terapêutica convencional, durante 3, 6 ou 12 meses, em dois estudos aleatorizados, abertos, de não-inferioridade (EISNTEIN DVT e EINSTEIN EP). Nos estudo EINSTEIN DVT e EINSTEIN PE os doentes foram considerados elegíveis se fosse confirmado o diagnóstico de TVP sintomática (sem EP sintomática) e EP sintomática (com ou sem TVP), respectivamente.6 Do ponto de vista do tratamento, no estudo EINSTEIN DVT foi confirmada a não inferioridade do Rivaroxabano em relação à terapêutica convencional no tratamento e prevenção do TEV recorrente ou morte relacionada (HR 0.68; IC95% 0.44–1.04; P<0.001) e na prevenção de eventos hemorrágicos major ou não-major clinicamente relevantes (HR 0.97; IC95% 0.76–1.22; p=0.77).22 Deste modo, concluiu-se que o Rivaroxabano apresenta uma eficácia e segurança semelhante ao tratamento convencional.22 Os resultados de eficácia do estudo EINSTEIN PE foram semelhantes (Quadro 7),no entanto, o Rivaroxabano foi associado a uma maior redução na incidência de hemorragias major (HR 0.49; IC 95% 0.31–0.79).23 Posteriormente, os resultados destes dois estudos foram reunidos numa análise pré-especificada (n= 8282 doentes), que permitiu a análise de subgrupos com elevado risco de TEV (doentes fragilizados, com cancro, com insuficiência renal moderada, eventos TEV recorrentes e maior carga de trombo)6, com o objetivo de obter resultados de eficácia e segurança mais precisos. Nesta análise conjunta, foi confirmada a não-inferioridade do Rivaroxabano, com a ocorrência de 2.1% de TEV recorrentes para o Rivaroxabano e 2.3% para a terapêutica convencional (HR 0.89; IC95% 0.66–1.19; p<0.001).24 Além disso, este DOAC foi associado a um menor número de eventos hemorrágicos major (hemorragias intracranianas e retroperitoneais) em relação à terapêutica convencional, nomeadamente, em doentes com idade ≥ 75 anos (1.2% e 4.5%, respectivamente; p<0.05) e em doentes com ClCr < 50mL/min (0.9% e 4.1%, respectivamente; p<0.05).6,24 O estudo EINSTEIN EXT é um estudo de superioridade, aleatorizado, de dupla-ocultação, que avaliou a eficácia e segurança do Rivaroxabano (20mg uma vez ao dia) contra placebo em doentes que completaram, pelo menos, 6–12 meses de anticoagulação e que tenham critérios para a sua continuação, durante mais 6–12meses.6 Neste estudo, o Rivaroxabano demonstrou uma maior eficácia na prevenção de eventos TEV recorrentes com uma diminuição do risco relativo e do risco absoluto de 82% e 5.8%, respectivamente.6,22 No entanto, registou-se um maior número de eventos hemorrágicos não major clinicamente relevantes com o Rivaroxabano (5.4% e 1.2%) e hemorragias major (0.7% e 0).22 Todavia, concluiu-se que o Rivaroxabano é um inibidor direto do FXa eficaz na prevenção secundária a longo prazo do TEV e que, embora evidencie uma maior taxa de eventos hemorrágicos comparativamente ao placebo, foi comprovada uma relação risco-benefício claramente favorável (4 eventos hemorrágicos major na prevenção de 34 eventos recorrentes de TEV).19
Apixabano (Eliquis®)
O Apixabano é um inibidor direto e reversível do FXa administrado por via oral, em dose fixa, sem necessidade de monitorização.25 Este fármaco apresenta uma biodisponibilidade oral de cerca de 50%, um rápido início de ação, com uma concentração plasmática máxima após 3–4 horas da sua administração, uma elevada ligação às proteínas plasmáticas (87%) e um tempo de semi-vida de, aproximadamente, 12 horas, em doentes saudáveis.26 Tal como todos os inibidores do FXa, é substrato da gp-P e metabolizado, principalmente, pelo CYP450 3A4. Por este motivo é contraindicada a administração concomitante de fármacos que sejam potentes indutores ou inibidores do CYP3A4 e/ ou gpP.16 (quadro 6) É eliminado por várias vias (apenas 27% por via renal). 25 (Quadro 4) Em 2014, foi aprovado pela EMA, para o tratamento e prevenção do TEV recorrente, em adultos, sem necessidade de HBPM na dose escalonada de 10mg duas vezes ao dias, durante os primeiros 7 dias, seguida de 5mg, duas vezes ao dia na continuação do tratamento e prevenção secundária da TVP e EP, tendo por base os estudos AMPLIFY e AMPLIFY-EXT.4 Ambos os estudos foram aleatorizados, de dupla-ocultação, de não-inferioridade e multicêntricos. (Quadro 5) No estudo AMPLIFY, o Apixabano, na dose recomendada, foi comparado com a terapêutica convencional, por um período de 6 meses, de forma a testar a sua eficácia e segurança em doentes com TVP e/ou EP sintomática (Quadro 7).27 A média de idades foi de 57 anos e o grupo da Varfarina alcançou um tempo médio de INR terapêutico de 61%.27 Neste estudo o Apixabano foi demonstrada a não-inferioridade e a similar eficácia do Apixabano comparativamente à terapêutica convencional (HR 0.84; IC95% O.60–1.18; p<0.001). Não obstante, este DOAC apresentou uma maior segurança com uma redução do risco relativo em 69% de hemorragias major comparativamente à terapêutica convencional (HR 0.31 IC95%0.17–0.55).28 Da mesma forma, o combinado hemorragias major e não-major clinicamente relevantes foi menos frequente no grupo tratado com Apixabano em relação à terapêutica convencional (4.3% e 9.7%, respectivamente). A taxa de outros eventos adversos foi semelhante nos dois grupos. 28 No estudo AMPLIFY-EXT foi avaliada a eficácia e segurança do Apixabano, contra placebo, nas doses de 2.5mg e 5mg, duas vezes ao dia, durante 12 meses, em doentes que completaram 6–12 meses de terapia anticoagulante inicial e que tenham indicação para a sua continuação.29 No final de um ano de tratamento, as duas doses testadas (2.5mg e 5mg) mostraram, de igual forma, uma eficácia superior ao placebo (Apixabano 2.5mg: HR 0.33; IC95% 0.11–0.33 e Apixabano 5mg: HR 0.36; IC95% 0.11–0.34), sendo necessário tratar 14 doentes para prevenir 1 episódio de TEV recorrente (NNT=14).29 Neste estudo, o número de eventos hemorrágicos major no grupo tratado com Apixabano (2.5mg e 5mg) foi semelhante ao placebo (Apixabano 2.5mg e 5mg: 0.2% e 0.1%, respectivamente; Placebo: 0.5%), no entanto, verificou-se um risco superior de hemorragia não-major clinicamente relevante no grupo tratado com Apixabano 5mg comparativamente à dose de 2.5mg e ao placebo (4.2% vs. 3.0% e 2.3%, respectivamente) 29. Desta forma, o estudo AMPLIFY-EXT concluiu que ambas as doses testadas de Apixabano são eficazes na prevenção secundária a longo prazo do TEV, no entanto, a dose 2.5mg, duas vezes ao dia, revelou ser mais segura.
Edoxabano (Lixiana®)
O Edoxabano é um inibidor direto e reversível do FXa, administrado por via oral, sem necessidade de monitorização.30 Tal como os outros inibidores diretos do FXa, apresenta um rápido início de ação (com um pico de concentração plasmática máxima após 1–2horas da sua administração), uma biodisponibilidade oral de aproximadamente 62% e um tempo de semi-vida de 8–10 horas, em doentes saudáveis. É eliminado de várias formas (35%-50% por via renal) e apresenta algumas interações medicamentosas, por ser substrato da gp-P e parcialmente (menos de 10%) metabolizado pelo CYP450 3A4 (Quadro 4 e quadro 6).16 A sua administração está contraindicada em doentes com ClCr <15 mL/min e é recomendado um ajuste da dose (para 30mg, uma vez ao dia) em doentes com ClCr <50mL/min ou peso corporal ≤ 60Kg.30 Comparativamente aos outros fármacos da mesma classe, o Edoxabano tem uma menor ligação às proteínas plasmáticas (55%), uma propriedade clinicamente importante em doentes a realizar hemodiálise.31
Em 2015, o Edoxabano foi aprovado pela FDA, com base no estudo HOKUSAI-VTE, na dose de 60mg uma vez ao dia após, pelo menos, 5 dias de terapêutica anticoagulante parentérica (HBPM ou HNF), para o tratamento e prevenção de episódios recorrentes de TVP e EP, em adultos.
O HOKUSAI-VTE é um estudo aleatorizado, em dupla-ocultação, de não inferioridade, onde foi comparada a eficácia e segurança do Edoxabano, na dose recomendada, com a Varfarina para o tratamento do TEV, em doentes com TVP e/ou EP, por um período de 3 a 12 meses.32 A duração do tratamento é determinada com base no risco de TEV recorrente, hemorragia e na preferência do doente.33 (Quadro 5)
Neste estudo, foi demonstrada a não inferioridade do Edoxabano, 60mg uma vez ao dia, em relação à Varfarina no tratamento e prevenção do TEV recorrente (HR 0.89; IC95% 0.70–1.13; p<0.001) e na prevenção de eventos hemorrágicos major (HR 0.84; IC95% 0.59–1.21).34 No entanto, o resultado primário de segurança (hemorragia major e não major clinicamente relevantes) foi menor no grupo tratado com Edoxabano (8.5%) em relação à terapêutica convencional (10.3%) (HR 0.81; IC95% 0.71– 0.94).27 Os eventos adversos não diferiram entre os dois grupos e nos doentes com critérios para receber Edoxabano na dose de 30mg, uma vez ao dia, foram obtidos resultados semelhantes em relação à dose de 60mg, uma vez ao dia.31 (Quadro 7) Num subgrupo pré-especificado de doentes com EP e disfunção ventricular direita, documentada por tomografia computorizada (TC) e/ou NT-pro-BNT≥500pg/ml, e nos doentes com disfunção ventricular direita, documentada por TC, o Edoxabano apresentou uma eficácia superior à Varfarina (HR 0.52; IC95% 0.28–0.98 e HR 0.42; IC95%0.15–1.20, respectivamente).34
Em virtude dos factos mencionados pelo estudo HOKUSAI-VTE, concluiu-se que o Edoxabano, 60mg ou 30mg uma vez ao dia, apesar de uma semelhante eficácia em relação à terapêutica convencional, apresenta uma segurança superior para o tratamento e prevenção do TEV.
MONITORIZAÇÃO DO TRATAMENTO
Os DOAC, ao contrário dos AVK, apresentam uma resposta anticoagulante previsível sem necessidade de monitorização de rotina.35 Contudo, em determinadas situações é vantajoso proceder à avaliação da sua atividade anticoagulante e, eventualmente à quantificação do fármaco, nomeadamente em caso de: eventos hemorrágicos, eventos trombóticos, necessidade de cirurgia urgente e em situações clínicas especiais como doentes com agravamento agudo da insuficiência renal ou hepática, potenciais interações medicamentosas ou suspeita de “overdose”.36
No entanto, os testes de coagulação utilizados por rotina não refletem com precisão o efeito anticoagulante dos DOAC, sendo o resultado influenciado pelos reagentes utilizados, que é variável entre os diferentes laboratórios, e pelo período decorrido entre a toma do fármaco e a colheita da amostra.16 Os testes realizados diferem consoante o fármaco (quadro 8). No caso do IDT, a avaliação qualitativa da atividade anticoagulante é determinada pelo aPTT (tempo de tromboplastina parcial ativado) ou pelo TT (tempo de trombina).35 O aPTT é o método qualitativo mais utilizado e apresenta uma relação curvilínea com o Dabigatrano.35 A mediana no aPTT 12 horas após a última dose é 1.5 vezes superior ao controlo (2 vezes superior ao controlo em 10% dos doentes), no entanto se o aPTT exceder duas vezes o limite superior do normal após 12–24horas de ingestão da última dose do fármaco, está associada a um elevado risco de hemorragia.37 O aPTT normal significa que a atividade anticoagulante não é relevante. O TT é um teste com elevada sensibilidade ao IDT, sendo útil na confirmação da não existência de atividade anticoagulante do fármaco, quando apresenta resultados dentro de valores normais. Pode ser utilizado para diferenciar o DOAC que está a ser utilizado pelo doente numa situação de emergência, pois na presença de um inibidor direto do FXa estará dentro dos valores normais. 35 O ECT (tempo de coagulação de Ecarina) e o dTT (tempo de trombina diluído), embora não sejam facilmente disponíveis, permitem uma avaliação quantitativa do Dabigatrano. O ECT é um teste utilizado em investigação que proporciona uma medida direta da atividade do IDT. Se o ECT exceder três vezes o limite superior do normal, após 12–24horas da ingestão da última dose de Dabigatrano, sugere um elevado risco de hemorragia. No entanto, como o ECT não se encontra disponível, foi desenvolvido o ensaio cromogénico da Ecarina (ECA), comercialmente disponível em laboratórios de coagulação de apoio ao doente.37 O dTT apresenta uma relação linear com o IDT e se for superior a 65 segundos, indicando uma concentração plasmática de Dabigatrano superior a 200ng/mL, após 12–24horas da ingestão da última dose, está associada a um elevado risco hemorrágico.37
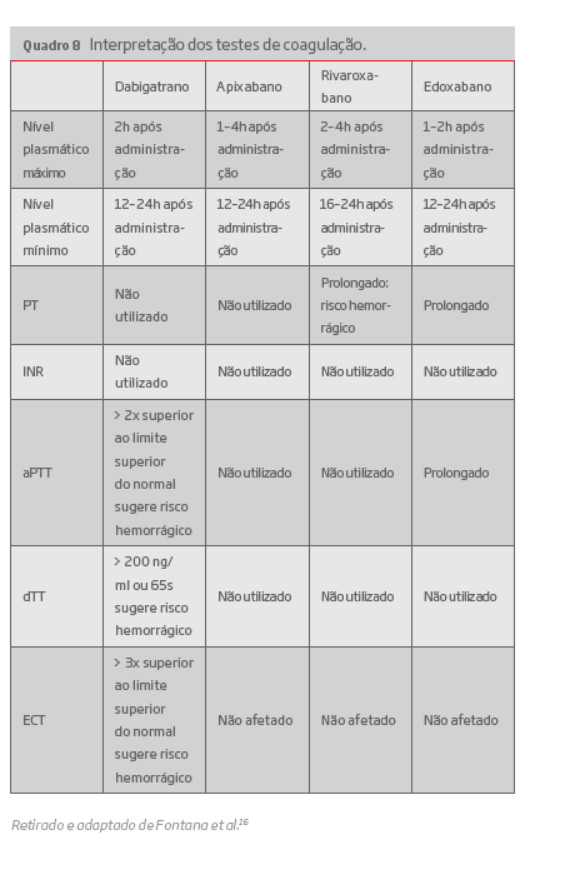
De forma a monitorizar os inibidores do FXa, o TP (tempo de protrombina) é o método qualitativo mais sensível para avaliação do efeito anticoagulante do Rivaroxabano com um prolongamento dependente da dose. No entanto é influenciado por vários fatores como, por exemplo, insuficiência hepática, sépsis, vários tipos de cancros e outras doenças sistémicas.35,37 Em contrapartida, para avaliação do efeito anticoagulante do Apixabano e do Edoxabano o PT não pode ser utilizado 32,37 A concentração destes fármacos também pode ser obtida com bastante precisão por métodos diretos (quantitativos), o ensaio cromogénico anti-Xa, usando calibradores validados e controlos específicos para cada inibidor do FXa.35
REVERSÃO DO EFEITO ANTICOAGULANTE
O risco hemorrágico é transversal a todos os DOAC. No entanto, esse risco pode estar aumentado em situações de insuficiência renal aguda, interações medicamentosas ou toma de dose excessiva intencionalmente, ou não, pelo doente.16 No caso de suspeita de ingestão de um DOAC em dose excessiva, os testes de coagulação podem ajudar a determinar o grau do risco hemorrágico. Devido à curta semi-vida destes fármacos (aproximadamente 12h), na maioria dos casos não acompanhados de hemorragia ativa uma atitude expectante é ideal.37 No entanto, numa situação particular de overdose em que a ingestação do DOAC ocorreu há ≤2 horas, pode-se ponderar o uso de carvão ativado com o objetivo de reduzir a absorção do fármaco pelo trato gastrointestinal.37 A abordagem inicial de uma complicação hemorrágica deve ter em conta a gravidade do evento hemorrágico, a situação clínica do doente, a necessidade de um procedimento invasivo para controlo da hemorragia e o tipo, a dose e o momento da última toma do DOAC administrado.38 Na ocorrência de uma hemorragia ligeira o tempo é o melhor
“antídoto”, pelo que a hemóstase local é muitas vezes suficiente.37 Nestes casos, 12–24h após a última dose administrada, espera-se que a hemóstase seja restaurada. No entanto, o tempo de eliminação do efeito anticoagulante está relacionado com a função renal, particularmente nos doentes a realizar terapia com Dabigatrano.35 Perante uma hemorragia moderada/grave, para além das medidas de suporte gerais (compressão mecânica, hemóstase cirúrgica, reposição de fluídos e outras medidas de suporte hemodinâmica) é necessário avaliar a necessidade de transfusão de componentes e/ou derivados do sangue e a realização de manobras invasivas.39 Em doentes com insuficiência renal e em terapia com Dabigatrano a diurese deve ser promovida e pode-se ponderar a realização de hemodiálise (os inibidores diretos do FXa não são dialisáveis).16 Na presença de uma hemorragia grave com risco de vida ou na necessidade de uma cirurgia emergente que não pode ser atrasada pelo menos 8h, além das medidas de suporte, deve-se ponderar a utilização de agentes de reversão da atividade anticoagulante dos DOAC.16 O Dabigatrano é o único DOAC com um agente de reversão específico — antídoto -, o Idarucizumab, que recebeu aprovação na Europa em Novembro de 2015.40 Este antídoto é um fragmento de anticorpo monoclonal humanizado com alta afinidade para o Dabigatrano livre e ligado à trombina, neutralizando a sua atividade anticoagulante em poucos minutos, normalizando os tempos de coagulação (dTT e/ ou ECT). É administrado por via intravenosa (infusão de 2 bólus de 50 ml de 2.5g correspondendo a um total de 5g).40 A segurança e eficácia do Idarucizumab em doentes com hemorragia grave ou com necessidade de uma cirurgia urgente foi demonstrada no estudo RE-VERSE AD (n=90) visto ter sido observada uma rápida e completa reversão do efeito anticoagulante em 88 a 98% dos doentes, sem efeitos adversos significativos.41 Neste estudo, imediatamente após a administração de Idarucizumab, a concentração do IDT livre reduziu para um valor igual ou próximo do limite inferior de quantificação, não se obtendo normalização do dTT e do ECT apenas num doente.41 No entanto, devido ao fenómeno de redistribuição do Dabigatrano do compartimento extravascular para o espaço intravascular, um aumento da concentração do Dabigatrano, evidente por um aumento dos tempos de coagulação, foi verificado em 7% e 18% doentes 12 e 24horas após a administração do antídoto, respectivamente. Todavia, é incerto se estes doentes beneficiariam de uma dose adicional de Idarucizumab.41 De forma a reverter o efeito dos inibidores diretos do FXa, encontra-se em desenvolvimento, o Andexanet alpha, um análogo recombinante do FXa, cataliticamente inativo, com capacidade de se ligar e sequestrar os inibidores do FXa no espaço intravascular, restabelecendo a atividade do FXa e reduzindo a atividade anticoagulante. Este fármaco demonstrou ter um rápido e eficaz efeito na reversão desses fármacos assim como naqueles com atividade anti-Xa, como a HBPM (enoxaparina).16,40 Este agente de reversão específico apresenta um curto tempo de semi-vida (1hora) e um efeito de reversão não sustentado, sendo administrado em bólus por via intravenosa durante 30 minutos seguido de infusão contínua por 2 horas.42 A sua eficácia e segurança foi avaliada nos estudos ANNEXA-A e ANNEXA-R que envolveram voluntários saudáveis tratados com Apixabano ou Rivaroxabano, respectivamente. Nestes estudos o Andexanet alpha reverteu de uma forma rápida e eficaz o efeito anticoagulante induzido pelo Apixabano e Rivaroxabano, com efeito máximo 2 a 5 minutos após a administração do bólus intravenoso e sustentada durante a infusão, sem eventos adversos significativos. A duração da reversão foi consistente com a semi-vida do agente de reversão.42 Como estes estudos não incluíram doentes com necessidade de reversão urgente do efeito anticoagulante (por hemorragia e/ou cirurgia emergente) foi desenvolvido o estudo ANNEXA-4 para avaliar a eficácia e segurança do Andexanet em doentes com uma hemorragia grave (nomeadamente gastrointestinal ou intracraniana) tratados com um inibidor do fator Xa.43
Este estudo demonstrou a eficácia do Andexanet alpha na reversão da atividade anticoagulante dos inibidores do FXa, a hemóstase foi obtida em 79% dos doentes após 12horas da infusão de Andexanet e em 18% dos doentes ocorreram eventos trombóticos.43 Por este motivo, será necessário um estudo controlado para avaliar se a frequência desses eventos foi superior ao esperado em doentes com risco aumentado de eventos trombóticos, para avaliar a segurança deste agente de reversão.43
Até à aprovação de um antídoto para os inibidores do FXa, numa hemorragia grave/risco de vida, como primeira linha devem-se considerar agentes não-específicos como o complexo concentrado protrombínico (CCP), numadose inicial de 50 U/Kg com uma dose adicional de 25 U/ Kg se clinicamente indicado, ou o complexo concentrado protrombínico ativado (aCCP) numa dose de 50 U/Kg até um máximo de 200 U/Kg/dia.40 Estes agentes também devem ser considerados em doentes em terapia com Dabigatrano se o Idarucizumab não estiver disponível.35 Testes in vitro, usando amostras de voluntários a tomar Rivaroxabano,
Apixabano e Dabigatrano mostraram que aCCP (semelhante ao CCP, mas com Fator VIIa (FVIIa) — Feiba®) corrigiu mais parâmetros de coagulação do que o CCP. 35 No entanto, é importante lembrar que a eficácia do CCP ou do aCCP não foi estabelecida em doentes sob DOAC sendo fundamental equilibrar os potenciais efeitos pro-trombóticos contra os potenciais benefícios anticoagulantes.37
Como segunda linha, deve-se considerar o FVIIa recombinante (rFVIIa)6, embora a sua utilização “off-label” não esteja recomendada por ter sido demonstrado um aumento do risco de trombose arterial em comparação com o placebo numa meta-análise de ensaios clínicos randomizados. 40 O plasma fresco, embora não seja utilizado para a reversão do efeito anticoagulante, é recomendado em doentes com outra coagulopatia associada ou que necessitam de uma transfusão massiva para expansão do volume plasmático.37
A Aripazina (PER977), uma pequena molécula sintética, é um antídoto em desenvolvimento que apresenta uma ligação direta a vários anticoagulantes (HNF, HBPM, DOAC) impedindo a ligação aos seus respetivos alvos, apresentando um efeito antagonista mais generalizado. No entanto, o seu mecanismo de ação permanece desconhecido.16,44
A figura 2 representa as medidas de atuação numa situação de hemorragia por um DOAC.
PROCEDIMENTOS INVASIVOS
Uma intervenção cirúrgica, associada a um risco hemorrágico, pode exigir a suspensão temporária do DOAC de acordo com uma análise balanceada entre os fatores relacionados com o procedimento (facilidade de hemóstase e risco hemorrágico) e as características particulares do doente (risco hemorrágico — antecedentes, interações medicamentosas e comorbilidades — e risco tromboembólico).16
A utilização de bridging com HBPM não está indicada nos doentes em tratamento com um DOAC, devido às suas propriedades farmacocinéticas e farmadinâmicas previsíveis. 16
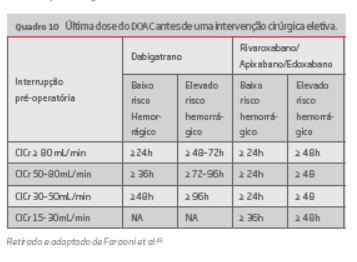
Os doentes em terapia com um inibidor do FXa e com função renal normal, o DOAC deve ser suspenso, pelo menos, 24h ou 48h antes de um procedimento com baixo ou elevado risco hemorrágico, respectivamente. Se o ClCr < 30mL/
min, recomenda-se a toma da última dose do fármaco pelo menos 36h ou 48h antes de uma intervenção com baixo ou elevado risco hemorrágico, respectivamente. Estes fármacos não devem ser utilizados quando o ClCr<15mL/min.45
Os doentes em tratamento com o IDT (Dabigatrano), o tempo de interrupção deste fármaco varia entre 24 a 48 horas para procedimentos com risco hemorrágico baixo, consoante o ClCr. Intervenções com risco hemorrágico elevado devem ser realizadas após 48–72 horas da última dose do fármaco em doentes com ClCr>50mL/min ou após 96 horas em doentes com ClCr<50mL/min. O Dabigatrano está contraindicado em doentes com ClCr<30mL/min.45
Quando uma intervenção está associada a um risco hemorrágico clinicamente não importante e sendo possível uma hemóstase local adequada, o procedimento cirúrgico pode ser realizado só suspendendo a toma prévia à manobra.
O DOAC pode ser retomado 6–8horas após a intervenção em situações de risco hemorrágico baixo, se hemóstase estiver assegurada.37
No entanto, para muitas intervenções, retomar os DOAC nas primeiras 48–72horas após o procedimento pode representar um risco hemorrágico superior ao risco tromboembólico.
Para intervenções associadas a um elevado risco tromboembólico, deve ser considerado o recurso a um anticoagulante parentérico (HBPM ou HNF), para tromboprofilaxia, 6–8h após a intervenção e a retoma do DOAC 48–72h após o procedimento invasivo.45
No quadro 9 é apresentada a classificação das intervenções de acordo com o risco hemorrágico e a quadro 10 apresenta o tempo recomendado entre a ingestão da última dose e a intervenção cirúrgica eletiva.

DISCUSSÃO
Até há 9ª edição da CHEST para o tratamento e prevenção do TEV apenas dois ensaios clínicos randomizados tinham comparado os DOAC (Dabigatrano e Rivaroxabano) com a terapêutica convencional. No entanto, a pouca experiência e a escassez de dados não permitiam apoiar a eficácia e segurança destes fármacos.5 Por este motivo, a terapêutica convencional era a recomendada para o tratamento e prevenção da TVP. Desde então, grandes ensaios randomizados compararam os DOAC (com ou sem terapêutica parentérica inicial) com a terapêutica convencional para o tratamento e prevenção a longo-prazo do TEV. Estes estudos demonstraram a não-inferioridade dos DOAC e concluíram que estes são tão ou mais eficazes do que a terapêutica convencional no tratamento e prevenção secundaria do TEV recorrente com a vantagem de apresentarem uma maior segurança associada a um menor número de eventos hemorrágicos major, nomeadamente hemorragias intracranianas.5 Apesar do custo direto dos DOAC ser superior aos AVK, a relação custo-eficácia é comparável ou superior dada a maior segurança e ausência de necessidade de monitorização por rotina.46 Perante a evidência das grandes vantagens desta nova classe de fármacos, a 10ª edição da CHEST para o tratamento e prevenção do TEV recomenda o uso dos DOAC em lugar da terapêutica convencional para o tratamento e prevenção secundária do TEV, em doentes sem cancro (Grau de evidência 2B).5
Note-se que a escolha do fármaco deve ser individualizada equacionando sempre o risco/benefício de acordo com os fatores de risco e preferência de cada doente (adesão ao tratamento, idade, comorbilidades, peso corporal, história de eventos hemorrágicos e interações medicamentosas) e que, embora o anticoagulante utilizado no tratamento inicial seja normalmente o mesmo na prevenção a longo-prazo, se houver razões para alterar o anticoagulante, esta mudança deve ser realizada.5 Além disso, a utilização dos DOAC poderá não ser possível em todos os doentes visto que a sua segurança não foi suficientemente estudada em doentes idosos, com doença hepática ou doença renal grave e doentes com determinadas trombofilias, nomeadamente a Síndrome do Anticorpo Antifosfolipídeo (SAF).46 A mudança da terapêutica (AVK para um DOAC) não é aconselhável em doentes com fraca adesão terapêutica ou que se sintam confortáveis com a monitorização e que apresentam INR terapêutico estável.46 Por outro lado, um doente que tenha dificuldade em manter a dose terapêutica do AVK, pode beneficiar se mudar para um DOAC.46 O DOAC deve ser iniciado imediatamente se o INR for inferior a 2.0 ou no dia seguinte se o valor de INR estiver entre 2.0–2.5.37 Se o valor de INR for superior a 2.5 é recomendado uma nova monitorização deste valor tendo em conta o tempo de semi-vida do AVK, de forma a estimar o tempo necessário para que o INR seja inferior ao valor de referência.37 Nos estudos RE-COVER e RE-SONATE, o Dabigatrano foi associado a um maior número de eventos adversos comparativamente à Varfarina e placebo, nomeadamente dispepsia e hemorragias gastrointestinais, respectivamente. Por este motivo, o IDT deve ser evitado em doentes com dispepsia.47 A adesão à terapêutica é crucial nos doentes em tratamento com um DOAC visto que o seu efeito anticoagulante desaparece rapidamente 12–24horas após a última dose e os testes de coagulação existentes, cuja interpretação dos resultados está dependente do intervalo de tempo decorrido entre a administração da última dose e a colheita da amostra, não devem ser utilizados para monitorizar a adesão, salientando a importância da educação do doente.37 Deste modo, embora os DOAC não necessitem de monitorização de rotina, são necessárias consultas de acompanhamento para reforçar a importância da adesão ao tratamento, registo de potenciais efeitos adversos e avaliação da função renal.46 Em determinadas ocasiões é vantajoso proceder à quantificação do fármaco. No entanto, a sensibilidade dos testes globalmente disponíveis, como o aPTT e o PT que permitem determinar o efeito anticoagulante do Dabigatrano e dos inibidores do FXa respectivamente35, é dependente do reagente utlizado o que dificulta a interpretação dos resultados, destacando a necessidade de testes padronizados.36 Infelizmente, os testes específicos que permitem quantificar o fármaco administrado (ECT, ECA, dTT, ensaio cromogénico anti-FXa) não estão amplamente disponíveis e, muitas vezes, não permitem obter um resultado em tempo útil.36 A aprovação do antídoto Idarucizumab possibilitou a reversão, de forma mais eficaz e segura, do efeito anticoagulante do Dabigatrano em doentes com hemorragia grave/risco de vida ou com necessidade de uma cirurgia emergente que não pode ser adiada pelo menos 8 horas. Atualmente, na ausência de antídotos aprovados para os inibidores diretos do FXa, a reversão destes fármacos é realizada com agentes não específicos como o CCP, aCCP ou rFVIIa.46
CONCLUSÃO
Durante décadas, o tratamento padrão da TVP envolveu uma terapêutica anticoagulante parentérica inicial, durante pelo menos 5 dias, seguida da utilização de AVK, durante pelo menos 3 meses. No entanto, as diversas limitações associadas à terapêutica convencional, nomeadamente a estreita janela terapêutica, a necessidade de monitorização laboratorial frequente, as diversas interações alimentares e medicamentosas e os polimorfismos genéticos promoveram o desenvolvimento de anticoagulantes orais alternativos. Os DOAC representam um passo muito importante no tratamento e prevenção secundária da TVP, ultrapassando muitas das limitações da terapêutica convencional. Além das características próximas de um anticoagulante ideal, vários ensaios clínicos randomizados demonstraram a não-inferioridade e o similar perfil de eficácia destes fármacos comparativamente à terapêutica convencional com a vantagem de apresentarem um melhor perfil de segurança associado a uma redução da incidência de hemorragias major. Apesar de serem necessários mais estudos para uma melhor quantificação dos DOAC e determinação da sua segurança em determinados subgrupos, muitos doentes poderão beneficiar desta nova abordagem. Assim, após décadas de uso dos dicumarínicos, a aprovação e recomendação dos DOAC pelas mais recentes orientações proporcionou uma mudança de paradigma no tratamento e prevenção secundária da TVP associado a uma redução da morbilidade, maior autonomia, relação risco-benefício e satisfação, o que sugere um aumento da adesão comparativamente à terapêutica convencional
CONFLITO DE INTERESSES
Os autores declaram não haver conflito de interesses.
BIBLIOGRAFIA
Cushman, M. Treating Acute Venous Thromboembolism: Shift with Care. N. Engl. J. Med. 8–10 (2013). doi:10.1056/NEJMe1307413 [ Links ]
M., B. et al. Deep vein thrombosis and novel oral anticoagulants: A clinical review. Eur. Rev. Med. Pharmacol. Sci. 17, 3123–3131 (2013). [ Links ]
Pascarella, L., Cox, M. W. & O'Brien, P. J. Venous thromboembolism: diagnosis and current anticoagulation strategies for deep vein thrombosis and pulmonary embolism. Pract. (1995) 40, 58–70 (2012). [ Links ]
Correio eletrónico: brunasofiaguimaraes@hotmail.com (B. Guimarães).














