Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Angiologia e Cirurgia Vascular
versão impressa ISSN 1646-706X
Angiol Cir Vasc vol.8 no.3 Lisboa set. 2012
Estratégia terapêuticana doença venosa crónica
Therapeutic strategy in the chronic venous disease
Júlia Medeiros*, Armando Mansilha **
*Aluna do 6º Ano de Mestrado Integrado em Medicina, Faculdade de Medicina da Universidade do Porto
** MD, PhD, FEBVS, Assistente Hospitalar de Angiologia e Cirurgia Vascular, Professor Convidado da Faculdade de Medicina da Universidade do Porto, Orientador do Projeto de Opção de Mestrado Integrado em Medicina, Coordenador da Unidade de Angiologia e Cirurgia Vascular do Hospital CUF Porto, Secretário-Geral da Sociedade Portuguesa de Angiologia e Cirurgia Vascular,
Secretário-Geral da Secção de Cirurgia Vascular da UEMS (União Europeia de Médicos Especialistas)
Faculdade de Medicina da Universidade do Porto
|RESUMO|
A doença venosa crónica é uma patologia bastante prevalente capaz de alterar a qualidade de vida do doente, e com um importante impacto socioeconómico. O seu tratamento passa pela adoção de medidas higieno-dietéticas, pela farmacoterapia, compressão elástica, incluindo ainda formas de tratamento que permitem a ablação do refluxo e hipertensão venosa como a ablação mecânica, térmica e química.
Face à multiplicidade de abordagens terapêuticas atualmente disponíveis torna-se importante averiguar aquelas mais eficazes.
O objetivo do presente trabalho é sistematizar a orientação clínica de doentes com doença venosa crónica, tendo em conta a classificação CEAP, os resultados de estudos publicados assim como as recomendações atualmente disponíveis, de forma a promover tanto a melhoria clínica como a satisfazer as expectativas do doente.
Pesquisaram-se na Medline artigos em língua inglesa no âmbito do tratamento da doença venosa crónica. Foram ainda consultados estudos, não incluídos na pesquisa inicial, mas citados nos artigos da mesma.
Foi possível aferir que o tratamento da doença venosa crónica deve ser individualizado e estabelecido de acordo com estádio clínico. As medidas higieno-dietéticas devem ser adotadas por todos os doentes e os diferentes graus de compressão aplicados de acordo com a classificação CEAP. A farmacoterapia promove alívio sintomático e melhoria das complicações decorrentes da doença. Todas as técnicas podem ser realizadas em ambulatório. A ablação térmica é prometedora; contudo, desconhecem-se resultados da recorrência a longo prazo, a química apesar de ser a mais barata está associada a maior incidência de pigmentação e recanalização. A ablação mecânica pode ser realizada sem anestesia geral e permite regressar às atividades profissionais no dia seguinte.
Palavras-chave: Doença venosa crónica, Varizes, Farmacoterapia, Compressão elástica, Ablação venosa
|ABSTRACT|
Chronic venous disease (CVD) is a highly prevalent pathology that compromises patient’s quality of life, and has an important impact socioeconomically. Its treatment passes through the adoption of hygiene-dietetic measures, pharmacological therapy and elastic compression, as well as approaches that are able to ablate venous reflux and hypertension such as mechanical, thermic or chemical ablations.
Due to the multiplicity of therapeutic approaches available nowadays, it is important to search for the more effective ones.
The objective of this work is to establish a systematic clinical orientation for patients with chronic venous disease, taking into account the CEAP classification, the published results and the recommendations available, in a way to achieve clinical improvement and to answer patient’s expectations.
English articles were searched in Medline in concern to the treatment of chronic venous disease. Articles cited by others contained in the initial research were also included.
It was possible to understand that chronic venous disease treatment must be individualized and established according to the clinical state. Hygiene-dietetic measures must be adopted by all patients and the different compressions degrees adjusted to the CEAP classification. Pharmacological therapy induces symptomatic relieve and improves complications. All ablation techniques can be performed in an ambulatory setting. Thermal ablation is a promising treatment although there is lack of long term results for recurrence, whereas the chemical ablation, despite being the cheapest, is the mayor cause of pigmentation and recanalization. Mechanical approaches can be performed without general anesthesia and patients are able to return to work the day after the procedure.
Key words: Chronic venous disease, Varicose veins, Pharmacological therapy, Compression, Venous ablation
LISTA DE ABREVIATURAS E SIGLAS
DVC Doença venosa crónica
AVF American Venous Forum
VCSS Venous Clinical Severity Score
SF-36 Short Form Health Survey
CIVIQ Chronic Venous Insufficiency Questionnaire
VEINES-QOL/Sym Venous Insufficiency Epidemiologic and Economic Study of Quality of Life
AVVQ Aberdeen Varicose Vein Questionnaire
CXVUQ Charing Cross Venous Ulceration Questionnaire
FFPM Fração flavonóica purificada micronizada
CHIVA Cure Conservatrice et Hemodynamique de L’insiffisance Veineuse en Ambulatiore)
ASVAL Ablation Sélective des Varices sous Anesthesié Locale
SVS/AVF Society of Vascular Surgery/American Venous Forum
INTRODUÇÃO
A doença venosa crónica (DVC) é uma patologia bastante prevalente, que atinge entre 5 a 30% da população adulta[1], capaz de reduzir a qualidade de vida e com repercussões importantes a nível socioeconómico, tendo em conta que a doença e as suas complicações podem ser responsáveis por dor crónica e incapacitante e, consequentemente, pela perda de dias de trabalho e antecipação da reforma. Os custos diretos são capazes de exceder os 10 milhões de euros por cada milhão de habitantes na Bélgica, França, Itália e Reino Unido[2].
O sistema venoso encontra-se dividido em superficial, perfurante e profundo, podendo a DVC estar relacionada com qualquer um desses compartimentos. O funcionamento venoso está dependente da plenitude das válvulas e de músculos propulsores, que garantem o fluxo venoso no sentido contrário à gravidade [1]. A incompetência valvular de veias superficiais pode resultar do enfraquecimento das paredes vasculares ou ser secundária a tromboflebites, enquanto a incompetência venosa profunda surge, frequentemente, na sequência de um evento obstrutivo[1].
A doença venosa crónica engloba qualquer alteração morfológica ou funcional do sistema venoso e cursa com uma série de apresentações clínicas que podem variar de telangiectasias a úlceras venosas[3]. Neste contexto surgiu a necessidade de criar um sistema capaz de conduzir a um diagnóstico e classificação precisos e adequados, que constitua a base para a escolha da estratégia terapêutica mais apropriada. Assim, em 1994, no âmbito do congresso anual do American Venous Forum (AVF), foi apresentada a classificação CEAP, a qual tem em conta a avaliação clínica do doente (C), a etiologia da doença (E), região anatómica envolvida (A) e o processo fisiológico subjacente (P)[4] |QUADRO 1|.
| QUADRO 1 | Classificação CEAP
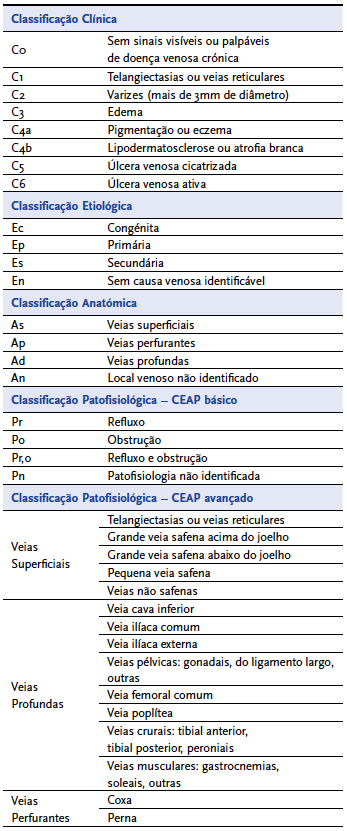
Todas as formas de apresentação clínica da DVC estão compartimentadas em sete categorias que variam de acordo com a gravidade, sendo C0 a ausência de sinais, C1 telangiectasias e/ou varizes reticulares, C2 varizes tronculares, C3 edema, C4a pigmentação e/ou eczema dos membros, C4b lipodermatosclerose e/ou atrofia branca, C5 úlcera venosa cicatrizada e C6 úlcera venosa ativa. A presença (S) ou ausência (A) de sintomatologia é igualmente registada[4]. As queixas mais frequentemente apresentadas pelos doentes são dor, prurido, calor, edema, sensação de "pernas pesadas", fadiga e/ou pernas inquietas[3].
Etiologicamente, a DVC encontra-se dividida em três classes: congénita (Ec), primária (Ep) ou secundária (Es), havendo, contudo, a possibilidade da não identificação da etiologia subjacente ao processo patológico (En).
No que diz respeito à anatomia venosa do membro inferior, esta é dividida em três sistemas: superficial (As), profundo (Ad) e perfurante (Ap), embora possa não ser possível identificar o sistema venoso atingido (An)[4].
Por fim, a DVC, em termos fisiopatológicos, poderá resultar de um fenómeno de refluxo (Pr), de obstrução (Po), ou da coexistência de ambos (Pr,o), podendo ainda não ser conhecido o processo desencadeante (Pn).
A classificação acima descrita diz respeito ao CEAP básico, usado essencialmente, na prática clínica diária, sendo por isso dotado de um certo grau de simplificação. No entanto, uma forma mais complexa, CEAP avançado, foi desenvolvida, com especial relevância em estudos científicos. Este último adiciona ao primeiro uma classificação anatómica dividida em 18 segmentos venosos, que clarifica a localização dos processos patológicos subjacentes[4]. No sistema superficial estão incluídas telangiectasias e veias reticulares (1), grande veia safena acima do joelho (2), grande veia safena abaixo do joelho (3), pequena veia safena (4) e veias não safenas (5). O sistema venoso profundo engloba a veia cava inferior (6), a veia ilíaca comum (7), a veia ilíaca interna (8), a veia ilíaca externa (9), veias pélvicas como as gonadais e veias do ligamento largo (10), veia femoral comum (11), veia femoral profunda (12), veia femoral (13), veia poplítea (14), veias crurais como tibial anterior, tibial posterior, peroniais (15) e ainda musculares (gastrocnémia e soleal) (16). Por fim, as veias perfurantes encontram-se divididas em perfurantes da coxa (17) e da perna (18).
Tendo por base a classificação CEAP, a doença venosa crónica é definida como qualquer forma de doença venosa desde C0s a C6, inclusive formas como telangiectasia cuja designação de "doença" é muitas vezes controversa, enquanto a insuficiência venosa crónica implica apresentações mais graves como edema (C3), alteração de pigmentação (C4) e úlcera venosa (C5-C6)[3].
Classificar adequadamente a DVC requer um elevado grau de precisão diagnóstica. Como tal, no artigo de revisão da classificação CEAP, foram ainda incluídos 3 níveis de avaliação diagnóstica. O primeiro (L1) inclui história clínica e exame físico completos, assim como estudo doppler portátil; o segundo (L2), exames laboratoriais não invasivos como eco doppler ou pletismografia; enquanto o terceiro (L3) diz respeito a formas diagnósticas mais invasivas ou a estudos imagiológicos mais complexos, como a venografia ascendente ou descendente, medidas de pressão venosa, venografia por tomografia computorizada ou por ressonância magnética[3].
A classificação da doença venosa crónica é um processo dinâmico que se inicia na primeira consulta e evolui ao longo do tempo, de acordo com os estudos efetuados, pelo que a data de examinação é outro dado que deve constar na avaliação CEAP.
Um dos grandes fatores que determinam a importância da classificação CEAP é a sua capacidade de distinguir entre doenças primárias, congénitas e secundárias, uma vez que a terapêutica associada a cada uma das etiologias é diferente.
O Venous Clinical Severity Score (VCSS), usado frequentemente na prática clínica, avalia a severidade da doença venosa crónica, atribuindo uma classificação de 0 a 3 para cada forma de apresentação da DVC [5].
A preocupação estética constitui uma importante motivação para a procura de ajuda médica, contudo, não raras vezes, a sintomatologia intensa constituiu a força motriz. Quando não tratada, a doença progride para uma forma mais severa, podendo cursar com agravamento sintomatológicos, alterações na pigmentação, lipodermatosclerose e ulceração.
Tendo sempre em vista as expetativas do doente, a terapêutica assume, assim, um papel determinante, uma vez que procura otimizar os resultados clínicos, os quais se traduzem pela melhoria dos sintomas e da qualidade de vida que, na realidade, podem nem expressar melhoria clínica significativa[5].
Assim, é importante avaliar o impacto do tratamento na melhoria da qualidade de vida, estando disponíveis uma série de questionários como o Short Form Health Survey (SF-36), o Chronic Venous Insufficiency Questionnaire (CIVIQ), o Venous Insufficiency Epidemiologic and Economic Study Of Quality Of Life (VEINES-QOL/Sym), o Aberdeen Varicose Vein Questionnaire (AVVQ) ou mesmo o Charing Cross Venous Ulceration Questionnaire (CXVUQ), os quais permitem avaliar as alterações nos sinais e sintomas ao longo do tempo e quantificar os resultados.
O SF-36 é uma medida de qualidade de vida genérica, podendo, como tal, ser aplicada em diversas patologias. O CIVIQ, VEINES-QOL/Sym, AVVQ e o CXVUQ são, por outro lado, instrumentos específicos para a doença venosa. Os dois primeiros englobam todo o espetro de manifestação da doença venosa crónica enquanto os últimos focam aspetos particulares da patologia venosa, sendo o AVVQ um questionário direcionado para varizes, enquanto CXVUQ é específico para ulceração venosa[5]. O CIVIQ avalia 4 dimensões: física, psicológica, social e a dor |QUADRO 2|, enquanto o VEINES-QOL/Sym estima o efeito da doença na qualidade de vida e mede os sintomas associados[5]. Estes são normalmente usados em trabalhos de investigação e publicação. A vantagem do CIVIQ sobre os restantes recai sobre o facto de ter sido validado em 10 línguas diferentes.
| QUADRO 2 | Questionário CIVIQ – Perguntas incluídas[6]
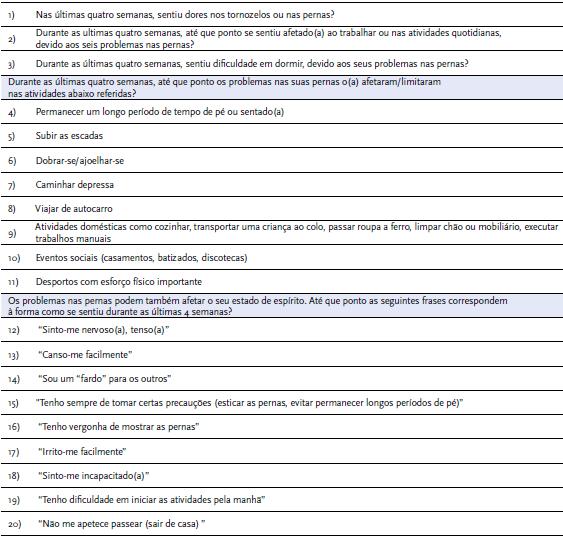
A escolha da abordagem terapêutica é, assim, um processo dinâmico e que deve ter em conta tanto a melhoria clínica como deve procurar satisfazer as necessidades e expectativas dos doentes, devendo todo o procedimento ser devidamente explicado para posteriormente poder ser dado o consentimento explícito por parte do doente.
PONTUAÇÃO
1 Nunca
2 Ocasionalmente
3 Regularmente
4 Frequentemente
5 Sempre
Dimensão física: Questões 5, 6, 7 e 9.
Dimensão psicológica: Questões 12, 13, 14, 15, 16, 17, 18, 19 e 20.
Dimensão social: Questões 8, 10 e 11.
Dimensão dor: Questões 1, 2, 3 e 4.
MATERIAIS E MÉTODOS
Foi efetuada uma pesquisa bibliográfica usando a plataforma Medline, limitada a artigos em língua inglesa, publicados desde 2000 a 2011, segundo a query ("Varicose veins"[MeSH]) OR ("Varicose Veins/drug therapy"[Mesh]) OR ("Varicose Veins/therapy"[Mesh]) OR ("Varicose Veins/surgery" [Mesh]) OR ("Stockings, compression"[MeSH]) OR ("Compression bandages" [MeSH]) OR ("Venous insufficiency"[MeSH]) OR ("Varicose Veins" AND ("Sclerotherapy" OR "Laser therapy"[MeSH])).
A pesquisa foi realizada no período compreendido entre 5 de maio de 2011 e 5 de fevereiro de 2012, tendo sido selecionados os artigos a consultar de acordo com os critérios de pertinência em relação ao tema e disponibilidade do artigo completo. Foram ainda incluídos outros artigos não abrangidos nos resultados da pesquisa, contudo com relevância para o assunto e citados como referência de outros artigos.
MEDIDAS HIGIENO-DIETÉTICAS
Atualmente sabe-se que a idade avançada, história familiar e o sexo constituem fatores de risco imutáveis para o desenvolvimento de doença venosa crónica. Há, contudo, outros que podem ser evitados de forma a atrasar a sua progressão. A Sociedade Portuguesa de Angiologia e Cirurgia Vascular desenvolveu uma lista de 10 conselhos que procuram informar os doentes com DVC acerca das medidas a adotar[6].
Permanecer muitas horas de pé ou sentados, principalmente de pernas cruzadas, deve ser evitado uma vez que poderá conduzir ao desenvolvimento de doença venosa. Caso o trabalho obrigue a permanecer longas horas sentados os doentes devem procurar realizar movimentos circulares com os pés ou caminhar no horário pós laboral.
A prática de exercício regular é também determinante uma vez que estimula a contração muscular e consequentemente o retorno venoso. Devem ser preferidos desportos como a ginástica, natação, ciclismo, dança que promovem a circulação venosa e evitados desportos como basquetebol e ténis que obrigam a movimentos bruscos. Estes últimos induzem variações de pressão nas veias que provocavam a sua dilatação e a diminuição do retorno venoso.
Lugares quentes devem também ser evitados uma vez que dilatam as veias e aumentam a estase. Exposição solar prolongada, banhos quentes, sauna, vestuário quente constituem fatores de risco. Por oposição, passar água fria nas pernas, assim como permanecer em locais frescos é aconselhado, uma vez que estimula o funcionamento venoso e alivia a dor e sensação de pernas pesadas.
A prisão de ventre e excesso de peso aumentam a pressão sanguínea venosa. Os doentes devem realizar uma alimentação rica em fibras (vegetais), com boa hidratação e redução da ingestão de gorduras saturadas (como, por exemplo, manteiga).
Roupa muito apertada comprime as veias e dificulta a circulação pelo que deve ser evitado. O uso de sapatos apropriados é também extremamente importante. Devem ser preferidos saltos de 3-4 cm em detrimento de sapatos de salto e sapatos planos.
Durante o sono, o sistema venoso não é estimulado pelo que é aconselhado a realização de movimentos de pedalar antes de adormecer assim como a elevação dos pés (10 a 15cm da cama).
Massajar as pernas de baixo para cima estimula o retorno venoso, pelo que deve ser efetuado.
A gravidez e a contraceção oral podem agravar a doença venosa crónica, uma vez que os estrogénios aumentam a permeabilidade venosa e a progesterona promove a dilatação[6].
TRATAMENTO FARMACOLÓGICO
Tratar o refluxo e a hipertensão venosa é uma prioridade, contudo reverter os sintomas e melhorar a qualidade de vida é também imperativo, sendo o tratamento farmacológico uma das modalidades terapêuticas capazes de atuar nesse sentido. O tratamento farmacológico está indicado para todas as classes de doença venosa crónica constituindo-se normalmente como um adjuvante ao tratamento compressivo, embora possa constituir uma alternativa ao mesmo, como em situações de doença arterial, infeções da pele, intolerância, fraca compliance ou mesmo em climas muito quentes onde usar meias elásticas se torna insuportável[7].
Os fármacos venoactivos podem ser divididos em agentes naturais e de origem sintética. Os primeiros incluem alfa-benzodiazepinas como a cumarina, flavonoides como a diosmina, fração flavonóica purificada micronizada (FFPM), constituída por 90% de diosmina e 10% de hesperidina, e rutina e rutosido; saponinas como a escina e extrato de ruscus; e outros extratos de plantas como antocianósicos, proantocianidinas e extrato de Ginkgo, heptaminol e troxerrutina. Os agentes sintéticos são o dobesilato de cálcio, naftazona e benzarona[8] |QUADRO 3|.
| QUADRO 3 | Classificação dos principais fármacos venoactivos[8]
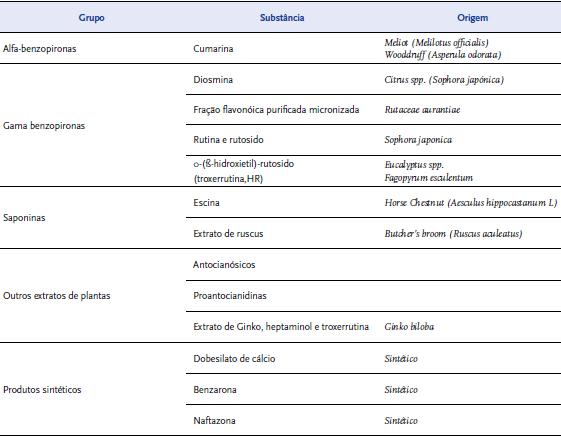
Os mecanismos pelo qual atuam não estão totalmente esclarecidos. No entanto, sabe-se que exercem efeitos a nível da macro e microcirculação. De uma forma geral, os venoactivos aumentam o tónus venoso, diminuem a híper-permeabilidade capilar, exercem efeito ao nível das paredes e válvulas venosas, protegendo as células endoteliais da hipoxia e prevenindo o refluxo venoso. Promovem a melhoria do fluxo linfático, exibem propriedades anti-inflamatórias que se traduzem pela inibição da interação leucócito-endotélio e redução dos radicais livres, assim como melhoram os parâmetros hemorreológicos[6] |QUADRO 4|.
| QUADRO 4 | Modo de ação dos principais fármacos venoactivos[6]
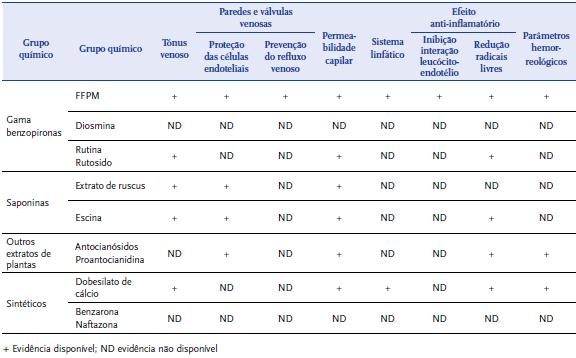
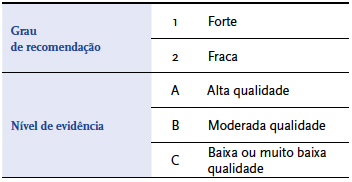
A eficácia dos fármacos venoactivos no alívio de sintomas como dor, cãibras, pernas inquietas, prurido, sensação de pernas pesadas e parestesias foi confirmada por uma revisão sistemática desenvolvida por Martinez et al que incluiu 44 estudos e evidenciou superioridade dos fármacos venoactivos face ao placebo no alívio sintomático[9]. O seu uso é sugerido pelas guidelines do American Venous Fórum com forte grau de recomendação e nível de evidência de moderada qualidade[10] |QUADRO 5|.
| QUADRO 5 | Grau de recomendação e nível de evidência para as guidelines do AVF e SVS/AVF [6, 10]
Apesar de ser um sinal não específico, o edema é extremamente comum na doença venosa crónica sendo tipicamente esporádico, uni ou bilateral, e limitado à extremidade distal dos membros apesar de poder estender-se proximalmente. Este agrava com ortostatismo prolongado e melhora com a elevação do membro[11]. A revisão do grupo Cochrane acima mencionada registou uma associação positiva entre a toma de venoactivos e a redução de edema[9]. Vários estudos têm demonstrado haver superioridade de FFPM, rutosido, escina, dobesilato de cálcio, proantrocianidina e rutina face ao placebo para o tratamento do edema[8]. Os diuréticos constituem a abordagem standard na redução do edema, pelo que também são recomendados.
O AVF sugere o uso de fármacos venoactivos, especialmente os rutosido, diosmina e hesperidina no tratamento do edema dos membros, grau 2B[10].
O crescente interesse na abordagem farmacológica da úlcera venosa ativa (C6), surge associado à dificuldade em tratá-la num curto espaço de tempo. Um estudo confirmou a eficácia do FFPM em úlceras grandes (5-10cm2) e de longa duração (entre 6 a 12 meses) quando associado à terapêutica convencional (compressão e tratamento local adequado)[12]. A pentoxifilina, um vasodilatador cerebral e/ou periférico, também tem mostrado ser efetivo no tratamento da úlcera venosa. Há evidência de que a toma de 400mg, três vezes por dia, promove e acelera a cura da lesão[13].
A pentoxifilina ou FFPM no contexto de úlcera venosa é recomendada pelo AVF, grau 1B[10].
Em geral os fármacos venoactivos são bem tolerados. Os efeitos adversos mais frequentemente observados são a dor abdominal, desconforto gástrico, dispepsia, vómitos e diarreia, insónia, sonolência, vertigens, cefaleias e cansaço, que se manifestam em cerca de 5% dos doentes. A cumarina e benzarona estão ainda associadas a algum grau de hepatotoxicidade[11].
A toma de fármacos venoactivos durante a gravidez tem decorrido sem complicações para alguns agentes, contudo é necessário maior tempo de seguimento para obter o verdadeiro impacto da sua administração em grávidas. Por falta de evidência face à toma de venoactivos durante o aleitamento, este deve ser feito, se feito, com precaução[11].
Podemos aferir que os fármacos venoactivos são adequados para todas as classes de DVC. A sua toma é aconselhada para indivíduos sem sinais de doença venosa crónica que se fazem acompanhar de sintomas (C0s), para telangiectasias e/ou veias reticulares (C1) e varizes tronculares (C2), uma vez que promovem o alívio sintomático que normalmente lhes estão associados. É recomendada a sua toma para redução e prevenção de edema (C3), assim como para alterações tróficas (C4). A abordagem farmacológica constitui, ainda, um importante adjuvante no tratamento de ulceras venosas (C5 e C6) por promover e acelerar o processo de cicatrização[6].
TRATAMENTO COMPRESSIVO
A compressão é a forma de tratamento mais frequentemente usada no contexto de varizes tronculares (C2), edema (C3), alterações da pigmentação da pele (C4) e úlcera venosa ativa (C6).
A compressão elástica promove a reabsorção do edema e previne a sua formação, diminuiu o calibre venoso aumentando consequente a velocidade do fluxo, reduz o refluxo em ortostatismo, o volume residual e a pressão venosa em ambulatório, melhorando, adicionalmente, a contractilidade muscular [14].
A pressão externa pode ser exercida através de meias elásticas, ligaduras elásticas compressivas, botas de Unna, botas ou ligaduras não elásticas e através de aparelhos pneumáticos, sendo as duas primeiras as mais amplamente usadas.
Atualmente existem três modelos de meias elásticas: meias até ao joelho, até à raiz da coxa e collants.
A draft European Standard procurou uniformizar os graus de compressão na Europa. Foi assim estabelecido que compressão grau 1 (ligeira) corresponde a uma pressão externa de 15-21mmHg, grau 2 (média) corresponde a 23-32mmHg, grau 3 (forte) a 34-46mmHg sendo que as meias grau 4 (muito forte) exercem uma pressão superior a 49mmHg[15].
A Sociedade Portuguesa de Angiologia e Cirurgia Vascular publicou, em Julho de 2011, recomendações no diagnóstico e tratamento da doença venosa crónica, das quais consta a compressão indicada para cada classe CEAP de doença venosa crónica[6].
Para C0s deve realizar-se compressão ligeira, enquanto para C1 e C2 estão indicadas tanto a ligeira como a moderada[6].
Para reduzir e prevenir o edema (C3), deverá ser exercida compressão na ordem dos 23-32mmHg, a qual é ainda recomendada para a abordagem das alterações tróficas (C4) [6].
No contexto de úlceras venosas cicatrizadas, a aplicação de uma pressão externa de grau moderado ou forte é o mais indicado[6].
A compressão elástica constitui a terapêutica de eleição na cura de úlceras venosas ativas, sendo as ligaduras elásticas as mais adequadas para o efeito[6].
Apesar de a sua eficácia estar comprovada e de o seu uso recomendado, esta metodologia terapêutica não atrasa a progressão da doença nem previne a recorrência de varizes[15]. Assim, esta abordagem não constitui o tratamento primário para doentes candidatos à ablação da veia safena, o que é apoiado por um estudo de Michels et al. que concluiu que o tratamento cirúrgico apresentava alívio sintomático e melhoria da qualidade de vida superiores que às proporcionadas pelo tratamento compressivo[16]. A relação custo-benefício privilegiou ainda a abordagem cirúrgica.
A compressão pós cirúrgica é largamente usada para prevenir tromboembolismo, reduzir a hemorragia, os hematomas, o edema e a dor.
Houtermans-Auckel et al concluíram que o uso de ligaduras elásticas, durante 3 dias após o stripping, seria suficiente para o controlo do edema, dor e outras complicações e que a aplicação de meias elásticas, após este período, não adicionaria qualquer benefício[17]. Outro ensaio clínico considerou que o uso de meias elásticas durante uma semana, após a aplicação de ligaduras elásticas, seria benéfico, não sendo necessário usá-las por períodos de tempo mais alargados[18].
Prescrever compressões inadequadamente excessivas em doentes com patologia venosa poderá conduzir a necrose por pressão e, se aplicadas num membro com doença arterial adicional, poderá levar a insuficiente perfusão do membro que possivelmente culminará na amputação do mesmo[15]. A meia ou ligadura podem ainda causar efeito de torniquete[15]. Assim sendo, é recomendado que a pressão externa seja prescrita por clínicos experientes de forma a minimizar os possíveis malefícios descritos previamente[19].
Um dos grandes problemas associados a esta abordagem é o elevado número de indivíduos que abandonam o tratamento. O calor incapacitante, associado ao seu uso, e o custo da aquisição constituem os principais fatores de dropout terapêutico. Doentes idosos com comorbilidades, como osteoartrite, doença reumática, entre outras, assim como indivíduos obesos, têm grande dificuldade em aplicar os sistemas de compressão, pelo que requerem ajuda diária [17].
ABLAÇÃO MECÂNICA
A ablação mecânica inclui técnicas como o stripping e a flebectomia que procuram tratar o refluxo e hipertensão venosa através da remoção de varizes, e outras como a CHIVA (cure conservatrice et hémodynamique de l’insiffisance veineuse en ambulatiore) e ASVAL (ablation sélective des varices sous anesthesié locale) que o fazem através da preservação da veia safena.
A laqueação da junção safeno-femoral é uma das formas mais antigas de tratamento da doença venosa crónica. No entanto, por estar associada a elevadas taxas de recorrência, foi necessário desenvolver uma técnica mais efetiva[20]. No início do século XX, o stripping é, assim, adicionado à laqueação simples[20]. Ao longo do tempo esta técnica foi sofrendo diversas modificações, pelo que atualmente é um procedimento muito menos invasivo, o que permite que o doente regresse a casa no próprio dia da intervenção e retome a sua atividade profissional no dia seguinte.
Apesar de ser considerada, até à data, a abordagem padrão no tratamento de varizes[21], resultados recentes, associados a técnicas como a ablação a laser ou por radiofrequência, têm vindo a tornar-se alternativas eficazes.
A safenectomia é realizada em ambulatório sob anestesia geral, regional ou local, estando disponíveis duas formas de intervenção: stripping convencional e por invaginação.
Na abordagem convencional é usado o aparelho de babcock, cuja ponta em forma de "bolota" é colocada no topo do stripper o qual é posteriormente puxado no sentido descendente, arrastando consigo a veia, enquanto na ablação por invaginação a safena é ligada à extremidade superior do stripper e, à medida que a inferior é puxada, a veia invagina para o próprio lúmen[10]. A grande diferença entre ambas prende-se com o facto de a primeira poder danificar o tecido perivenoso e causar, adicionalmente, lesão nervosa ou linfática[22].
Quando comparadas, foi possível concluir que o stripping por invaginação atenua a perda sanguínea, está associado a menor formação de coágulos, menor sensação dolorosa e menor lesão nervosa, apresentando ainda efeitos cosméticos de maior qualidade[22], o que a torna mais indicada no tratamento da doença venosa crónica.
A grande veia safena é raramente removida abaixo do nível do joelho devido ao elevado risco de lesão do nervo safeno, uma vez que este descreve um trajeto muito próximo da veia, principalmente junto ao maléolo medial[23]. O stripping parcial permite que a porção distal da grande veia safena possa ser usada para um eventual bypass futuro.
O American Venous Forum recomenda laqueação da junção safeno-femoral e safenectomia por invaginação até ao nível do joelho, grau 1B[10].
Rasmussen et al observou infeção na incisão inguinal, tromboflebite, equimoses e hematomas em 2%, 3%, 25% e 8% dos membros submetidos a stripping por invaginação, respetivamente[24]. A qualidade de vida, avaliada pelo VCSS, AVVQ e pelo SF-36, melhorou significativamente com esta abordagem[24]. Wood et al documentou alterações neurológicas sensitivas em 27% dos membros tratados com remoção parcial da grande veia safena por invaginação, às 6 semanas mas, aos 12 meses, apenas 12.7% dos indivíduos tratados mantinham estas alterações[25]. As lesões nervosas decorrentes da safenectomia estão, normalmente, associadas a reduzida morbilidade[23].
Rasmussen et al, após dois anos de seguimento, observou recorrência em 37% dos indivíduos. Os autores afirmam poder dever-se a erros estratégicos e técnicos, assim como à neovascularização e à progressão da doença[26].
Após a cirurgia de remoção de varizes safenas é comum realizar, concomitantemente, flebectomia para exérese de trajetos varicosos associados.
Um estudo foi desenvolvido no sentido de observar a eventual regressão espontânea dos trajetos varicosos remanescentes após a remoção da grande veia safena[27]. Os resultados apoiaram a hipótese pelo que os autores sugerem que uma abordagem terapêutica focada na irradicação da fonte de hipertensão poderá diminuir a necessidade de tratar as veias remanescentes por flebectomia. Como tal, apontam a necessidade de um seguimento mais prolongado após a remoção da safena no sentido de averiguar quais as varizes que regridem espontaneamente e quais as que efetivamente necessitam ser removidas[27].
Estes resultados põem em causa a realização de flebectomia concomitantemente à safenectomia, o que implicaria uma segunda ocupação da sala de intervenção, estando assim associado a um gasto acrescido. Para além disso, tornaria o tratamento da doença venosa crónica um processo mais moroso, o que pode não corresponder às expectativas do doente. Esta prática alternativa poderia ser vantajosa na medida em que reduziria o número de incisões e consequentemente as complicações que lhe estão associadas.
A flebectomia transiluminada permite a visualização direta das veias que serão removidas, requer menor número de incisões e reduz a quantidade de varizes residuais, estando associada a uma diminuição considerável do tempo de intervenção quando comparada com a convencional[28]. Não foram observadas diferenças estatisticamente significativas no que diz respeito às variáveis dor, celulite, lesão nervosa, equimoses, veias residuais, recorrência, efeitos cosméticos e satisfação avaliadas no mesmo estudo[28].
Apesar das vantagens mencionadas, a flebectomia transiluminada é uma técnica mais dispendiosa[28] e realizada sob anestesia geral ou regional com sedação, contrariamente à convencional[29].
O AVF recomenda flebectomia para a remoção de varizes, após safenectomia, tanto durante o mesmo procedimento como num período posterior com grau de recomendação e evidência 1B[10]. A flebectomia transiluminada constitui uma alternativa à convencional apesar da fraca evidência para o seu uso (2C)[10].
ABLAÇÃO TÉRMICA
A ablação térmica endovenosa é um tratamento percutâneo e minimamente invasivo que tem demostrado ser extremamente eficaz no tratamento da incompetência das veias safenas. Desta fazem parte a ablação a laser e por radiofrequência.
O procedimento é realizado em ambulatório com anestesia local tumescente. A fibra de laser ou cateter de radiofrequência, guiados ecograficamente, são introduzidos no interior da safena incompetente[30]. O sistema, uma vez ativado, gera calor, o qual promove lesão endotelial com consequente contração venosa e oclusão fibrótica[30].
A obstrução venosa parcial secundária a um episódio de tromboflebite, assim como veias extremamente tortuosas, dificultam a introdução da fibra ou cateter, pelo que constituem possíveis contraindicações para ablação térmica[31]. Indivíduos com varizes mais superficiais ou com dilatação aneurismática da junção safeno-femoral devem ser submetidos a safenectomia. Coagulopatia não controlada, disfunção hepática que limite a administração de anestesia local, imobilidade, gravidez e amamentação são outros critérios de exclusão relativos[31].
A ablação a laser é recomendada no tratamento de telangiectasias, grau 1A[10], no entanto, está mais indicada para as localizadas na face e no peito.
A trombose venosa superficial é esperada no contexto de ablação térmica, contudo esta técnica pode tanto potenciar o desenvolvimento de trombose profunda como promover a extensão do trombo do sistema superficial para o profundo[32]. Marsh et al observou trombose venosa profunda em 1% dos membros submetidos a ablação a laser e 0.7% com radiofrequência, sendo que um dos indivíduos deste grupo desenvolveu tromboembolismo pulmonar[32].
A realização de profilaxia antitrombótica é um assunto dotado de alguma controvérsia. Esta é aconselhada em indivíduos com história de tromboflebite, trombose venosa profunda, trombofilia e obesidade[33]. Puggioni et al concluiu que deve ser considerada em pacientes com idade superior a 50anos[34], enquanto Enoch et al afirma que deve ser realizada apenas em grupos de risco aumentado, apesar de considerar ser difícil estabelecer até que ponto sofrer de doença venosa crónica constitui um risco desta ordem[35].
A ablação a laser pode desenvolver outras complicações como a tromboflebite (2.5%), equimoses ligeiras (15.9%) ou moderadas (25.4%), celulite (2%), edema (0.9%), neovascularização e inflamação perivenosa (0.9%) e parestesias (0.5%)[36].
A ablação por radiofrequência pode causar queimaduras da pele (1.2%), não obstante a sua incidência ter diminuído significativamente após a introdução da anestesia tumescente à técnica, flebite (2.9%), infeção no local de acesso à veia (0.2%) e parestesias (12.3%), sendo que aos cinco anos apenas 2.6% mantinha alterações desta ordem)[37].
Têm sido documentadas altas taxas de oclusão no seguimento da ablação a laser, o que foi demostrado por um estudo da Society for Clinical Vascular Surgery, que registou 98.7% de oclusão aos 6 meses e 91.4% aos 30 meses, o que corrobora os resultados publicados noutros estudos e mencionados no mesmo artigo[36]. Contudo, o sucesso terapêutico num ensaio clínico realizado por Myers et al foi consideravelmente inferior, sendo que aos quatro anos apenas 75% dos indivíduos submetidos a ablação a laser mantinham oclusão venosa[38].
Quanto à abordagem por radiofrequência, a taxa de oclusão imediata observada por Merchant et al foi de 96.8%, decaindo para 87.2% ao fim de cinco anos[37]. Neste contexto foram definidos três tipos de falência anatómica que justificam o observado:
Tipo I (não oclusão) – veias não sofreram oclusão com o tratamento e mantiveram-se sempre permeáveis ao longo do seguimento (12.4%).
Tipo II (recanalização) – veias que inicialmente ocluiram mas recanalizaram total ou parcialmente (69.7%).
Tipo III (refluxo inguinal) – após a oclusão, algumas veias desenvolveram refluxo na região inguinal envolvendo frequentemente uma veia acessória (17.8%)[37].
Tanto a ablação a laser como com radiofrequência estão associadas a melhoria significativa da qualidade de vida proporcionando ainda um rápido regresso às atividades da vida diária e às profissionais [39].
O American Venous Fórum considera as abordagens térmicas efetivas no tratamento da incompetência safena, com grau de recomendação e evidência 1A[10].
ABLAÇÃO QUÍMICA
A escleroterapia, apesar de amplamente aplicada no tratamento de telangiectasias e veias reticulares, tem vindo a ganhar algum terreno no tratamento de veias safenas incompetentes e das suas tributárias, por ser uma técnica minimamente invasiva.
Esta consiste na administração endovenosa de esclerosantes que provocam lesão endotelial e exposição das fibras de colagénio, tornando-as sujeitas à ação dos agentes. A cascata de coagulação é ativada, o que potencia a formação de trombos com consequente oclusão venosa. Todos os esclerosantes, embora atuem de forma diferente, produzem o mesmo efeito, divergindo apenas na eficácia, potência e reações adversas[40].
Os agentes esclerosantes estão divididos de acordo com o seu mecanismo de ação, sendo estes classificados de osmóticos, detergentes e alcoólicos.
Os primeiros dizem respeito a soluções salinas hipertónicas indicadas no tratamento de telangiectasias e veias reticulares[40]. A sua administração está associada a elevada sensação álgica[41] podendo induzir necrose tecidual massiva secundária ao extravasamento, mesmo quando pequenos volumes do agente ultrapassam a veia[40]. A solução salina hipertónica constitui uma alternativa aos detergentes quando os doentes desenvolvem reações alérgicas aos mesmos[40].
Entre os detergentes destacam-se o tetradecil sulfato de sódio e o polidocanol. O primeiro é considerado um fármaco eficiente[41] e indolor à injeção[40]. Está, contudo, associado a elevada incidência de hiperpigmentação (cerca de 30% dos doentes), a significativa necrose tecidual por extravasamento e a alguns casos de anafilaxia[41]. O polidocanol, para além de indolor, não produz necrose e apresenta baixa incidência de reações alérgicas[41]. Ocasionalmente provoca hiperpigmentação embora em menor proporção que os restantes agentes[41].
A glicerina cromada, um agente alcoólico, pode ser aplicada em telangiectasias e veias reticulares, apesar de ser considerado um fraco esclerosante[42].
A ablação química pode ser realizada na forma líquida e em espuma. Na primeira, os esclerosantes são diluídos e a concentração ajustada ao diâmetro venoso enquanto na segunda os agentes são misturados com gás, o que permite a formação de micelas que exercem maior contacto entre a parede venosa e o detergente[43]. Desta forma o volume de esclerosante necessário para que a oclusão venosa se verifique é menor, o que torna a escleroterapia com espuma mais potente e menos tóxica que a formulação líquida[40, 44].
Para o tratamento de telangiectasias e veias reticulares, o AVS recomenda a escleroterapia grau 1B[10], sendo que a Society of Vascular Surgery juntamente com o American Venous Forum (SVS/AVF) consideram a líquida mais eficaz [19].
Para varizes não safenas é sugerida a escleroterapia, grau 2B[10], sendo que o SVS/AVF refere haver maior eficiência com o uso da formulação em espuma[19].
Vários estudos documentaram superioridade da escleroterapia com espuma face à líquida no tratamento das veias safenas[45, 46]; no entanto, existe muito fraca evidência acerca da sua eficácia e durabilidade, pelo que o SVS/AVF se refere à escleroterapia como uma opção terapêutica com grau de recomendação e evidência 2C[19].
A ablação química está contraindicada em indivíduos com alergia severa aos detergentes e com trombose venosa profunda ou superficial[44]. A sua administração na presença de buraco ovale patente, está associado a alguma controvérsia [44].
As complicações mais frequentes da escleroterapia são alteração da pigmentação da pele, tromboflebite e trombose venosa comuns a ambas as formas de escleroterapia[47].
A ablação química pode ainda desencadear uma série de efeitos sistémicos, os quais, apesar de mais frequentes na escleroterapia com espuma podem também ser observados na líquida[48]. As partículas de gás podem embolizar e causar efeitos pulmonares, visuais e cerebrais, observados particularmente em indivíduos com buraco ovale patente ou shunt direito - esquerdo[49]. Bergan et al observou dor no peito, tosse seca, alterações visuais em 4, 3 e 2 indivíduos, respetivamente, de 416 tratados com escleroterapia[50]. Um caso de acidente vascular cerebral fatal foi registado após a injeção de espuma, num indivíduo com buraco ovale patente largo e não diagnosticado[51].
Um ano após ablação safena por escleroterapia com espuma, foi possível observar sucesso terapêutico em 77% dos indivíduos num estudo realizado por Gonzalez-Zeh et al[52], enquanto Darvall et al observou oclusão venosa em 87.8%[53]. Aos três anos, Myers et al documentou apenas 52.4% de sucesso com a ablação química[54].
Thomasset et al concluiu que a compliance, face ao uso de meias elásticas, é o fator mais importante para garantir o sucesso da escleroterapia com espuma das veias safenas[55].
COMPARAÇÃO ENTRE AS TÉCNICAS
É importante estabelecer a comparação entre as várias técnicas no sentido de averiguar aquela mais adequada para o tratamento de varizes.
Quando comparado o stripping por invaginação com a ablação a laser, Ramusen et al concluiu que ambas as técnicas seriam eficazes na eliminação do refluxo da grande veia safena, no alívio sintomático e na melhoria da qualidade de vida[24]. Não foram encontradas diferenças estatisticamente significativas entre os grupos, no que diz respeito à recorrência.[26]
A radiofrequência demonstrou ter maior impacto na melhoria da qualidade de vida e na brevidade no regresso às atividades da vida diária quando comparada com a safenectomia [56], no entanto, foram obtidos resultados semelhantes no que diz respeito à eficácia clínica, à recorrência e à neovascularização[56]. Outro estudo documentou menor sensação álgica, menor número de equimoses e menor durabilidade de execução técnica com ablação por radiofrequência[57].
O SVS/AVF recomenda a ablação a laser ou radiofrequência em detrimento do stripping (grau de recomendação e evidência 1B)[19].
Almeida et al, ao comparar as técnicas de ablação térmica, registou superioridade da radiofrequência no recobro e parâmetros alusivos à qualidade de vida[58]. Complicações como a tromboflebite foram significativamente mais incidentes após intervenção a laser[58].Outro estudo registou superioridade da ablação a laser face ao estreitamento venoso e recanalização[59].
Bountouroglu et al comparou escleroterapia com espuma com a safenectomia por invaginação[60]. A escleroterapia revelou ser mais económica e rápida de realizar, associada a uma recuperação mais célere e a uma melhoria de qualidade de vida mais pronunciada. As complicações foram pouco frequentes em ambos os grupos. As percentagens de obliteração a curto prazo (três meses) favoreceram o stripping (93%), face à escleroterapia com espuma (87%)[60]. Kalodiki et al concluiu que aos três e cinco anos de seguimento, as abordagens em questão, eram igualmente efetivas[61].
Rasmussen et al desenvolveu um ensaio clinico randomizado que comparou todas as técnicas acima mencionadas, stripping, ablação térmica com laser e por radiofrequência e ablação química com espuma, no tratamento da incompetência da grande veia safena[21].
A melhoria da qualidade de vida foi observada com todas as formas de ablação venosa. No entanto, as variáveis dor e dimensão física, avaliadas pelo SF-36, beneficiaram com a radiofrequência e escleroterapia [21]. Adicionalmente, as duas técnicas mencionadas proporcionaram regressar às atividades da vida diária e ao trabalho mais rapidamente[21].
As complicações foram essencialmente minor. Foi registado um caso de trombose venosa com tromboembolismo pulmonar no seguimento de escleroterapia e outro de trombose venosa profunda após safenectomia[21]. A tromboflebite foi significativamente mais incidente nos indivíduos submetidos a radiofrequência e escleroterapia[21].
A recorrência, após um ano de seguimento, foi de 14.8%, 13.8%, 11.6%, 7.3% no stripping, escleroterapia com espuma, ablação endovenosa a laser e radiofrequência, respetivamente. Estas diferenças não foram, contudo, estatisticamente significativas[21].
Após um ano de seguimento, a falência terapêutica foi mais incidente com a ablação química (16.3%) [21], sendo o stripping a técnica que apresentou percentagens de recorrência mais elevadas (14.8% contra 13.8%, 11.6% e 7.3% com escleroterapia, laser e radiofrequência, respetivamente) [21].
As abordagens mais dispendiosas são a radiofrequência e o laser sendo a escleroterapia a mais económica[21]. No entanto, quando adicionados os custos inerentes à da perda de dias de trabalho, embora a escleroterapia continue a ser mais económica, a radiofrequência torna-se a segunda mais barata[21].
É importante realçar que seria necessário um período de seguimento mais alargado para se estabelecer o sucesso terapêutico real. Para além disso, atualmente é possível regressar às atividades da vida diária e ao trabalho no dia seguinte à intervenção, com qualquer uma das técnicas mencionadas, o que de certa forma anula o efeito dos custos relativos à perda de dias de trabalho.
Ao longo desta revisão foi ainda referido que tanto a flebectomia como a escleroterapia seriam eficientes no tratamento de varizes não safenas, grau de recomendação 1B e 2B respetivamente[10]. Um estudo que procurou comparar ambas as técnicas, concluiu haver menor taxa de recorrência com a primeira, sendo que consideram a flebectomia uma técnica eficaz no tratamento de varizes[62].
CONCLUSÃO
As varizes sintomáticas e edema beneficiam com a toma de fármacos venoactivos, assim como do uso concomitante de tratamento compressivo (grau 2B)[10]. Ambas as metodologias terapêuticas estão indicadas para todas as classes de DVC desde C1 a C6.
As telangiectasias e varizes reticulares (C1) devem ser tratadas com escleroterapia (grau 1A) [10], sendo a forma líquida a mais recomendada[19]. Os detergentes devem ser preferidos; contudo, a solução salina hipertónica constitui uma alterativa em caso de alergia ao primeiro.
Para o tratamento da incompetência da grande ou pequena safenas, é recomendado a ablação a laser ou radiofrequência em detrimento do stripping clássico com grau de recomendação e evidência 1B[19]. O American Venous Forum recomenda laqueação da junção safeno-femoral e safenectomia por invaginação até ao nível do joelho, grau 1B[10]. Devido à fraca evidência, no que diz respeito à eficácia e durabilidade da técnica, a escleroterapia constitui uma alternativa no tratamento das veias safenas, grau 2C[19].
Para o tratamento das tributárias incompetentes, tanto a flebectomia como a escleroterapia são eficazes (grau 1B)[19]; todavia, o AVF sugere o uso da primeira em detrimento da segunda com grau de recomendação e evidência 2B[10]. A flebectomia transiluminada constitui uma alternativa à flebectomia tradicional, apesar da fraca evidência para o seu uso (grau 2C)[10]. Caso se opte pela realização de escleroterapia, a formulação com espuma tem mostrado ser mais efetiva no tratamento de varizes[19].
Alterações tróficas beneficiam com tratamento farmacológico, compressivo, assim como com a ablação das fontes de refluxo e hipertensão venosas subjacentes ao processo.
A compressão constitui o tratamento de eleição para a cura de úlceras venosas ativas (grau 1B)[19], sendo recomendado o uso de ligaduras elásticas. O tratamento farmacológico poderá constituir um adjuvante, uma vez que acelera o processo de cura. Para úlceras grandes e de longa duração, é recomendado o uso de pentoxifilina e FFPM associado à compressão, grau 1B[10]. Para evitar a recorrência da lesão deve ser realizada a ablação das veias incompetentes e aplicada compressão elástica por um longo período de tempo[19].
Com esta revisão foi ainda possível concluir que:
1. A incompetência venosa é uma doença crónica.
2. O tratamento da doença venosa crónica deve ser individualizado e estar de acordo com o estádio clínico da doença.
3. O tratamento inclui medidas higieno-dietéticas, farmacoterapia, compressão elástica e terapêuticas ablativas.
4. As medidas higieno-dietéticas devem ser adotadas por todos os doentes.
5. Os diferentes graus de compressão devem ser adequados à classificação CEAP.
6. A farmacoterapia promove alívio sintomático e melhoria das complicações decorrentes da doença. Esta inclui fármacos venoactivos e diuréticos.
7. Todas as técnicas podem ser, atualmente, realizadas em ambulatório.
8. A ablação térmica é prometedora, desconhecendo-se, no entanto, as taxas de recorrência a longo prazo.
9. A ablação química com espuma é a técnica mais barata, contudo, está associada a maior incidência de pigmentação e de recanalização.
10. As modernas técnicas de ablação mecânica, incluindo a flebectomia hemodinâmica em ambulatório, não necessitam de anestesia geral e permitem retomar as atividades profissionais no dia seguinte à intervenção.
BIBLIOGRAFIA
[1] EBERHARDT, R.T. AND J.D. RAFFETTO, Chronic venous insufficiency. Circulation, 2005. 111(18): p. 2398-409. [ Links ]
[2] CARPENTIER, P.H., et al., Prevalence, risk factors, and clinical patterns of chronic venous disorders of lower limbs: a population-based study in France. J Vasc Surg, 2004. 40(4): p. 650-9. [ Links ]
[3] EKLOF, B., et al., Updated terminology of chronic venous disorders: the VEIN-TERM transatlantic interdisciplinary consensus document. J Vasc Surg, 2009. 49(2): p. 498-501. [ Links ]
[4] EKLOF, B., et al., Revision of the CEAP classification for chronic venous disorders: consensus statement. J Vasc Surg, 2004. 40(6): p. 1248-52. [ Links ]
[5] VASQUEZ, M.A. and C.E. MUNSCHAUER, Venous Clinical Severity Score and quality-of-life assessment tools: application to vein practice. Phlebology, 2008. 23(6): p. 259-75. [ Links ]
[6] MATOS, A.A., MANSILHA, A., BRANDÃO, E.S., CÁSSIO, I., BARBOSA, J., FRANÇA, J., MACEDO, M., CORREIA, P., ALMEIDA, R., ed. Recomendações no diagnóstico e tratamento da doença venosa crónica. Sociedade Portuguesa de Angiologia e Cirurgia Vascular ed. 2011, Sociedade Portuguesa de Angiologia e Cirurgia Vascular. 52. [ Links ]
[7] RAMELET, A.A., et al., Veno-active drugs in the management of chronic venous disease. An international consensus statement: current medical position, prospective views and final resolution. Clin Hemorheol Microcirc, 2005. 33(4): p. 309-19. [ Links ]
[8] PERRIN, M. and A.A. RAMELET, Pharmacological treatment of primary chronic venous disease: rationale, results and unanswered questions. Eur J Vasc Endovasc Surg, 2011. 41(1): p. 117-25. [ Links ]
[9] MARTINEZ, M.J., et al., Phlebotonics for venous insufficiency. Cochrane Database Syst Rev, 2005(3): p. CD003229. [ Links ]
[10] GLOVICZKI, P. and M.C. DALSING, Handbook of venous disorders : guidelines of the American Venous Forum. 3rd ed2009, London ;: Hodder Arnold. xxiii, 744 p. [ Links ]
[10] NICOLAIDES, A.N., et al., Management of chronic venous disorders of the lower limbs: guidelines according to scientific evidence. Int Angiol, 2008. 27(1): p. 1-59. [ Links ]
[12] COLERIDGE-SMITH, P., C. LOK, and A.A. RAMELET, Venous leg ulcer: a meta-analysis of adjunctive therapy with micronized purified flavonoid fraction. Eur J Vasc Endovasc Surg, 2005. 30(2): p. 198-208. [ Links ]
[13] BEVIS, P. and J. EARNSHAW, Venous ulcer review. Clin Cosmet Investig Dermatol, 2011. 4: p. 7-14. [ Links ]
[14] FELTY, C.L. and T.W. ROOKE, Compression therapy for chronic venous insufficiency. Semin Vasc Surg, 2005. 18(1): p. 36-40. [ Links ]
[15] PALFREYMAN, S.J. and J.A. MICHAELS, A systematic review of compression hosiery for uncomplicated varicose veins. Phlebology, 2009. 24 Suppl 1: p. 13-33. [ Links ]
[16] MICHAELS, J.A., et al., Randomised clinical trial, observational study and assessment of cost-effectiveness of the treatment of varicose veins (REACTIV trial). Health Technol Assess, 2006. 10(13): p. 1-196, iii-iv. [ Links ]
[17] HOUTERMANS-AUCKEL, J.P., et al., To wear or not to wear compression stockings after varicose vein stripping: a randomised controlled trial. Eur J Vasc Endovasc Surg, 2009. 38(3): p. 387-91. [ Links ]
[18] BISWAS, S., A. CLARK, and D.A. SHIELDS, Randomised clinical trial of the duration of compression therapy after varicose vein surgery. Eur J Vasc Endovasc Surg, 2007. 33(5): p. 631-7. [ Links ]
[19] GLOVICZKI, P., Highlights Of The SVS/AVF Document On The Treatment Of Lower Extremity Varicose Veins, in 38th Annual Vascular and Endovascular Issues, Techniques and Horizons (VEITHsymposium),2011, Division of Vascular and Endovascular Surgery, Mayo Clinic, Rochester, MN: New York City. [ Links ]
[20] VAN DEN BREMER, J. and F.L. MOLL, Historical overview of varicose vein surgery. Ann Vasc Surg, 2010. 24(3): p. 426-32. [ Links ]
[21] RASMUSSEN, L.H., et al., Randomized clinical trial comparing endovenous laser ablation, radiofrequency ablation, foam sclerotherapy and surgical stripping for great saphenous varicose veins. Br J Surg, 2011. 98(8): p. 1079-87. [ Links ]
[22] SCHELTINGA, M.R., et al., Conventional versus invaginated stripping of the great saphenous vein: a randomized, double-blind, controlled clinical trial. World J Surg, 2007. 31(11): p. 2236-42. [ Links ]
[23] MORRISON, C. and M.C. DALSING, Signs and symptoms of saphenous nerve injury after greater saphenous vein stripping: prevalence, severity, and relevance for modern practice. J Vasc Surg, 2003. 38(5): p. 886-90. [ Links ]
[24] RASMUSSEN, L.H., et al., Randomized trial comparing endovenous laser ablation of the great saphenous vein with high ligation and stripping in patients with varicose veins: short-term results. J Vasc Surg, 2007. 46(2): p. 308-15. [ Links ]
[25] WOOD, J.J., et al., A prospective study of cutaneous nerve injury following long saphenous vein surgery. Eur J Vasc Endovasc Surg, 2005. 30(6): p. 654-8. [ Links ]
[26] RASMUSSEN, L.H., et al., Randomised clinical trial comparing endovenous laser ablation with stripping of the great saphenous vein: clinical outcome and recurrence after 2 years. Eur J Vasc Endovasc Surg, 2010. 39(5): p. 630-5. [ Links ]
[27] MONAHAN, D.L., Can phlebectomy be deferred in the treatment of varicose veins? J Vasc Surg, 2005. 42(6): p. 1145-9. [ Links ]
[28] AREMU, M.A., et al., Prospective randomized controlled trial: conventional versus powered phlebectomy. J Vasc Surg, 2004. 39(1): p. 88-94. [ Links ]
[29] SPITZ, G., Transilluminated powered phlebectomy in an office setting: procedural considerations and clinical outcomes. J Endovasc Ther, 2011. 18(5): p. 734-8. [ Links ]
[30] LEOPARDI, D., et al., Systematic review of treatments for varicose veins. Ann Vasc Surg, 2009. 23(2): p. 264-76. [ Links ]
[31] GLOVICZKI, P., et al., The care of patients with varicose veins and associated chronic venous diseases: clinical practice guidelines of the Society for Vascular Surgery and the American Venous Forum. J Vasc Surg, 2011. 53(5 Suppl): p. 2S-48S. [ Links ]
[32] MARSH, P., et al., Deep vein thrombosis (DVT) after venous thermoablation techniques: rates of endovenous heat-induced thrombosis (EHIT) and classical DVT after radiofrequency and endovenous laser ablation in a single centre. Eur J Vasc Endovasc Surg, 2010. 40(4): p. 521-7. [ Links ]
[33] GEERTS, W.H., et al., Prevention of venous thromboembolism: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest, 2008. 133(6 Suppl): p. 381S-453S. [ Links ]
[34] PUGGIONI, A., et al., Endovenous laser therapy and radiofrequency ablation of the great saphenous vein: analysis of early efficacy and complications. J Vasc Surg, 2005. 42(3): p. 488-93. [ Links ]
[35] ENOCH, S., E. Woon, and S.D. Blair, Thromboprophylaxis can be omitted in selected patients undergoing varicose vein surgery and hernia repair. Br J Surg, 2003. 90(7): p. 818-20. [ Links ]
[36] KNIPP, B.S., et al., Endovenous laser ablation: venous outcomes and thrombotic complications are independent of the presence of deep venous insufficiency. J Vasc Surg, 2008. 48(6): p. 1538-45. [ Links ]
[37] MERCHANT, R.F. and O. PICHOT, Long-term outcomes of endovenous radiofrequency obliteration of saphenous reflux as a treatment for superficial venous insufficiency. J Vasc Surg, 2005. 42(3): p. 502-9; discussion 509. [ Links ]
[38] MYERS, K.A. and D. JOLLEY, Outcome of endovenous laser therapy for saphenous reflux and varicose veins: medium-term results assessed by ultrasound surveillance. Eur J Vasc Endovasc Surg, 2009. 37(2): p. 239-45. [ Links ]
[39] SHEPHERD, A.C., et al., Randomized clinical trial of VNUS ClosureFAST radiofrequency ablation versus laser for varicose veins. Br J Surg, 2010. 97(6): p. 810-8. [ Links ]
[40] DUFFY, D.M., Sclerosants: a comparative review. Dermatol Surg, 2010. 36 Suppl 2: p. 1010-25. [ Links ]
[41] BERGAN, J.J., The vein book2007, Amsterdam ; Boston: Elsevier Academic Press. xvii, 617 p. [ Links ]
[42] KERN, P., Sclerotherapy of varicose leg veins. Technique, indications and complications. Int Angiol, 2002. 21 (2 Suppl 1): p. 40-5. [ Links ]
[43] KERN, P., et al., Single-blind, randomized study comparing chromated glycerin, polidocanol solution, and polidocanol foam for treatment of telangiectatic leg veins. Dermatol Surg, 2004. 30(3): p. 367-72; discussion 372. [ Links ]
[44] BREU, F.X. and S. GUGGENBICHLER, European Consensus Meeting on Foam Sclerotherapy, April, 4-6, 2003, Tegernsee, Germany. Dermatol Surg, 2004. 30(5): p. 709-17; discussion 717. [ Links ]
[45] RABE, E., et al., Efficacy and safety of great saphenous vein sclerotherapy using standardised polidocanol foam (ESAF): a randomised controlled multicentre clinical trial. Eur J Vasc Endovasc Surg, 2008. 35(2): p. 238-45. [ Links ]
[46] OUVRY, P., et al., Efficacy of polidocanol foam versus liquid in sclerotherapy of the great saphenous vein: a multicentre randomised controlled trial with a 2-year follow-up. Eur J Vasc Endovasc Surg, 2008. 36(3): p. 366-70. [ Links ]
[47] COLERIDGE SMITH, P., Saphenous ablation: sclerosant or sclerofoam? Semin Vasc Surg, 2005. 18(1): p. 19-24. [ Links ]
[48] COLERIDGE SMITH, P., Foam and liquid sclerotherapy for varicose veins. Phlebology, 2009. 24 Suppl 1: p. 62-72. [ Links ]
[49] MORRISON, N., et al., Comparisons of side effects using air and carbon dioxide foam for endovenous chemical ablation. J Vasc Surg, 2008. 47(4): p. 830-6. [ Links ]
[50] BERGAN, J., L. PASCARELLA, and L. MEKENAS, Venous disorders: treatment with sclerosant foam. J Cardiovasc Surg (Torino), 2006. 47(1): p. 9-18. [ Links ]
[51] FORLEE, M.V., et al., Stroke after varicose vein foam injection sclerotherapy. J Vasc Surg, 2006. 43(1): p. 162-4. [ Links ]
[52] GONZALEZ-ZEH, R., R. ARMISEN, and S. BARAHONA, Endovenous laser and echo-guided foam ablation in great saphenous vein reflux: one-year follow-up results. J Vasc Surg, 2008. 48(4): p. 940-6. [ Links ]
[53] DARVALL, K.A., et al., Duplex ultrasound outcomes following ultrasound-guided foam sclerotherapy of symptomatic primary great saphenous varicose veins. Eur J Vasc Endovasc Surg, 2010. 40(4): p. 534-9. [ Links ]
[54] MYERS, K.A., et al., Outcome of ultrasound-guided sclerotherapy for varicose veins: medium-term results assessed by ultrasound surveillance. Eur J Vasc Endovasc Surg, 2007. 33(1): p. 116-21. [ Links ]
[55] THOMASSET, S.C., et al., Ultrasound guided foam sclerotherapy: factors associated with outcomes and complications. Eur J Vasc Endovasc Surg, 2010. 40(3): p. 389-92. [ Links ]
[56] LURIE, F., et al., Prospective randomised study of endovenous radiofrequency obliteration (closure) versus ligation and vein stripping (EVOLVeS): two-year follow-up. Eur J Vasc Endovasc Surg, 2005. 29(1): p. 67-73. [ Links ]
[57] HINCHLIFFE, R.J., et al., A prospective randomised controlled trial of VNUS closure versus surgery for the treatment of recurrent long saphenous varicose veins. Eur J Vasc Endovasc Surg, 2006. 31(2): p. 212-8. [ Links ]
[58] ALMEIDA, J.I., et al., Radiofrequency endovenous ClosureFAST versus laser ablation for the treatment of great saphenous reflux: a multicenter, single-blinded, randomized study (RECOVERY study). J Vasc Interv Radiol, 2009. 20(6): p. 752-9. [ Links ]
[59] GALE, S.S., et al., A randomized, controlled trial of endovenous thermal ablation using the 810-nm wavelength laser and the ClosurePLUS radiofrequency ablation methods for superficial venous insufficiency of the great saphenous vein. J Vasc Surg, 2010. 52(3): p. 645-50. [ Links ]
[60] BOUNTOUROGLOU, D.G., et al., Ultrasound-guided foam sclerotherapy combined with sapheno-femoral ligation compared to surgical treatment of varicose veins: early results of a randomised controlled trial. Eur J Vasc Endovasc Surg, 2006. 31(1): p. 93-100. [ Links ]
[61] KALODIKI, E., et al., Long-term results of a randomized controlled trial on ultrasound-guided foam sclerotherapy combined with saphenofemoral ligation vs standard surgery for varicose veins. J Vasc Surg, 2011. [ Links ]
[62] DE ROOS, K.P., F.H. NIEMAN, and H.A. NEUMANN, Ambulatory phlebectomy versus compression sclerotherapy: results of a randomized controlled trial. Dermatol Surg, 2003. 29(3): p. 221-6. [ Links ]
Al. Prof. Hernâni Monteiro,
4200-319 Porto (Portugal)
917686581














