Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Acta Obstétrica e Ginecológica Portuguesa
versão impressa ISSN 1646-5830
Acta Obstet Ginecol Port vol.10 no.1 Coimbra mar. 2016
ARTIGO DE REVISÃO/REVIEW ARTICLE
Um novo modelo de carcinogénese para cancro do ovário: implicações clínicas da salpingectomia profiláctica
A new model of carcinogenesis for ovarian cancer: clinical implications for prophylactic salpingectomy
Ana Filipa Rodrigues Ferreira*, Maria João Carvalho**, Teresa Rebelo***, Francisco Falcão***, Isabel Torgal****
*Interna da especialidade de Ginecologia e Obstetrícia, Serviço de Ginecologia A - Centro Hospitalar e Universitário de Coimbra; Assistente convidada, Faculdade de Medicina da Universidade de Coimbra
**Assistente hospitalar, Serviço de Ginecologia A - Centro Hospitalar e Universitário de Coimbra; Assistente convidada, Faculdade de Medicina da Universidade de Coimbra;
***Assistente hospitalar Graduado, Serviço de Ginecologia A - Centro Hospitalar e Universitário de Coimbra
****Directora do Serviço de Ginecologia A - Centro Hospitalar e Universitário de Coimbra; Professora Auxiliar, Faculdade de Medicina da Universidade de Coimbra
Endereço para correspondência | Dirección para correspondencia | Correspondence
ABSTRACT
Ovarian cancer is the most lethal gynaecological malignancy. There is limited knowledge regarding this cancer and we are witnessing a paradigm shift, in which the Fallopian tube is considered the primary site of most high-grade serous carcinoma (HGSC). The aim of this article is to review the current body of knowledge of the origin and pathogenesis of ovarian cancer and the clinical implications of the new model of carcinogenesis. During more than 30 years, the prevailing view on the origin of HGSC was that it derived from the ovary, since the ovarian surface epithelium is exposed to inflammation and oxidative stress induced by ovulation. The incessant ovulation hypothesis was proposed by Fathalla in 1971. At the beginning of this century, many studies were published demonstrating the presence of invasive and non-invasive carcinoma in the fallopian tubes of prophylactic salpingo-oophorectomies performed in carriers of BRCA mutation, which led some authors to suggest the fallopian tube as the origin of these tumors. This theory was published in 2007, by Kindelberger, who described the precursor lesion - serous tubal intraepithelial carcinoma (STIC). The advances in cellular and molecular biology and in genetics added support for this new concept, indicating that the HGSC develops from an occult intraephitelial carcinoma in the fimbria of the fallopian tube and involves the ovary secondarily. Observational epidemiologic evidence strongly supports that tubal ligation and hysterectomy are associated with a decrease in the risk of ovarian cancer, by approximately 26-34%. The additional bilateral salpingectomy to hysterectomy does not affect ovarian function, and has no significant differences in rate of complications and operative time. Considering the new insights into the origin of HGSC, in which the majority is of tubal origin, there is a significant preventive potential by performing prophylactic salpingectomy.
Keywords: Carcinogenesis; Ovarian Neoplasms; Salpingectomy.
Introdução
O cancro do ovário é a principal causa de morte por cancro ginecológico e a 5ª causa de morte por cancro, com uma taxa de sobrevivência global aos 5 anos inferior a 45%1. Apesar da introdução de fármacos derivados da platina no tratamento, observou-se uma pequena alteração em relação à sobrevivência de mulheres com cancro do ovário2. Em Portugal, de acordo com o Registo Oncológico Nacional de 2008, a incidência de cancro do ovário foi de 8,9 por 100 mil mulheres3. O cancro epitelial do ovário (CEO) é uma doença heterogénea, constituída por diferentes subtipos histológicos com comportamento biológico e perfil genético diferentes. O subtipo mais comum é o carcinoma seroso de alto grau (CSAG), que representa 60-80% dos tipos histológicos, comum ao carcinoma peritoneal primário e carcinoma da trompa, tendo sido considerados como pertencentes ao mesmo grupo - carcinoma seroso pélvico. É diagnosticado em estádios avançados, 80% das neoplasias são diagnosticadas nos estádios III e IV segundo a classificação da Federação Internacional de Ginecologia e Obstetrícia4.
O conhecimento em relação à sua origem e história natural é limitado, tendo-se assistido a uma alteração do paradigma, no qual a trompa é reconhecida como o local primário de origem deste tumor. O novo modelo de carcinogénese não é apenas uma discussão académica mas poderá ter implicações clínicas importantes em relação à prevenção, rastreio, diagnóstico e tratamento do CEO. A salpingectomia profiláctica no contexto de histerectomia por patologia benigna foi proposta pela primeira vez em 2009, por Shannon Salvador5.
Este artigo tem como objectivo rever os conceitos actuais sobre carcinoma do ovário tendo em consideração a sua origem, patogenia e as implicações clínicas do novo modelo de carcinogénese no que respeita à salpingectomia profiláctica.
Modelo de carcinogénese do carcinoma epitelial do ovário
Origem celular
A origem celular e vias moleculares são elementos necessários para o entendimento em relação à biologia de uma neoplasia maligna.
A composição celular do CEO tem duas particularidades intrigantes: assemelha-se a locais extraováricos, isto é, os tumores seroso, endometrióide e mucinoso apresentam-se morfologicamente idênticos à trompa de Falópio, endométrio e endocolo, respectivamente; a diferenciação celular é superior à do tecido epitelial ovárico normal, ao contrário do que acontece com outros cancros. É igualmente curioso o facto de o CEO apresentar semelhanças morfológicas com o epitélio de origem embriológica das trompas de Falópio, útero e terço superior da vagina - epitélio mülleriano. Estas estruturas desenvolvem-se a partir dos canais de Müller, enquanto o ovário tem origem no epitélio celómico6. Além dos aspectos morfológicos, o CEO expressa HOX genes, que são responsáveis pela diferenciação mülleriana, estando presentes no epitélio das trompas, útero e vagina. Não foi encontrada expressão destes genes no epitélio de superfície normal do ovário7.
Durante mais de 30 anos, foi aceite a hipótese de que o CEO teria origem no epitélio de superfície do ovário (ESO), após um processo de metaplasia mülleriana. Esta teoria foi proposta em 1971, por Fathalla, argumentando que a disrupção cíclica do ESO, exposto a um ambiente inflamatório e stress oxidativo causaria lesão de ADN (ácido desoxirribonucleico), activando mecanismos de reparação e transformação neoplásica e originando quistos de inclusão cortical (QIC). A teoria da ovulação incessante é apoiada pelos dados epidemiológicos, os quais demonstram o efeito protector da contracepção hormonal e paridade no cancro do ovário8. Além disso, Casagrande et al concluíram que a «idade ovulatória», a idade desde a menarca até ao diagnóstico de cancro do ovário ou à menopausa, associada ao efeito protector da contracepção hormonal e da gravidez, está fortemente associada ao risco de cancro do ovário9. No entanto, a presença de quistos de inclusão poderá não estar relacionada com a ovulação uma vez que estes quistos são frequentes na síndrome do ovário poliquístico, dando mais suporte à hipótese das gonadotrofinas, que explica a transformação maligna pela estimulação estrogénica devido à exposição excessiva a gonadotrofinas10. Além da hipótese da ovulação incessante e das gonadotrofinas, foi proposta a hipótese hormonal, defendendo a influência dos androgénios na proliferação do ESO11. Estas teorias não se excluem mutuamente e suportam o papel pró-inflamatório do processo fisiológico da ovulação, potencialmente mutagénico. A utilização de anti-inflamatórios não esteróides está associada a menor risco de CEO. O factor protector da histerectomia e da laqueação tubária poderá ser explicado pela diminuição da exposição a um ambiente inflamatório12. Além disso, foi demonstrado in vitro que fibroblastos senescentes criam um fenótipo pró-inflamatório secundário, promovendo a génese tumoral do ESO13.
A endossalpingiose consiste na presença de epitélio semelhante à mucosa tubária (células colunares ciliadas, células colunares secretoras e células intercaladas) fora das trompas. Os defensores da hipótese da metaplasia celómica explicam a presença deste epitélio nos QIC pelo processo de metaplasia mülleriana do mesotélio celómico, desencadeada pelo estímulo hormonal6. No entanto, Li et al identificaram um fenótipo tubário (PAX8 +/ calretinina -) na maioria dos quistos de inclusão (78%), contrariamente ao fenótipo mesotelial (calretinina +/ PAX8 -) encontrado em quase todo o ESO, o que vem de encontro à sugestão de Dubeau, de que as neoplasias epiteliais do ovário têm origem em células müllerianas. Neste estudo, os autores concluíram, ainda, que existia um aumento progressivo do ratio células secretoras/ciliadas dos quistos de inclusão/cistadenomas para os tumores borderline e carcinoma seroso de baixo grau, sugerindo que os carcinomas serosos de baixo grau representam uma expansão clonal do epitélio secretor, que poderá ser desencadeada por um evento molecular, nomeadamente a aquisição de mutações no KRAS e BRAF14. Esselen et al compararam a expressão de vários biomarcadores em endossalpingiose, epitélio tubário normal e ESO, obtendo resultados semelhantes ao estudo de Li et al, com forte expressão imunohistoquímica do PAX8 nos dois primeiros epitélios e expressão fraca no ESO. Além disso, a maioria das proteínas expressas na endossalpingiose foi igualmente expressa em tumores serosos borderline e malignos15. Auersperg sugeriu uma hipótese unificadora da origem celular, na junção interepitelial, incluindo o mesotélio de superfície do ovário e o epitélio das fimbrias, argumentando a origem embrionária comum do epitélio celómico que torna esta zona de transição propensa a transformação maligna, tendo em conta um menor grau de diferenciação16. A origem mülleriana da endossalpingiose pode ser explicada pela proximidade anatómica do epitélio das fimbrias ao ovário, com implantação directa, possivelmente facilitada pela ovulação, inflamação e formação de aderências. Estes implantes formam QIC após um processo de invaginação e podem, posteriormente, sofrer transformação maligna. No entanto, a origem no epitélio das fimbrias não permite explicar todos os diagnósticos de carcinoma do ovário, mesmo os com diferenciação serosa, uma vez que muitos se desenvolvem a partir de estruturas quísticas em que não há homologia com os componentes das fimbrias. Além disso, portadoras de mutação dos genes BRCA1/ /BRCA2 submetidas a salpingo-ooforectomia profiláctica mantêm o risco de carcinoma seroso peritoneal. A explicação para estes dois pontos poderá ser a existência de epitélio mülleriano extrauterino, que inclui endossalpingiose, endometriose e endocervicose, dando origem ao carcinoma seroso, carcinoma endometrióide/células claras e carcinoma mucinoso, respectivamente. Esta hipótese explica a presença de QIC, cistadenomas paraováricos e paratubários, assim como o carcinoma peritoneal primário, tendo em conta que os componentes do epitélio mülleriano extrauterino podem estar afastados do ovário e trompas. Embora apelativo, este conceito necessita de maior evidência em estudos experimentais6,17.
Existem alguns cancros que têm origem em zonas de transição entre dois tipos de epitélio, como a junção gastroesofágica e podem originar-se de células multipotentes. A junção do mesotélio peritoneal e epitélio tubário foi proposta como um potencial local de carcinogénese após a identificação de metaplasia e hiperplasia mesotelial em 20% e 17%, respectivamente, de 228 trompas de 182 mulheres submetidas a salpingo-ooforectomia por diversas indicações18. Outra hipótese para a origem celular do CEO inclui o nicho de stem cell presentes no ESO que poderá ser responsável pela reparação tecidular após a ovulação. Estas células foram identificadas na região do hilum de ovários de modelos in vivo que utilizam ratos, na transição entre o mesotélio e o epitélio tubário, e apresentaram aumento do potencial de transformação após inactivação dos genes supressores tumorais p53 e Rb119.
Precursores putativos
A compreensão em relação à carcinogénese de uma determinada neoplasia inclui a identificação de lesões precursoras, como a neoplasia intraepitelial cervical no cancro do colo do útero e as alterações displásicas da mucosa no cancro colo-rectal. No entanto, até à data, ainda não foram identificadas no ovário lesões precursoras do CEO.
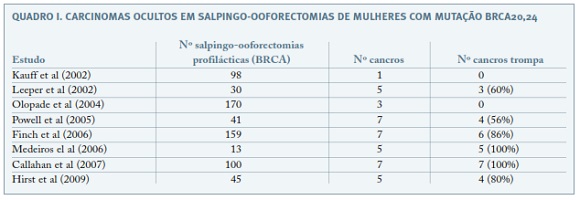
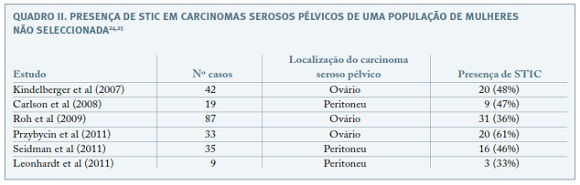
No início deste século, foram publicados vários trabalhos com análise detalhada das trompas de mulheres com mutação dos genes BRCA1/BRCA2 submetidas a salpingo-ooforectomias profilácticas (Quadro I). A análise sistematizada destas trompas por um protocolo publicado em 2006, o SEE-FIM (Sectioning and Extensively Examining the FIMbriated End of the Fallopian Tube), permitiu constatar uma frequência desproporcionalmente elevada de cancros na trompa em relação ao ovário, estando presentes carcinoma invasivo e não invasivo nas trompas, na ausência de carcinoma do ovário. Este achado conduziu alguns autores a sugerir a trompa como o local de origem dos tumores do ovário20-23. A hipótese tubária é publicada em 2007, por Kindelberger, que introduz o conceito de STIC (serous tubal intraepithelial carcinoma) como lesão precursora, após demonstrar que dos 42 carcinomas classificados como serosos primários do ovário, 20 (48%) tinham carcinoma intraepitelial tubário. Esta análise foi realizada em carcinomas serosos pélvicos de mulheres não classificadas como de alto risco para cancro do ovário e foram seguidamente publicados mais trabalhos com resultados semelhantes24-26 (Quadro II).
Após a introdução deste conceito aumentou consideravelmente o interesse na avaliação da trompa, através de estudos histológicos, moleculares e genéticos. As STIC caracterizam-se pela presença de epitélio estratificado, atipias nucleares, ausência de polaridade nuclear, pleomorfismo e ausência de células ciliadas. Apresentam um elevado índice proliferativo (Ki 67 >40%) e a expressão imunohistoquímica da p53 é intensa e difusa (80-92%). O nível elevado de γH2AX, marcador de quebras na cadeia dupla de ADN, indica uma instabilidade genética27. Kuhn et al identificaram mutações idênticas da p53 em 27 STIC dos 29 casos de CSAG diagnosticados, compatíveis com crescimento clonal. Foram identificadas mutações missense em 61% e mutações frameshift/splicing junction/nonsense em 39%28. Um grupo de investigadores propôs uma alteração como sendo a mais precoce na sequência de eventos que levam à formação das STIC, que corresponde à expansão das células secretoras - SCOUT. Estas células estão presentes nas regiões proximal e distal da trompa e apresentam subexpressão do PAX2, alteração igualmente identificada em carcinomas da trompa29. A realização de imunohistoquímica para a p53 em trompas de mulheres com mutação BRCA permitiu a identificação de células aparentemente normais mas com sobreexpressão da p53. Estas células foram denominadas p53 signatures e foram encontradas sobretudo na região distal da trompa, em células secretoras e com evidência de lesão de ADN30. Assim, foi proposta uma sequência de carcinogénese para o CSAG, que se inicia com lesões SCOUT, provavelmente em lesões benignas, que proliferam e expressam p53 (p53 signatures), progredindo para lesões STIC e culminando no carcinoma invasivo4,24,31,32.
Além das STIC, foi definida uma lesão tubária que consiste na proliferação de células epiteliais que formam aglomerados com padrão papilar e geralmente associadas a corpos psamomatosos - papillary tubal hyperplasia (PTH). Kurman et al sugerem a PTH como lesão precursora dos tumores serosos de baixo grau, envolvendo locais ováricos ou extraováricos (atypical proliferative serous tumors, implantes epiteliais não invasivos e endossalpingiose)33. Mais recentemente, Vang, Shih e Kurman sugeriram que todos os carcinomas serosos do ovário, de baixo e alto grau, poderão ter origem tubária, tendo como lesões precursoras as PTH e as STIC, respectivamente34.
Classificação clínico-patogénica
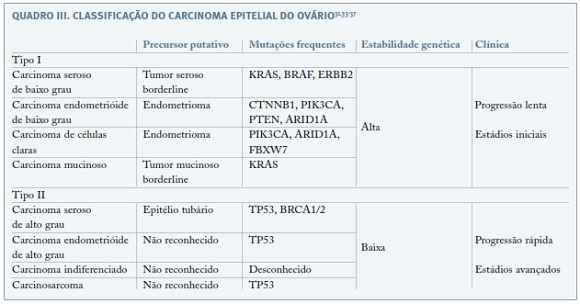
Consideram-se duas vias moleculares distintas para o carcinoma do ovário. A primeira caracteriza-se por um processo de transformação maligna gradual, incluindo um espectro tumoral de lesões benignas a malignas, cuja lesão precursora no ovário é conhecida e geralmente apresenta-se confinada ao ovário na altura do diagnóstico. A segunda é caracterizada por um desenvolvimento tumoral rápido e comportamento agressivo, geralmente diagnosticada em estádios avançados. Com base nas características clínicas, histopatológicas, moleculares e genéticas, o CEO foi classificado por Kurman et al segundo um modelo dualístico, em tumores Tipo I e Tipo II (Quadro III). Este modelo permite explicar a incapacidade da ecografia endovaginal no rastreio e detecção precoce (estádio I) do carcinoma do ovário. A ecografia endovaginal iria selectivamente identificar os tumores Tipo I que, pelo seu crescimento lento, podem ser diagnosticados numa fase precoce. No entanto, a maioria dos tumores são do Tipo II, pelo que este método de rastreio a larga escala seria ineficaz. Por outro lado, ainda não é conhecida uma lesão precursora ovárica cuja detecção precoce permitisse adoptar medidas preventivas e interventivas35-37.
Novo Paradigma
A teoria mais duradoura e universalmente aceite para a origem do CEO, apoiada por dados epidemiológicos, assenta numa origem ovárica, no ESO. A teoria emergente defende que o epitélio tubário das fimbrias está exposto a um stress oxidativo devido ao microambiente inflamatório do processo ovulatório (fluido folicular), promovendo a selecção de células com mutação na p53 e originando STIC que se desprendem e se implantam no ovário ou no peritoneu38. Dados epidemiológicos mais recentes reportam uma relação inversa entre a presença de lesões precursoras tubárias e a utilização de contracepção oral e paridade39.
Após a sugestão de uma origem tubária para o CSAG, a investigação crescente, nomeadamente através de métodos moleculares e genéticos, assim como o desenvolvimento de modelos experimentais, tem permitido suportar esta hipótese. Actualmente, consideram-se as seguintes linhas que fundamentam a hipótese tubária: a) presença de STIC em ≥ 50% dos casos de CSAG; b) presença de mutações TP53 idênticas nas STIC e no carcinoma do ovário, indiciando uma proliferação clonal; c) presença de STIC em salpingectomias profilácticas na ausência de carcinoma do ovário; d) aumento da expressão de oncogenes nas STIC (cyclin E1, RSf-1, fatty acid synthase) que têm sobreexpressão no CSAG; e) presença de telómeros mais curtos nas STIC associadas a CSAG do que nos CSAG; f) perfis de expressão génica e imunohistoquímica do CSAG assemelham-se mais com o epitélio das trompas (mülleriano) do que com o de superfície do ovário (mesotelial)4,24,34,40.
Levanon et al desenvolveram um sistema de cultura de células epiteliais das trompas para estudar a susceptibilidade destas células à transformação neoplásica, tendo concluído que as células secretoras apresentavam maior susceptibilidade à lesão de ADN após radiação ionizante do que as células ciliadas41. Karst et al desenvolveram um modelo com xenotransplantes em que demonstraram a transformação das células secretoras tubárias humanas em tumores müllerianos de alto grau42. Kim et al desenvolveram um modelo experimental com ratos knockout com inactivação dos genes DICER e PTEN, demonstrando o desenvolvimento e progressão para ovário e peritoneu do CSAG com origem na trompa. Estas neoplasias revelaram semelhanças moleculares com o CSAG em humanos. Além disso, a remoção das trompas preveniu o aparecimento de cancro, enquanto a ooforectomia não teve influência43.
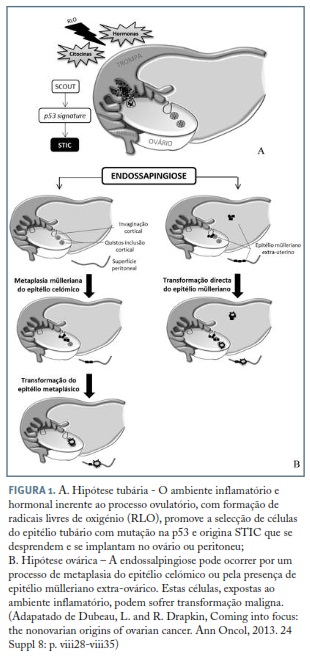
A associação entre o epitélio tubário e o CSAG parece estar bem estabelecida e aceite no meio científico. A dúvida permanece em relação à consistência desta associação. A ausência de STIC em alguns CSAG levou vários autores a sugerir que, além da hipótese tubária, os CSAG poderiam ter origem ovárica. Ainda assim, a origem poderá ser directamente no ESO, ocorrendo formação de QIC com metaplasia mülleriana, sob influência do estroma ovárico, ou pode ter uma origem extraovárica, através de implantação directa de epitélio mülleriano ou através do epitélio mülleriano extrauterino40,44,45. Nem a hipótese do epitélio mülleriano extrauterino foi definitivamente estabelecida, nem a metaplasia mülleriana foi inequivocamente provada. No entanto, vários autores consideram pouco provável a transformação de um epitélio mesotelial simples num epitélio mülleriano altamente diferenciado46. Outra questão importante consiste em entender porque motivo um tumor proveniente da trompa se vai desenvolver maioritariamente no ovário. Alguns autores especulam que o ambiente hormonal do estroma ovárico poderá ser um estímulo à proliferação epitelial do carcinoma40. As hipóteses tubária e ovárica estão esquematizadas na Figura 1.
Implicações clínicas
Rastreio/Diagnóstico precoce
Não existe, actualmente, nenhum método de rastreio eficaz para o carcinoma do ovário. Os resultados de 3 grandes estudos randomizados são desanimadores. Um estudo multicêntrico realizado nos Estados Unidos - Prostate, Lung, Colorectal and Ovarian Cancer Screening (PLCO) comparou a utilização da ecografia endovaginal e doseamento do CA 125 com a vigilância habitual, tendo concluído não existir diminuição da mortalidade por cancro do ovário no grupo de intervenção47. O estudo Japonês utilizou este mesmo método de rastreio no grupo de intervenção e concluiu que o número de carcinomas diagnosticados em estádios precoces não foi diferente48. O United Kingdom Collaborative Trial of Ovarian Cancer Screening (UKCTOCS) concluiu existir benefício na triagem de doentes com valores de CA 125 elevados seguida da realização de ecografia endovaginal. No entanto, não obtiveram resultados que demonstrassem diminuição da mortalidade49. Estes resultados são concordantes com as conclusões de Brown e Palmer: para atingir uma sensibilidade de 50% na detecção de tumores antes do estádio III seria necessário que a ecografia anual permitisse a detecção de tumores com 1,3 cm de diâmetro. No modelo desenvolvido por estes autores, há uma «janela de oportunidade» de mais de 4 anos para o diagnóstico de STIC e estádios I e II do CSAG, enquanto os estádios III e IV duram cerca de 1 ano até se tornarem clinicamente evidentes50. Além disso, apenas 25-50% dos tumores em estádio I apresentam elevações do CA 125, marcador que poderá também estar elevado noutras condições, como a menstruação, a endometriose ou a doença hepática, entre outras51. A detecção precoce destes tumores poderá passar pela utilização de biomarcadores ainda não identificados. Kinde et al utilizou a citologia cervical com o objectivo de identificar mutações somáticas presentes nos tumores do endométrio e ovário, tendo obtido resultados promissores em relação ao endométrio. No entanto, menos de metade das mutações do ovário foi detectada52. A citologia do lavado peritoneal detectou a presença de implantes peritoneais com acuidade moderada53.
Estratégia cirúrgica
Uma meta-análise realizada por Cibula et al estudou o risco de CEO em mulheres submetidas a laqueação tubária, tendo confirmado uma redução do risco de 34%, sendo a redução mais evidente para o carcinoma endometrióide (RR=0,40) seguido do carcinoma seroso (RR=0,73). Não houve redução significativa para o carcinoma mucinoso54. Outra meta-análise obteve resultados semelhantes em relação à laqueação tubária e analisou ainda a redução do risco de CEO após histerectomia, confirmando uma redução de 26%55. Existem alguns mecanismos para explicar estas conclusões, sendo o mais consistente a prevenção da progressão ascendente de células endometriais e células epiteliais da trompa proximal, assim como de factores pró-inflamatórios, compatível com o facto da redução do risco ser observada nos tipos histológicos endometrióide e seroso, que poderão ter origem no endométrio e trompa, respectivamente56.
Salpingectomia profiláctica diminui o cancro do ovário?
Não existem, actualmente, estudos que evidenciem esta relação. Foi realizado um estudo retrospectivo num hospital universitário da Alemanha, com mulheres na pré-menopausa (40-55 anos) submetidas a LAVH (laparoscopically assisted vaginal hysterectomy) por patologia benigna com e sem remoção das trompas, entre 2001 e 2007. O follow-up foi realizado por um questionário e durou cerca de 7 anos. O estudo concluiu existir uma redução significativa da patologia anexial benigna no grupo submetido a salpingectomia. No entanto, não houve casos de patologia maligna em nenhum dos grupos57. Lessard-Anderson et al apresentaram no encontro anual da Sociedade de Ginecologia Oncológica em 2013 um estudo que demonstrou um menor risco de desenvolver CEO e peritoneal primário em mulheres submetidas a salpingectomia como método de contracepção definitiva (OR=0,36)58.
Salpingectomia profiláctica tem mais riscos?
Alguns autores argumentam que a salpingectomia apresenta risco iatrogénico de alteração da função ovárica por alteração da vascularização e inervação das estruturas anexiais57,59. Estudos publicados concluíram não existir diferença na resposta ovárica a gonadotrofinas60,61 nem nos níveis de hormona anti-mülleriana (HAM)62,63. Morelli et al demonstraram não existir alteração da função ovárica através da análise de diferentes parâmetros, incluindo a HAM, a FSH (do inglês, follicle stimulating hormone), a contagem de folículos antrais, o diâmetro médio dos ovários e o pico de velocidade sistólica dos vasos ováricos. Além disso, como resultado secundário, o estudo realizado por estes autores concluiu não existir diferenças entre os grupos que realizaram histerectomia com ou sem salpingectomia em relação ao tempo operatório, variação do valor de hemoglobina, permanência hospitalar, regresso à actividade habitual e taxa de complicações63. Entretanto, não há ainda estudos a revelar o potencial efeito da salpingectomia na idade da menopausa. Alguns autores, com este argumento, não recomendam a realização de salpingectomia profiláctica fora do contexto da investigação clínica64.
Que estratégia adoptar?
A maioria dos autores recomenda a realização de salpingectomia profiláctica no contexto de contracepção definitiva ou histerectomia por patologia benigna24,45,46,51,65-67 e alguns consideram, ainda, no contexto de cirurgia abdominal não ginecológica21,65. Tone et al acreditam que a salpingectomia profiláctica irá reduzir o número de CSAG em cerca de 30% nas próximas duas décadas51. Num estudo publicado recentemente foram identificados 4 casos de STIC após análise completa e sistematizada das trompas de 522 mulheres submetidas a cirurgia por patologia benigna. Foi realizada pesquisa de mutação hereditária BRCA1/BRCA2 nas 4 mulheres, não tendo sido identificada em nenhuma. Dos 4 casos, 3 não teriam sido identificados pelo método standard de examinação da trompa, motivo pelo qual os autores recomendam uma exame detalhado, mesmo nas mulheres de baixo risco para cancro do ovário68.
Uma outra questão que se coloca, ainda sem consenso, é a realização de quimioterapia adjuvante em casos em que foram encontradas STIC, uma vez que o lavado peritoneal pode ser positivo nalgumas destas situações69,70 indicando disseminação de células malignas. Foram descritos casos de mulheres que desenvolveram cancro peritoneal 2 anos após a cirurgia51.
A opinião de clínicos em relação à prática cirúrgica da salpingectomia foi abordada em 2 estudos, através de um questionário. No estudo Irlandês, apesar da reduzida frequência com que os clínicos realizam este procedimento no contexto de contracepção (3,9%) e histerectomia (26%), mais de 70% ponderar começar a realizar71. Nos Estados Unidos, cerca de metade dos clínicos inquiridos realizam salpingectomia no contexto de histerectomia e fazem-no sobretudo (75%) por acreditarem que diminui o risco de cancro, embora os restantes argumentem contra este procedimento por considerarem não existir benefício, além de aumentar o tempo operatório e o risco de complicações72.
O Ovarian Cancer Research Program (OvCaRe) British Columbia lançou em Setembro de 2010 uma campanha educacional dirigida aos clínicos do Canadá. Este projecto recomenda que os clínicos informem as doentes dos benefícios e riscos da salpingectomia, oferecendo a possibilidade de realização deste procedimento, e é apoiado pela Sociedade de Ginecologia Oncológica do Canadá73. Por fim, a Sociedade Portuguesa de Ginecologia recomenda a remoção das trompas no contexto de histerectomia em que se equacione a preservação ovárica74.
Conclusões
O paradigma da carcinogénese do carcinoma do ovário sofreu uma alteração, acreditando-se que a maioria dos CSAG tem origem na trompa, onde são reconhecidas as suas lesões precursoras, as STIC. Actualmente não existem estudos que evidenciem que a salpingectomia profiláctica diminua o risco de CSAG, embora haja evidência da ausência de riscos deste procedimento. Serão necessários alguns anos para avaliar o impacto da remoção das trompas na incidência e mortalidade do cancro do ovário.
Embora não se qualifique exactamente como método de prevenção secundária, o potencial de remoção de uma lesão pré-maligna ao realizar salpingectomia é provável à luz dos novos conhecimentos da carcinogénese do ovário. Considerando não parecer existir um propósito biológico da trompa em mulheres que não desejam ter mais filhos e a ausência de riscos na sua remoção, a realização de salpingectomia em mulheres submetidas a histerectomia por patologia benigna ou que desejem contracepção definitiva parece ser uma opção estratégica lógica para diminuir o número de casos de carcinoma epitelial do ovário.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Siegel R, Ma J, Zou Z, Jemal A. Cancer statistics, 2014. CA Cancer J Clin 2014;64:9-29. [ Links ]
2. Vaughan S, Coward JI, Bast RC, Jr., Berchuck A, Berek JS, Brenton JD et al. Rethinking ovarian cancer: recommendations for improving outcomes. Nat Rev Cancer 2011;11:719-725. [ Links ]
3. RORCentro. Registo Oncológico Nacional 2008. Instituto Português de Oncologia de Coimbra Francisco Gentil - EPE, 2014. ROR-Centro. 2014. at http://www.rorcentro.com.pt/
4. Nik NN, Vang R, Shih Ie M, Kurman RJ. Origin and pathogenesis of pelvic (ovarian, tubal, and primary peritoneal) serous carcinoma. Annu Rev Pathol 2014;9:27-45. [ Links ]
5. Salvador S, Gilks B, Kobel M, Huntsman D, Rosen B, Miller D. The fallopian tube: primary site of most pelvic high-grade serous carcinomas. Int J Gynecol Cancer 2009;19:58-64. [ Links ]
6. Dubeau L. The cell of origin of ovarian epithelial tumours. Lancet Oncol 2008;9:1191-1197. [ Links ]
7. Cheng W, Liu J, Yoshida H, Rosen D, Naora H. Lineage infidelity of epithelial ovarian cancers is controlled by HOX genes that specify regional identity in the reproductive tract. Nat Med 2005;11:531-537. [ Links ]
8. Fathalla MF. Incessant ovulation and ovarian cancer - a hypothesis re-visited. Facts Views Vis Obgyn 2013;5:292-297. [ Links ]
9. Casagrande JT, Louie EW, Pike MC, Roy S, Ross RK, Henderson BE. «Incessant ovulation» and ovarian cancer. Lancet 1979;2:170-173. [ Links ]
10. Fleming JS, Beaugie CR, Haviv I, Chenevix-Trench G, Tan OL. Incessant ovulation, inflammation and epithelial ovarian carcinogenesis: revisiting old hypotheses. Mol Cell Endocrinol 2006;247:4-21. [ Links ]
11. Saad AF, Hu W, Sood AK. Microenvironment and pathogenesis of epithelial ovarian cancer. Horm Cancer 2010;1:277-290. [ Links ]
12. Haruta S, Furukawa N, Yoshizawa Y, Tsunemi T, Nagai A, Kawaguchi R et al. Molecular genetics and epidemiology of epithelial ovarian cancer (Review). Oncol Rep 2011;26:1347-1356. [ Links ]
13. Shan W, Liu J. Inflammation: a hidden path to breaking the spell of ovarian cancer. Cell Cycle 2009;8:3107-3111. [ Links ]
14. Li J, Abushahin N, Pang S, Xiang L, Chambers SK, Fadare O et al. Tubal origin of ‘ovarian’ low-grade serous carcinoma. Mod Pathol 2011;24:1488-1499. [ Links ]
15. Esselen KM, Ng SK, Hua Y, White M, Jimenez CA, Welch WR et al. Endosalpingiosis as it relates to tubal, ovarian and serous neoplastic tissues: an immunohistochemical study of tubal and Mullerian antigens. Gynecol Oncol 2014;132:316-321. [ Links ]
16. Auersperg N. The origin of ovarian carcinomas: a unifying hypothesis. Int J Gynecol Pathol 2011;30:12-21. [ Links ]
17. Dubeau L, Drapkin R. Coming into focus: the nonovarian origins of ovarian cancer. Ann Oncol 2013;24 Suppl 8:viii28-viii35. [ Links ]
18. Seidman JD, Yemelyanova A, Zaino RJ, Kurman RJ. The fallopian tube-peritoneal junction: a potential site of carcinogenesis. Int J Gynecol Pathol 2011;30:4-11. [ Links ]
19. Flesken-Nikitin A, Hwang CI, Cheng CY, Michurina TV, Enikolopov G, Nikitin AY. Ovarian surface epithelium at the junction area contains a cancer-prone stem cell niche. Nature 2013;495: 241-245. [ Links ]
20. Crum CP, Drapkin R, Kindelberger D, Medeiros F, Miron A, Lee Y. Lessons from BRCA: the tubal fimbria emerges as an origin for pelvic serous cancer. Clin Med Res 2007;5:35-44. [ Links ]
21. Dietl J, Wischhusen J, Hausler SF. The post-reproductive Fallopian tube: better removed? Hum Reprod 2011;26:2918-2924. [ Links ]
22. Piek JM, van Diest PJ, Zweemer RP, Jansen JW, Poort-Keesom RJ, Menko FH, Gille JJ, Jongsma AP, Pals G, Kenemans P, Verheijen RH. Dysplastic changes in prophylactically removed Fallopian tubes of women predisposed to developing ovarian cancer. J Pathol 2001;195:451-456. [ Links ]
23. Piek JM, Verheijen RH, Kenemans P, Massuger LF, Bulten H, van Diest PJ. BRCA1/2-related ovarian cancers are of tubal origin: a hypothesis. Gynecol Oncol 2003;90:491. [ Links ]
24. Chene G, Rahimi K, Mes-Masson AM, Provencher D. Surgical implications of the potential new tubal pathway for ovarian carcinogenesis. J Minim Invasive Gynecol 2013;20:153-159. [ Links ]
25. Kindelberger DW, Lee Y, Miron A, Hirsch MS, Feltmate C, Medeiros F et al. Intraepithelial carcinoma of the fimbria and pelvic serous carcinoma: Evidence for a causal relationship. Am J Surg Pathol 2007;31:161-169. [ Links ]
26. Przybycin CG, Kurman RJ, Ronnett BM, Shih Ie M, Vang R. Are all pelvic (nonuterine) serous carcinomas of tubal origin? Am J Surg Pathol 2010;34:1407-1416. [ Links ]
27. Mehrad M, Ning G, Chen EY, Mehra KK, Crum CP. A pathologist’s road map to benign, precancerous, and malignant intraepithelial proliferations in the fallopian tube. Adv Anat Pathol 2010;17:293-302. [ Links ]
28. Kuhn E, Kurman RJ, Vang R, Sehdev AS, Han G, Soslow R et al. TP53 mutations in serous tubal intraepithelial carcinoma and concurrent pelvic high-grade serous carcinoma-evidence supporting the clonal relationship of the two lesions. J Pathol 2012;226:421-426. [ Links ]
29. Chen EY, Mehra K, Mehrad M, Ning G, Miron A, Mutter GL et al. Secretory cell outgrowth, PAX2 and serous carcinogenesis in the Fallopian tube. J Pathol 2010;222:110-116. [ Links ]
30. Lee Y, Miron A, Drapkin R, Nucci MR, Medeiros F, Saleemuddin A, Garber J, Birch C, Mou H, Gordon RW, Cramer DW, McKeon FD, Crum CP. A candidate precursor to serous carcinoma that originates in the distal fallopian tube. J Pathol 2007;211:26-35. [ Links ]
31. Li HX, Lu ZH, Shen K, Cheng WJ, Malpica A, Zhang J et al. Advances in serous tubal intraepithelial carcinoma: correlation with high grade serous carcinoma and ovarian carcinogenesis. Int J Clin Exp Pathol 2014;7:848-857. [ Links ]
32. Chene G, Dauplat J, Radosevic-Robin N, Cayre A, Penault-Llorca F. Tu-be or not tu-be: that is the question... about serous ovarian carcinogenesis. Crit Rev Oncol Hematol 2013;88:134-143. [ Links ]
33. Kurman RJ, Vang R, Junge J, Hannibal CG, Kjaer SK, Shih Ie M. Papillary tubal hyperplasia: the putative precursor of ovarian atypical proliferative (borderline) serous tumors, noninvasive implants, and endosalpingiosis. Am J Surg Pathol 2011;35:1605-1614. [ Links ]
34. Vang R, Shih Ie M, Kurman RJ. Fallopian tube precursors of ovarian low- and high-grade serous neoplasms. Histopathology 2013;62:44-58. [ Links ]
35. Kurman RJ, Visvanathan K, Roden R, Wu TC, Shih Ie M. Early detection and treatment of ovarian cancer: shifting from early stage to minimal volume of disease based on a new model of carcinogenesis. Am J Obstet Gynecol 2008;198:351-356. [ Links ]
36. Kurman RJ, Shih Ie M. Molecular pathogenesis and extraovarian origin of epithelial ovarian cancer—shifting the paradigm. Hum Pathol 2011;42:918-931. [ Links ]
37. Koshiyama M, Matsumura N. Recent concepts of ovarian carcinogenesis: type I and type II. 2014;2014:934261. [ Links ]
38. Crum CP, Drapkin R, Miron A, Ince TA, Muto M, Kindelberger DW et al. The distal fallopian tube: a new model for pelvic serous carcinogenesis. Curr Opin Obstet Gynecol 2007;19:3-9. [ Links ]
39. Reade CJ, McVey RM, Tone AA, Finlayson SJ, McAlpine JN, Fung-Kee-Fung M et al. The fallopian tube as the origin of high grade serous ovarian cancer: review of a paradigm shift. J Obstet Gynaecol Can 2014;36:133-140. [ Links ]
40. Kurman RJ. Origin and molecular pathogenesis of ovarian high-grade serous carcinoma. Ann Oncol 2013;24 Suppl 10:x16-21. [ Links ]
41. Levanon K, Ng V, Piao HY, Zhang Y, Chang MC, Roh MH et al. Primary ex vivo cultures of human fallopian tube epithelium as a model for serous ovarian carcinogenesis. Oncogene 2010;29: 1103-113. [ Links ]
42. Karst AM, Levanon K, Drapkin R. Modeling high-grade serous ovarian carcinogenesis from the fallopian tube. Proc Natl Acad Sci U S A 2011;108:7547-7552. [ Links ]
43. Kim J, Coffey DM, Creighton CJ, Yu Z, Hawkins SM, Matzuk MM. High-grade serous ovarian cancer arises from fallopian tube in a mouse model. Proc Natl Acad Sci U S A 2012;109:3921-3926. [ Links ]
44. Crum CP, Herfs M, Ning G, Bijron JG, Howitt BE, Jimenez CA et al. Through the glass darkly: intraepithelial neoplasia, top-down differentiation, and the road to ovarian cancer. J Pathol 2013;231:402-412. [ Links ]
45. Erickson BK, Conner MG, Landen CN, Jr. The role of the fallopian tube in the origin of ovarian cancer. Am J Obstet Gynecol 2013;209:409-414. [ Links ]
46. Dietl J. Revisiting the pathogenesis of ovarian cancer: the central role of the fallopian tube. Arch Gynecol Obstet 2014;289: 241-246. [ Links ]
47. Buys SS, Partridge E, Black A, Johnson CC, Lamerato L, Isaacs C et al. Effect of screening on ovarian cancer mortality: the Prostate, Lung, Colorectal and Ovarian (PLCO) Cancer Screening Randomized Controlled Trial. JAMA 2011;305:2295-2303. [ Links ]
48. Kobayashi H, Yamada Y, Sado T, Sakata M, Yoshida S, Kawaguchi R, Kanayama S, Shigetomi H, Haruta S, Tsuji Y, Ueda S, Kitanaka T. A randomized study of screening for ovarian cancer: a multicenter study in Japan. Int J Gynecol Cancer 2008;18:414-420. [ Links ]
49. Menon U, Gentry-Maharaj A, Hallett R, Ryan A, Burnell M, Sharma A, Lewis S, Davies S, Philpott S, Lopes A, Godfrey K, Oram D, Herod J, Williamson K, Seif MW, Scott I, Mould T, Woolas R, Murdoch J, Dobbs S, Amso NN, Leeson S, Cruickshank D, McGuire A, Campbell S, Fallowfield L, Singh N, Dawnay A, Skates SJ, Parmar M, Jacobs I. Sensitivity and specificity of multimodal and ultrasound screening for ovarian cancer, and stage distribution of detected cancers: results of the prevalence screen of the UK Collaborative Trial of Ovarian Cancer Screening (UKCTOCS). Lancet Oncol 2009;10:327-340. [ Links ]
50. Brown PO, Palmer C. The preclinical natural history of serous ovarian cancer: defining the target for early detection. PLoS Med 2009;6:e1000114. [ Links ]
51. Tone AA, Salvador S, Finlayson SJ, Tinker AV, Kwon JS, Lee CH et al. The role of the fallopian tube in ovarian cancer. Clin Adv Hematol Oncol 2012;10:296-306. [ Links ]
52. Kinde I, Bettegowda C, Wang Y, Wu J, Agrawal N, Shih Ie M et al. Evaluation of DNA from the Papanicolaou test to detect ovarian and endometrial cancers. Sci Transl Med 2013;5:167ra4.
53. Sneige N, Thomison JB, Malpica A, Gong Y, Ensor J, Silva EG. Peritoneal washing cytologic analysis of ovarian serous tumors of low malignant potential to detect peritoneal implants and predict clinical outcome. Cancer Cytopathol 2012;120:238-244. [ Links ]
54. Cibula D, Widschwendter M, Majek O, Dusek L. Tubal ligation and the risk of ovarian cancer: review and meta-analysis. Hum Reprod Update 2011;17:55-67. [ Links ]
55. Rice MS, Murphy MA, Tworoger SS. Tubal ligation, hysterectomy and ovarian cancer: A meta-analysis. J Ovarian Res 2012; 5:13. [ Links ]
56. Cibula D, Widschwendter M, Zikan M, Dusek L. Underlying mechanisms of ovarian cancer risk reduction after tubal ligation. Acta Obstet Gynecol Scand 2011;90:559-563. [ Links ]
57. Vorwergk J, Radosa MP, Nicolaus K, Baus N, Jimenez Cruz J, Rengsberger M et al. Prophylactic bilateral salpingectomy (PBS) to reduce ovarian cancer risk incorporated in standard premenopausal hysterectomy: complications and re-operation rate. J Cancer Res Clin Oncol 2014;140: 859-865. [ Links ]
58. Lessard-Anderson CR, Handlogten KS, Molitor RJ, Dowdy SC, Cliby WA, Weaver AL et al. Effect of Tubal Sterilization Technique on Risk of Serous Ovarian and Primary Peritoneal Carcinoma. Gynecol Oncol 2014. [ Links ]
59. Chan CC, Ng EH, Li CF, Ho PC. Impaired ovarian blood flow and reduced antral follicle count following laparoscopic salpingectomy for ectopic pregnancy. Hum Reprod 2003;18:2175-2180. [ Links ]
60. Strandell A, Lindhard A, Waldenstrom U, Thorburn J. Prophylactic salpingectomy does not impair the ovarian response in IVF treatment. Hum Reprod 2001;16:1135-1139. [ Links ]
61. Dar P, Sachs GS, Strassburger D, Bukovsky I, Arieli S. Ovarian function before and after salpingectomy in artificial reproductive technology patients. Hum Reprod 2000;15:142-144. [ Links ]
62. Findley AD, Siedhoff MT, Hobbs KA, Steege JF, Carey ET, McCall CA et al. Short-term effects of salpingectomy during laparoscopic hysterectomy on ovarian reserve: a pilot randomized controlled trial. Fertil Steril 2013;100:1704-1708. [ Links ]
63. Morelli M, Venturella R, Mocciaro R, Di Cello A, Rania E, Lico D, D’Alessandro P et al. Prophylactic salpingectomy in premenopausal low-risk women for ovarian cancer: primum non nocere. Gynecol Oncol 2013;129:448-451. [ Links ]
64. Tanner EJ, Long KC, Visvanathan K, Fader AN. Prophylactic salpingectomy in premenopausal women at low risk for ovarian cancer: risk-reducing or risky? Fertil Steril 2013;100:1530-1531. [ Links ]
65. Gilks CB, Miller D. Opportunistic salpingectomy for women at low risk for development of ovarian carcinoma: the time has come. Gynecol Oncol 2013;129:443-444. [ Links ]
66. Dwyer PL. Ovarian cancer and the pelvic floor surgeon: the case for prophylactic bilateral salpingectomy during POP surgery. Int Urogynecol J 2012;23:655-656. [ Links ]
67. Anderson CK, Wallace S, Guiahi M, Sheeder J, Behbakht K, Spillman MA. Risk-reducing salpingectomy as preventative strategy for pelvic serous cancer. Int J Gynecol Cancer 2013;23:417-421. [ Links ]
68. Rabban JT, Garg K, Crawford B, Chen LM, Zaloudek CJ. Early detection of high-grade tubal serous carcinoma in women at low risk for hereditary breast and ovarian cancer syndrome by systematic examination of fallopian tubes incidentally removed during benign surgery. Am J Surg Pathol 2014;38:729-742. [ Links ]
69. Colgan TJ, Boerner SL, Murphy J, Cole DE, Narod S, Rosen B. Peritoneal lavage cytology: an assessment of its value during prophylactic oophorectomy. Gynecol Oncol 2002;85:397-403. [ Links ]
70. Manchanda R, Drapkin R, Jacobs I, Menon U. The role of peritoneal cytology at risk-reducing salpingo-oophorectomy (RRSO) in women at increased risk of familial ovarian/tubal cancer. Gynecol Oncol 2012;124:185-191. [ Links ]
71. Kamran MW, Vaughan D, Crosby D, Wahab NA, Saadeh FA, Gleeson N. Opportunistic and interventional salpingectomy in women at risk: a strategy for preventing pelvic serous cancer (PSC). Eur J Obstet Gynecol Reprod Biol 2013;170:251-254. [ Links ]
72. Gill SE, Mills BB. Physician opinions regarding elective bilateral salpingectomy with hysterectomy and for sterilization. J Minim Invasive Gynecol 2013;20:517-521. [ Links ]
73. British Columbia Ovarian Cancer Prevention Project at http://www.ovcare.ca/prevention/ [ Links ]
74. Ginecologia SPd, Oncológica SdG, Médica SPdO, Oncologia SPdR, Patológica SPdA, Médicos CdGeOdOd, Médicos CdOMdOd, Médicos CdRdOd. Cancro Ginecológico - Consensos Nacionais 2013. 2013. [ Links ]
Endereço para correspondência | Dirección para correspondencia | Correspondence
Ana Filipa Rodrigues Ferreira
Centro Hospitalar e Universitário de Coimbra
E-mail: filipaferreira44@gmail.com
Recebido em: 16-11-14
Aceite para publicação: 22-06-15