Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Portuguesa de Pneumologia
Print version ISSN 0873-2159
Rev Port Pneumol vol.16 no.4 Lisboa Aug. 2010
Pneumonia aguda fibrinosa e organizante
Cláudia Santos 1, Fátima Fradinho 2 e Alexandra Catarino 2
1 Interna Complementar de Pneumologia
2 Assistente Hospitalar de Pneumologia
Serviço de Pneumologia dos Hospitais da Universidade de Coimbra
Director – Dr. Mário Chaves Loureiro
Resumo
O padrão histológico de Pneumonia Aguda Fibrinosa e Organizante (AFOP – Acute Fibrinous And Organizing Pneumonia), descrito por Beasley em 2002, caracteriza-se pela existência de fibrina intra-alveolar sob a forma de bolas de fibrina e pneumonia organizativa difusa. A apresentação clínica desta doença intersticial pulmonar pode ser aguda ou subaguda, diferindo no entanto dos outros padrões histológicos habitualmente associados a lesão pulmonar aguda – Lesão Alveolar Difusa (DAD), Pneumonia Organizativa (OP) e Pneumonia Eosinofílica (EP). A propósito deste tema, os autores fazem uma revisão da literatura e descrevem o caso clínico de um doente de 44 anos, com aspectos imagiológicos e evolução pouco habituais.
Palavras-chave: AFOP, bolas de fibrina, pneumonia organizativa.
Acute fibrinous and organizing pneumonia
Abstract
The histologic pattern of Acute Fibrinous and Organizing Pneumonia (AFOP), described by Beasley in 2002, is characterized by the existence of intra alveolar fibrin in the form of fibrin “balls” and diffuse organizing pneumonia. Presenting symptoms of this interstitial pulmonary disease can be acute or subacute. However, it differs from the well -recognized histologic patterns of acute pulmonary lesion – Diffuse Alveolar Damage (DAD), Organizing Pneumonia (OP) and Eosinophilic Pneumonia (EP).
The authors carry out a review of the literature concerning this topic and describe the clinical case of a 44 -year -old patient with unusual imaging features and outcome.
Key-word: AFOP, fibrin balls, organizing pneumonia.
A Pneumonia Aguda Fibrinosa e Organizante (AFOP – Acute Fibrinous and Organizing Pneumonia) é um padrão histológico descrito por Beasley et al.1 em 2002. Está associado a uma apresentação clínica aguda ou subaguda, diferindo no entanto dos padrões histológicos clássicos de lesão pulmonar aguda – Lesão Alveolar Difusa (DAD – Diffuse Alveolar Damage), Pneumonia Organizativa (OP – Organizing Pneumonia) e Pneumonia Eosinofílica (EP – Eosinophilic Pneumonia)2.
Histologicamente, caracteriza-se pela existência de fibrina intraalveolar na forma de bolas de fibrina dentro dos espaços alveolares e pneumonia organizativa com distribuição difusa, consistindo em tecido conjuntivo intraluminal nos ductos alveolares e bronquíolos. Na série de 17 doentes de Beasley foram ainda encontrados hiperplasia de pneumócitos tipo II, edema, inflamação aguda e crónica e alargamento intersticial.
Os doentes com AFOP têm uma evolução clínica semelhante àqueles com padrão histológico de DAD. Apesar disso, diferem em vários aspectos, nomeadamente por na AFOP a fibrina intraalveolar organizada constitui a característica dominante, não sendo esta o componente principal da DAD, as membranas hialinas clássicas da DAD estão ausentes e a distribuição da fibrina é difusa, ao contrário do que se verifica na DAD. Os doentes com padrão histológico de DAD têm habitualmente uma má evolução clínica, com insuficiência respiratória aguda, conduzindo muitas vezes à necessidade de ventilação mecânica, com uma taxa de mortalidade de 50 a 60%. Apesar da evolução clínica semelhante destas duas entidades, que levou Beasley a supor que a AFOP pudesse representar uma variante fibrinosa da DAD, quase todos os doentes com padrão de DAD necessitam de suporte ventilatório, situação que no entanto apenas se verificou em 30% dos doentes da série desta autora. Todos estes dados sugerem que a AFOP representa provavelmente um padrão histológico único previamente não identificado. O padrão OP é caracterizado pela existência de corpos fibroblásticos de Masson nos espaços alveolares, ductos e bronquíolos, não característicos da AFOP.
Tal como a AFOP, também o padrão EP pode ter fibrina intraalveolar. No entanto, o achado histológico principal neste padrão é a acumulação intraalveolar de eosinófilos e macrófagos, com predomínio dos primeiros. Pelo contrário, na AFOP, os eosinófilos são raros ou estão ausentes.
Na série de Beasley, os sintomas de apresentação eram agudos ou subagudos, sendo que nenhum dos doentes teve sintomas mais de 2 meses antes da realização da biopsia. Os sintomas dominantes eram a dispneia, a febre e a tosse. Hemoptises e sintomas constitucionais foram menos frequentes.
A AFOP pode ser idiopática ou estar associada a causas conhecidas ou doenças subjacentes. Na série de Beasley, verificou-se associação a doenças vasculares do colagénio (polimiosite e espondilite anquilosante), também referida por Balduin et al.3, exposições ocupacionais (zoologia, minas de carvão, construção civil, spray de cabelo), alterações do estado imunitário (corticoterapia prolongada, diabetes mellitus mal controlada, alcoolismo, linfoma), exposição a fármacos (amiodarona) e infecções (Haemophilus influenza e Acinetobacter baumanni).
A propósito da associação com infecções, Hwang et al.4 descreveu, em doentes com SARS (severe acute respiratory syndrome), um predomínio de padrão DAD ou AFOP, ou a mistura dos dois, realçando uma vez mais a possibilidade de associação destes dois tipos histológicos.
Yokogawa e Alcid5 relataram um caso clínico de AFOP subsequente a uma reacção de hipersensibilidade ao abacavir numa doente VIH positiva, com infiltrados pulmonares bilaterais e necessidade de ventilação mecânica. A evolução foi favorável após suspensão dos antiretrovirais. Ainda no contexto da AFOP secundária a fármacos, foi descrita associação desta entidade com a decitabina, utilizada no tratamento da síndroma mielodisplásica6.
Noutro caso clínico descrito por Prahalad et al.7, uma doente de 14 anos com dermatomiosite juvenil desenvolveu infiltrados pulmonares difusos, com evolução fulminante apesar de todas as medidas terapêuticas. A biópsia mostrou as bolas de fibrina associadas à AFOP.
Foi também descrito por Kim et al.8, numa doente a quem foi diagnosticada leucemia linfoblástica aguda e que apresentava infiltrado no lobo superior do pulmão direito, lesão pulmonar aguda fibrinosa com organização difusa correspondente a AFOP.
Lee et al.9 descreveram um caso de AFOP num doente com leucemia mielóide aguda submetida a transplante alogénico da medula óssea, que apresentava na TAC do tórax nódulos miliares difusos e opacidades em vidro despolido bilateralmente.
Cincotta et al.10, para além de descreverem o caso de uma criança com AFOP no contexto de infecção pelo vírus sincicial respiratório, fez um estudo retrospectivo de biopsias pulmonares de crianças com ARDS (acute respiratory distress syndrome), verificando que nas 9 incluídas 7 tinham achados clássicos de DAD, 2 características sugestivas de padrão misto (DAD e AFOP) e em 5 havia alterações sugestivas de infecção viral. Neste estudo é formulada a hipótese de a AFOP ser uma característica das fases tardias da lesão pulmonar aguda, predominando a DAD nas fases precoces da mesma.
Relativamente aos achados imagiológicos, Beasley descreveu essencialmente infiltrados parenquimatosos difusos predominantes nos lobos inferiores, não havendo referência a lesões nodulares. No entanto, Kobayashi et al.11 descreveu o caso de um doente de 52 anos, com tosse e dispneia com 2 meses de evolução, cujos exames imagiológicos revelaram um nódulo pulmonar solitário com 2 cm de diâmetro, com broncograma aéreo e um contorno esfumado. A histologia da biopsia evidenciou bolas de fibrina e tecido organizado. Um aspecto curioso deste caso clínico diz respeito ao facto dos achados imagiológicos se terem alterado após 3 semanas, com infiltrado difuso e pequenos nódulos centrilobulares, consolidação alveolar e espessamento de paredes brônquicas. A alteração dos aspectos imagiológicos faz lembrar o que pode suceder na pneumonia organizativa criptogénica (COP). Na COP as alterações imagiológicas mais frequentes e típicas correspondem a múltiplas opacidades alveolares difusas, com distribuição periférica e bilateral, podendo migrar espontanemente12,13.
Beasley não fez referência quer ao estudo funcional dos doentes que estudou quer a eventuais alterações do líquido de lavagem broncoalveolar.
Jarbou et al.14 descreveram um caso clínico de um doente de 70 anos com dispneia de esforço e pieira, fumador de 20 UMA e com DPOC ligeira. Este autor refere que a doença obstrutiva das vias aéreas poderá representar um factor de risco para o desenvolvimento futuro de AFOP sob determinadas circunstâncias.
Beasley, à semelhança de outro autores15, refere que o diagnóstico da AFOP é mais bem estabelecido quando efectuado a partir de amostras maiores, obtidas por VATS (video-assisted toracoscopic surgery), biopsias a céu aberto ou amostras de autópsias, em comparação com outras biopsias, cujo material seria à partida insuficiente.
As modalidades de tratamento usadas nos doentes da série descrita por Beasley incluíram antibióticos de forma isolada, corticosteróides isolados, corticosteróides após ausência de melhoria com antibióticos, antibióticos e corticosteróides em simultâneo, diuréticos e necessidade de instituição de ventilação mecânica nalguns doentes. Nenhum tipo de tratamento foi identificado como o mais vantajoso, mesmo quando a condição subjacente é identificada. No caso de AFOP descrito por Damas et al16, o doente efectuou terapêutica com prednisona e ciclofosfamida, com boa evolução. Recentemente, foi também descrito um caso clínico de um doente com AFOP que se apresentou com doença pulmonar rapidamente progressiva, com necessidade de suporte ventilatório. Após estabelecido o diagnóstico foi iniciada terapêutica com metilprednisolona e micofenolato de mofetil, com excelente resposta e rápida recuperação17.
Beasley descreveu dois tipos de evolução clínica: aqueles com doença fulminante e progressão rápida para a morte e aqueles com evolução subaguda, menos fulminante, que recuperaram. Na primeira situação, relativa a 9 doentes, o tempo que decorreu entre a apresentação dos sintomas e a morte variou entre 6 e 36 dias, com média de 29 dias.
Caso clínico
Os autores descrevem o caso clínico de um doente do sexo masculino, 44 anos, raça caucasiana, casado, soldador, natural e residente em Vilela, fumador, com história de toracalgia pleurítica à direita e expectoração hemoptóica desde há um mês. O doente negava dispneia, febre, sudorese nocturna, astenia, anorexia e perda ponderal.
Para esclarecimento desta sintomatologia, recorreu ao Serviço de Urgência dos Hospitais da Universidade de Coimbra (Janeiro de 2008), tendo realizado telerradiografia do tórax que evidenciou opacidade homogénea no andar médio do hemitórax direito, de contornos mal definidos, vagamente nodular (Fig. 1). Face ao resultado, foi solicitada tomografia computorizada (TC) do tórax, realizada em ambulatório, que mostrou alterações fortemente sugestivas de corresponderem a neoplasia primitiva pulmonar (Fig. 2), motivo pelo qual o doente foi enviado à consulta de pneumologia.
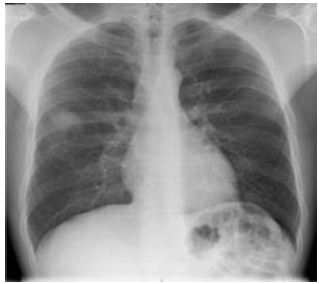
Fig. 1 – Telerradiografia do tórax (PA) – opacidade homogénea no andar médio do hemitórax direito, de contornos mal definidos, vagamente nodular.
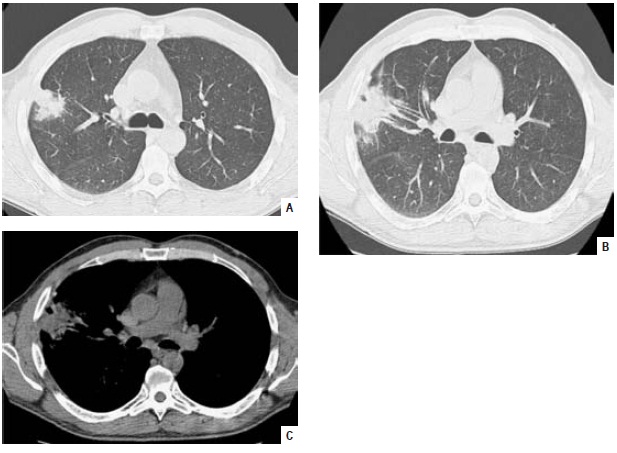
Fig. 2 (A, B e C) – TC do tórax – formação expansiva de contorno espiculado localizada no segmento anterior do lobo superior direito, medindo 4,2 cm de diâmetro. Trata-se de uma formação sólida, evidenciando uma zona mais hipodensa central, após administração de contraste, compatível com área necrótica. O aspecto é fortemente sugestivo de corresponder a neoplasia primitiva
Dos antecedentes pessoais, de referir hepatite C crónica, diagnosticada em 1998, sendo o doente seguido em consulta externa de infecciologia e tendo já efectuado terapêutica com ribavirina e interferão á peguilado, por períodos de 24 semanas, em 2000 e 2005. Tratava-se de um doente com hábitos etílicos moderados, fumador de 20 UMA e ex-toxicodependente de cocaína inalada há 10 anos, tendo consumido durante 2 anos. Relativamente à história epidemiológica, de referir o contacto com canários desde há 15 anos. Quanto à história profissional, o doente foi rectificador de motores de automóveis durante 20 anos, trabalhou 2 meses em minas de volfrâmio e era soldador desde 1995. Sem antecedentes familiares relevantes.
Ao exame objectivo apresentava-se consciente, orientado e colaborante, com bom estado geral, eupneico, acianótico, apirético e normotenso, sem adenopatias palpáveis. À auscultação pulmonar apresentava murmúrio vesicular simetricamente audível, sem ruídos adventícios. A auscultação cardíaca era rítmica, sem sopros detectáveis. Sem alterações abdominais ou dos membros inferiores.
Dos exames complementares de diagnóstico solicitados, de referir discreta elevação das provas hepáticas (TGP 75 U/L; TGO 55 U/L; Gama GT 81 U/L), discreta leucocitose (11,7 G/L) e gasometria arterial (FiO2 21%) normal (pH 7,44; PaO2 96 mmHg; PaCO2 36 mmHg; HCO3 22,9 mEq/L; saturação O2 98%).
Os marcadores tumorais solicitados (CEA, PSA, CA 19.9, CYFRA 21.1, NSE) e os anticorpos VIH 1 e 2 foram negativos. Não apresentava alterações no estudo uncional ventilatório: CVF – 4,86L (113,50%), VEMS – 3,65L (103,73%), VEMS/CVF % – 75,02, CPT – 7,12L (109,5%), Difusão alveolocapilar pelo monóxido de carbono – 95,1%.
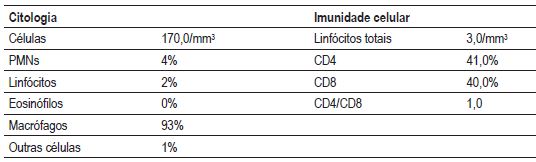
O doente realizou videobroncofibroscopia que não evidenciou lesões endobrônquicas visíveis, com orifícios permeáveis e esporões afilados. A cultura do aspirado brônquico era polimicrobiana, sem significado patogénico, sendo a pesquisa de micobactérias negativa. A citologia do aspirado brônquico não mostrou células neoplásicas. Foram efectuadas biopsias distais do lobo superior direito, cujo resultado histológico não permitiu chegar a conclusões diagnósticas. No mesmo acto, foi efectuada lavagem broncoalveolar, que não evidenciou alterações relevantes (Quadro I).
Quadro I – Líquido de lavagem broncoalveolar
A ecografia abdominal superior, solicitada para estudo de eventuais lesões secundárias, tendo em conta a forte suspeita clínica e imagiológica de neoplasia primitiva, não mostrou alterações.
Face aos resultados inconclusivos, o doente foi proposto para realização de biopsia transtorácica (BTT), sendo que o resultado anatomopatológico não foi esclarecedor, sugerindo patologia inalatória ou eventualmente alveolite alérgica específica.
Perante a persistência de incerteza diagnóstica, e com intuito de reavaliação imagiológica, foi solicitada nova TC do tórax (Fig. 3), que evidenciou redução das dimensões da lesão, mantendo no entanto contornos irregulares. Proposto então para ressecção cirúrgica, foi realizada ressecção em cunha do nódulo pulmonar. Macroscopicamente, observou-se um nódulo com cerca de 4 cm com aspecto de lesão inflamatória. Microscopicamente, o parênquima pulmonar evidenciava algumas áreas com arquitectura habitual preservada e outras em que se observava um discreto espessamento dos septos interalveolares e infiltrado inflamatório de intensidade moderada (à custa de linfócitos, plasmócitos, alguns neutrófilos e macrófagos). Os espaços alveolares encontravam-se preenchidos por células inflamatórias (macrófagos, alguns linfócitos e neutrófilos). Em zona central existia uma área cavitada, abcedada, preenchida por abundantes neutrófilos. Nalguns espaços alveolares observavam-se depósitos de fibrina, desencadeando um processo inflamatório de tipo crónico, com macrófagos e células gigantes multinucleadas a envolver a fibrina. Havia igualmente proliferação fibroblástica com formação de estruturas polipóides que se projectavam para o interior dos espaços alveolares. Estava ainda presente hiperplasia de pneumócitos tipo II. A pleura visceral apresentava áreas de fibrose e proliferação neovascular associada a infiltrado inflamatório de tipo crónico de intensidade ligeira. Os aspectos histomorfológicos eram enquadráveis em Pneumonia Aguda Fibrinosa e Organizante (AFOP – Acute Fibrinous and Organizing Pneumonia) (Fig. 4).
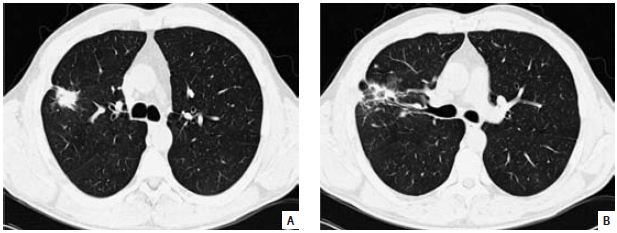
Fig. 3 (A e B) – TC do tórax – Duas áreas de densificação parenquimatosa, justapostas, com contornos espiculados, localizadas no LSD. Ligeira redução das dimensões comparativamente ao exame anterior. A lesão de maior dimensão mede actualmente cerca de 25 mm. Ligeiro espessamento da pleura parietal adjacente
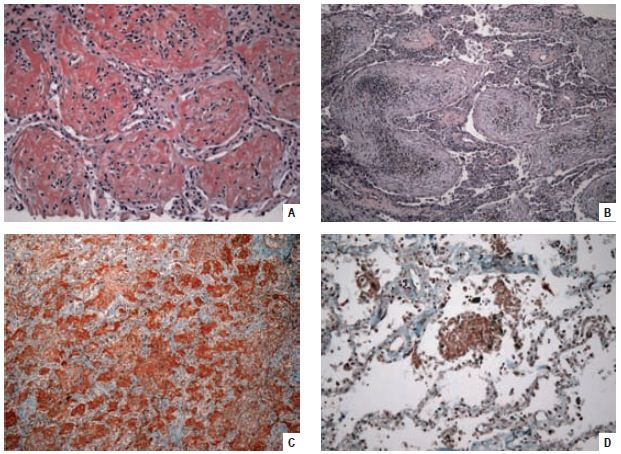
Fig. 4 – Exame histológico. A – Presença de massas de fibrina em “bola” nos espaços alveolares, HE, 200×. B – Área de pneumonia em organização, HE, 200×. C – Extensa deposição de fibrina nos espaços alveolares, característica da AFOP, HE, 100x. D – “Bola” de fibrina posta em evidência pela técnica tricrómico de Masson, TM, 200×
Uma vez realizada a ressecção da lesão em causa, e atendendo à ausência de sintomatologia respiratória ou outra à data do diagnóstico, à ausência de alterações funcionais e de insuficiência respiratória, não foi efectuada terapêutica médica.
Dois meses após a ressecção cirúrgica, foi efectuado novo controlo imagiológico por TC do tórax (Fig. 5), que evidenciou sobretudo alterações fibróticas.
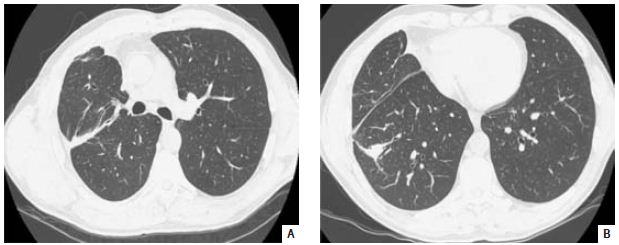
Fig. 5 – TC do tórax (A e B) – Várias opacidades lineares grosseiras à direita, de tipo fibrótico, que assumem morfologia pseudonodular em algumas áreas, envolvendo quer o lobo superior quer o inferior. Distorção da arquitectura broncovascular, com redução do volume do LSD e discreto desvio homolateral do mediastino. Espessamento pleural à direita
Em Outubro de 2008 o doente foi novamente internado no Serviço de Pneumologia, agora por pneumonia à esquerda (Fig. 6). Analiticamente apresentava elevação da PCR e leucocitose com neutrofilia, verificando-se boa evolução clínica e imagiológica sob antibioterapia com amoxicilina/ácido clavulânico e azitromicina. O doente mantém seguimento regular em consulta externa de pneumologia, estando assintomático até à data e sem alterações imagiológicas relevantes (Fig. 7).
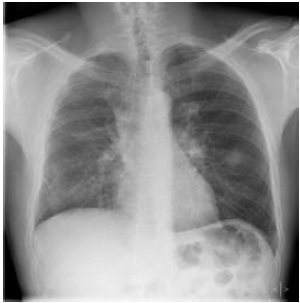
Fig. 6 – Telerradiografia do tórax (PA) – Opacidades lineares grosseiras nos andares médio e inferior do hemitórax direito, de provável natureza residual; opacidade vagamente nodular, de limites imprecisos, com densidade de tecidos moles e cerca de 3 cm de diâmetro, na transição do andar médio para o andar inferior do hemitórax esquerdo
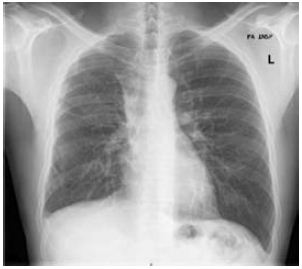
Fig. 7 – Telerradiografia do tórax (PA) – opacidades lineares grosseiras nos andares médio e inferior do hemitórax direito, de provável natureza residual; sem outras alterações parenquimatosas relevantes
Discussão
A AFOP é uma entidade histológica muito recente, referente a doença intersticial pulmonar com envolvimento de vias aéreas, que necessita ainda de melhor caracterização clínica e imagiológica. Neste sentido, os autores consideraram ser útil a descrição do caso clínico anterior e o destaque das suas particularidades, menos habituais relativamente à descrição de Beasley.
Neste caso, a sintomatologia dominante consistiu em toracalgia pleurítica, (referida apenas por 5 doentes da série de Beasley) e expectoração hemoptóica, ambas com 1 mês de evolução.
O doente referia exposição ocupacional significativa, quer na indústria automóvel, quer nas minas de volfrâmio. Salienta-se também a exposição prolongada a fármacos e o facto de se tratar de um doente portador de hepatite C crónica, com antecedentes de toxicodependência. Resta saber se alguns destes factores têm implicação directa no aparecimento da entidade clínica e histológica descrita.
As alterações imagiológicas descritas, muito sugestivas de neoplasia pulmonar primitiva atendendo ao contorno espiculado da área de densificação parenquimatosa e à sua dimensão, não são as mais típicas desta entidade, se tivermos em conta a descrição de Beasley. No entanto, há que ter em consideração a descrição prévia11 sob a forma de nódulo solitário do pulmão.
Pouco tempo após a ressecção cirúrgica que permitiu o diagnóstico, o doente desenvolveu clínica compatível com infecção respiratória, com leucocitose e elevação da PCR. A telerradiografia do tórax evidenciou uma opacidade vagamente nodular, de limites imprecisos, na transição do andar médio para o andar inferior do hemitórax esquerdo. A dúvida permanecerá se essa opacidade não seria uma nova lesão de AFOP, migratória como no caso do doente de Kobayashi11.
O estudo funcional ventilatório e os resultados do líquido de lavagem broncoalveolar, ambos sem alterações dignas de registo, não permitem tirar conclusões relativas a esta entidade.
O facto de o doente ter sido submetido a ressecção em cunha da área pulmonar afectada, não apresentar alterações funcionais ventilatórias, não ter insuficiência respiratória e estar assintomático após a intervenção cirúrgica, motivou a opção da não instituição de terapêutica médica. Há que ter em conta que a forte suspeição imagiológica de neoplasia pulmonar primária conduziu ao procedimento cirúrgico instituído, atitude esta não preconizada em nenhum dos outros casos clínicos revistos.
O doente, presentemente seguido em consulta externa de pneumologia, teve uma evolução favorável, mantendo-se actualmente assintomático.
Conclusão
A AFOP, caracterizada por bolas de fibrina intraalveolar e por áreas de pneumonia organizada, parece corresponder a um padrão histológico distinto das outras entidades associadas a apresentação clínica aguda – DAD, OP e EP.
No entanto, é necessária mais informação clínica e imagiológica para melhor caracterizar esta entidade, motivo pelo qual procedemos à revisão da literatura e à descrição deste caso clínico, esperando assim contribuir com mais dados para um conhecimento mais aprofundado desta patologia recentemente descrita e ainda controversa.
Bibliografia
1. Beasley MB, Franks TJ, Galvin JR, et al. Acute fibrinous and organizing pneumonia: a histologic pattern of lung injury and possible variant of diffuse alveolar damage. Arch Pathol Lab Med 2002; 126:1064 -1070. [ Links ]
2. Robalo Cordeiro C. Airway involvement in interstitial lung disease. Curr Opin Pulm Med 2006; 12(5):337 -341. [ Links ]
3. Balduin R, Giacometti C, Saccarola L, et al. Acute fibrinous and organizing pneumonia in a patient with collagen vascular disease stigma. Sarcoidosis Vasc Diffuse Lung Dis 2007; 24(1):78 -80. [ Links ]
4. Hwang DM, Chamberlain DW, Poutanen SM, et al. Pulmonary pathology of severe acute respiratory syndrome in Toronto. Mod Pathol 2005; 18:1 -10. [ Links ]
5. Yokogawa N, Alcid DV. Acute fibrinous and organizing pneumonia as a rare presentation of abacavir hypersensitivity reaction. AIDS 2007; 21:2116 -2117. [ Links ]
6. Vasu TS, Cavallazzi R, et al. A 64 -year -old male with fever and persistent lung infiltrate. Respir Care 2009; 54(9):1263 -1265. [ Links ]
7. Prahalad S, Bohnsack JF, Maloney CG, Leslie KO. Fatal acute fibrinous and organizing pneumonia in a child with juvenile dermatomyositis. J Pediatr 2005; 146:289 -292. [ Links ]
8. Kim BC, Servi R, Sucai BI, Ramsey R. Acute lymphoblastic leukemia presenting with an acute fibrinous and organizing pneumonia. J Resp Dis 2007; 28:33 -35. [ Links ]
9. Lee SM, Park JJ, et al. Acute fibrinous and organizing pneumonia following hematopoietic stem cell transplantation. Korean J Intern Med 2009; 24:156 -159. [ Links ]
10. Cincotta DR, Sebire NJ, Lim E, Peters MJ. Fatal acute fibrinous and organizing pneumonia in an infant: the histopathologic variability of acute respiratory distress syndrome. Pediatr Crit Care Med 2007; 8(4):378-382. [ Links ]
11. Kobayashi H, Sugimoto C, Kanoh S, et al. Acute fibrinous and organizing pneumonia: initial presentation as a solitary nodule. J Thorac Imaging 2005; 20:291 -293. [ Links ]
12. Cordier JF. Organising pneumonia. Thorax 2000; 55:318 -328. [ Links ]
13. Akira M, Yamamoto S, Sakatani M. Bronchiolitis obliterans organizing pneumonia manifesting as multiple large nodules or masses. AJR 1998; 170:291 -295. [ Links ]
14. Jarbou M, Yusof M, Coberly E, et al. Acute fibrinous and organizing pneumonia. Chest 2006; 130:300Sc301. [ Links ]
15. Poletti V, Casoni GL. Cryptogenic organizing pneumonia or acute fibrinous and organizing pneumonia? Eur Respir J 2005; 25:1128. [ Links ]
16. Damas C, Morais A, Moura CS, Marques JA. Acute fibrinous and organizing pneumonia. Rev Port Pneumol 2006; XII(5):615 -620. [ Links ]
17. Bhatti S, Hakeem A, et al. Severe acute fibrinous and organizing pneumonia (AFOP) causing ventilator failure: successful treatment with mycophenolate mofetil and corticosteroids. Respiratory Medicine 2009; 103: 1764 -1767. [ Links ]
Serviço de Pneumologia dos Hospitais da Universidade de Coimbra
Praceta Prof. Mota Pinto
3000 -075 Coimbra
e-mail: claudiaraimundo80@gmail.com
Recebido para publicação/received for publication: 09.11.03
Aceite para publicação/accepted for publication: 10.01.07