Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Pneumologia
versão impressa ISSN 0873-2159
Rev Port Pneumol v.15 n.6 Lisboa nov. 2009
Estratégias de suporte ventilatório no recém-nascido pré-termo – Inquérito nacional (2008)
Resumo
Introdução: As estratégias de suporte ventilatório utilizadas no recém-nascido têm sido motivo de grande investigação.
Objectivos: Avaliar as práticas de suporte ventilatório nas unidades de neonatologia nacionais utilizadas na assistência ao recém-nascido de extremo baixo peso e avaliar se estão em conformidade com a prática baseada na evidência.
Métodos: Foi enviado, por via electrónica, a 31 unidades de neonatologia nacionais, um inquérito sobre tipos de ventiladores, modos de ventilação, monitorização da função pulmonar, valores de saturação de oxigénio permitidos e prevalência de doença pulmonar crónica da prematuridade.
Resultados: A percentagem de resposta foi de 94%. O modelo de ventilador Draeger Babylog é o mais utilizado. Doze (41%) unidades preconizam o NCPAP precoce. A ventilação sincronizada é de eleição em 24 (83%) unidades (SIMV, SIPPV, PSV) e 4 (14%) têm possibilidade de ventilação por alta frequência oscilatória. O modo ventilatório SIMV é o mais utilizado (n=13, 45%) no desmame ventilatório. O surfactante exógeno é usado preferencialmente de modo profiláctico em 12 (41%) unidades. Todas as unidades usam valores de função respiratória no ajuste dos parâmetros ventilatórios e cinco (17%) utilizam monitorização contínua da PaCO2: medição transcutânea = 3; capnometria = 2. Dezassete (59%) unidades utilizam valores de saturação de oxigénio de 90%-95% na doença das membranas hialinas e 15 (52%) utilizam valores de 85%-90% na doença pulmonar crónica da prematuridade. A prevalência de doença pulmonar crónica da prematuridade variou entre os 0% e os 75% (mediana: 10).
Conclusão: As estratégias de suporte ventilatório usadas nas unidades portuguesas reflectem, em parte, a evidência de estudos multicêntricos aleatorizados. É necessário mais investimento no uso de NCPAP precoce, preferencialmente com prongs binasal, uso do modo SIPPV no desmame ventilatório, uso de estratégias ventilatórias com volumes correntes optimizados e utilização criteriosa de surfactante exógeno, de modo a assegurar a prática baseada na evidência.
Palavras-chave: Recém-nascido, ventilação, doença pulmonar crónica da prematuridade, doença das membranas hialinas, saturação de oxigénio.
Respiratory support strategies for the preterm newborn – National survey 2008
Abstract
Background: Respiratory support strategies for the preterm newborn have been the subject of intense research.
Aim: To survey neonatal respiratory support practices in Portugal and to determine whether they reflect evidence from randomised trials.
Methods: Questionnaires were given out to 31 Portuguese neonatal units to determine the types of ventilators, modes of ventilation, lung function monitoring, use of exogenous surfactant, oxygen saturation levels used and the prevalence of chronic lung disease in the preterm newborn.
Results: There was a 94% response rate. Draeger babylog was the most frequently used ventilator in neonates. Twelve (41%) units prefer to use early nasal continuous positive airway pressure (NCPAP) whenever possible. Triggered ventilation is the choice of invasive ventilation in 24 (83%) units (SIMV, SIPPV, PSV); four (14%) units have high frequency oscillation ventilation. SIMV is the most frequent (n=13, 45%) weaning mode. Exogenous surfactant is used as prophylactic in 12 (41%) units. All units use lung function measurements to aid choice of ventilator settings and five (17%) units monitor PaCO2 (transcutaneous = 3; capnometry = 2). Seventeen (59%) units allow oxygen saturation levels from 90% to 95% in infants with respiratory distress syndrome and 15 (52%) levels from 85% to 90% in infants with chronic lung disease. Prevalence of chronic lung disease of prematurity ranged from 0% to 75% (median: 10).
Conclusions: Many respiratory strategies for extremely low birth weight infants reflect the result of large randomised trials. More effective methods may be required to encourage the use of early NCPAP preferably with binasal prongs, the use of SIPPV as the main weaning mode, the use of volume targeted ventilation and a more judicious use of exogenous surfactant in order to ensure evidence–based practice.
Key-words: Newborn, ventilation, chronic lung disease of prematurity, respiratory distress syndrome, oxygen saturation.
Introdução
Nos últimos 50 anos tem-se assistido a uma diminuição importante na mortalidade perieneonatal. Entre os vários avanços nas diferentes áreas da medicina associados a esta melhoria merecem especial destaque a descoberta (1959)1, a utilização com sucesso (1980)2 e a aprovação (1990)3 do uso de surfactante exógeno para o tratamento da doença das membranas hialinas, o uso antenatal de corticosteróides (1972)4, bem como o progresso nos aparelhos e técnicas utilizadas no suporte ventilatório do recém-nascido de risco.
A ventilação assistida é a principal das técnicas utilizadas em cuidados intensivos neonatais.
Desde antigas descrições, no Antigo Testamento, de reanimação com respiração boca-a-boca e da primeira descrição de Hipócrates (400 aC)5 de intubação traqueal para ventilação pulmonar, a era moderna de ventilação mecânica na criança pode ser datada a 1953, com Donald e Lord6. Desde então, o aperfeiçoamento dos aparelhos e o desenvolvimento de novas metodologias de ventilação contribuíram de modo significativo para aumentar a sobrevivência do recém-nascido de risco. Actualmente, a taxa de sobrevivência é superior a 50% para recém-nascidos pré-termo acima das 25 semanas de idade gestacional7 e é observada uma sobrevivência acima das 32 semanas próxima da do recém-nascido de termo (≥ 37 semanas).
Devido ao melhor seguimento e aos avanços da tecnologia médica, o aumento da sobrevivência de recém-nascidos pré–termo acompanha-se de um significativo número de complicações, nomeadamente a evolução para doença pulmonar crónica da prematuridade, também referida como displasia broncopulmonar8.
Como consequência deste facto, têm surgido várias publicações traduzindo os resultados de investigação clínica efectuada com o objectivo de melhorar as estratégias de suporte ventilatório no recém–nascido pré-termo, sobretudo no de extremo baixo peso (peso ao nascimento < 1000 g)9. Este estudo teve por objectivo analisar as práticas correntes nas unidades de neonatologia nacionais, em relação a estratégias de suporte ventilatório utilizadas na assistência ao recém-nascido de extremo baixo peso, e verificar se estas práticas reflectem a evidência de estudos multicêntricos aleatorizados.
Material e métodos
Foi enviado, por via electrónica, um questionário (em anexo) a 31 unidades de neonatologia de Portugal continental, Açores e Madeira. (Nota: Em Portugal existem 40 unidades de neonatologia, 19 com apoio perinatal diferenciado e 21 sem apoio perinatal diferenciado, tendo o inquérito sido enviado às mais representativas em número de nascimentos.). Foi contactado um elemento de cada uma dessas unidades que ficaria responsável pelo preenchimento e re envio do inquérito. O preenchimento do inquérito deveria ser efectuado por um ou mais clínicos, de modo a traduzir as práticas utilizadas na unidade. No caso de dúvidas no preenchimento do inquérito poderia ser contactado qualquer um dos elementos da Comissão para a Investigação da Secção de Neonatologia da Sociedade Portuguesa de Pediatria.
O inquérito incluía 18 questões, sendo 14 de resposta sim/não, três de resposta directa e uma de resposta opcional. As questões abrangiam as práticas de suporte ventilatório utilizadas na assistência ao recém-nascido de extremo baixo peso, desde o nascimento à retirada (desmame) do ventilador. Foram também inquirido os valores de saturação de oxigénio obtidos por oximetria de pulso, indicados no recém-nascido com doença das membranas hialinas e com doença pulmonar crónica da prematuridade, quantos recém-nascidos de extremo baixo peso são admitidos anualmente e qual a percentagem de doença pulmonar crónica nos sobreviventes no ano 2007. Foi também dada a possibilidade de responder livremente às questões de resposta sim/não sobre estratégias ventilatórias.
Os resultados obtidos foram comparados com os resultados de estudos aleatorizados e quase aleatorizados, nomeadamente os que reuniram critérios de inclusão para as últimas revisões da Cochrane Database of Systematic Reviews sobre ventilação mecânica sincronizada no recém-nascido (14 estudos) de 20089, sobre volume corrente optimizado (quatro estudos) de 200510, ventilação de alta frequência oscilatória (15 estudos) de 200811 e aparelhos e pressões para administração de pressão positiva contínua nasal no recém-nascido pré-termo (sete estudos) de 200812.
Resultados
A taxa de resposta ao inquérito foi de 94% (29/31), incluindo 19 (70%) centros com apoio perinatal diferenciado. Dois centros (7%) não possuem maternidade, pelo que não prestam assistência no parto, sendo, no entanto, centros de referência de recém-nascidos pré-termo nascidos em centros sem apoio perinatal diferenciado.
Os aparelhos para ventilação invasiva disponíveis nas diversas unidades encontram-se discriminados no Quadro I. Nove (31%) unidades possuem um único tipo de ventilador (Draeger Babylog = 5; Bear Cub = 2; Servo 2000 = 1; VIP Bird = 1). Os ventiladores mais frequentemente utilizados no recém-nascido de extremo baixo peso são: Draeger Babylog (20 unidades); VIP Bird (cinco unidades); SLE 2000 (quatro unidades); SLE 5000 (duas unidades); Bear Cub (duas unidades); Servo 300 (duas unidades); Vyasis Avea (uma unidade).
Quadro I – Aparelhos de ventilação invasiva disponíveis nas 29 unidades de neonatologia

Entre as 27 unidades que prestam assistência no parto, 13 (48%) (das quais, 12 unidades com apoio perinatal diferenciado) têm a possibilidade de utilizar NCPAP (nasal continuous positive airway pressure) na sala de partos e 12 (44%) optam preferencialmente pela sua utilização na assistência ao recém-nascido de extremo baixo peso com alguma capacidade respiratória (Quadro II). Catorze (52%) unidades têm a possibilidade de efectuar o transporte do recém-nascido de extremo baixo peso com NCPAP da sala de partos para a unidade de cuidados intensivos neonatais.
Quadro II – Utilização do NCPAP na sala de partos, transporte e na UCIN

Uma unidade tem possibilidade de usar NCPAP na sala de partos, mas não de efectuar o transporte para o internamento. Uma unidade tem possibilidade de uso precoce e transporte em NCPAP; no entanto, a política de assistência ao recém-nascido de extremo baixo peso com capacidade ventilatória inclui intubação e ventilação convencional. Uma unidade, sem possibilidade de transporte com NCPAP, opta pelo CPAP nasofaríngeo. Em três (11%) unidades o transporte do recém-nascido de extremo baixo peso com necessidade de suporte ventilatório é efectuado com recurso a máscara insufladora e tubo endotraqueal, por indisponibilidade de incubadora de transporte equipada com ventilador.
Os tipos de NCPAP utilizados são: Infant Flow Driver = 14 unidades; ventilador com modo CPAP = 3; ambos = 11; uma unidade sem apoio perinatal diferenciado não utiliza NCPAP. A maioria das unidades utiliza mais de um tipo de aplicação de NCPAP: prongs nasais = 26; máscara nasal = 22; sonda nasofaríngea = 7; cânulas nasais = 1. Uma unidade utiliza unicamente CPAP faríngeo. Uma unidade que utiliza NCPAP utiliza também CPAP endotraqueal.
Na assistência ao recém-nascido de extremo baixo peso na unidade de cuidados intensivos o suporte ventilatório é preferencialmente: NCPAP = 19 (66%); ventilação convencional (VC) = 9 (31%); ventilação por alta frequência oscilatória (VAFO) = 1 (3%). Das unidades que usam preferencialmente NCPAP, uma usa preferencialmente VAFO no recém-nascido com peso ao nascimento inferior a 750 g. As modalidades de suporte ventilatório usadas na fase aguda de dificuldade respiratória (doença das membranas hialinas) e de desmame ventilatório encontram-se representadas no Quadro III. Treze (45%) unidades usam mais de um modo ventilatório na fase aguda. Quinze (52%) utilizam o modo SIMV (synchronized intermitent mandatory ventilation), isoladamente ou associado às opções VG (volume garantido), PS (pressão de suporte) ou PC-PA (pressure controled, pressure assisted).
Quadro III – Modos de ventilação usados no recém-nascido de extremo baixo peso com necessidade de ventilação invasiva, na “fase aguda” e no “desmame” ventilatório
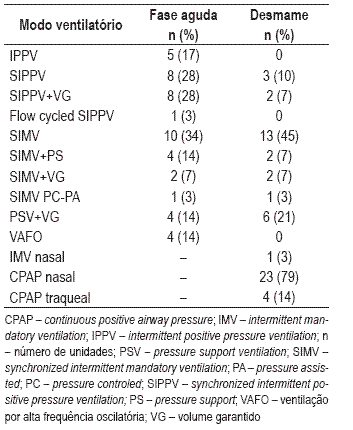
O modo ventilatório mais utilizado no recém-nascido de extremo baixo peso com necessidade de ventilação invasiva é o SIMV, sendo o modo preferido por 10 (34%) unidades. O SIPPV (synchronized intermitent positive pressure ventilation, também designado A/C – assisted controlled) é utilizado isoladamente em seis (21%) unidades, em associação com a op ção VG em seis (21%) unidades, e ambas possibilidades em duas (7%). Uma (3%) unidade utiliza flow cycled SIPPV.
Doze (41%) unidades utilizam surfactante exógeno preferencialmente de modo profiláctico, onze (38%) utilizam apenas de modo curativo e as seis (21%) restantes unidades utilizam ambas as estratégias.
Cinco (17%) unidades utilizam monitorização contínua indirecta da pressão arterial de dióxido de carbono (PaCO2): medição transcutânea = 3; capnometria = 2. Vinte e três (79%) unidades usam parâmetros de função respiratória na correcção da estratégia ventilatória (Quadro IV). Para esse efeito utilizam o monitor do ventilador e duas recorrem também ao uso de monitor separado do ventilador.
Quadro IV – Utilização de parâmetros de função respiratória

No recém-nascido não ventilado com necessidade de oxigenoterapia, as modalidades de administração de oxigénio mais utilizadas são: oxigénio na incubadora = 27 (93%) unidades; sonda nasolabial = 14 (48%); prongs nasais = 13 (45%) e oxigénio sob campânula = 8 (28%).
As saturações de oxigénio por oximetria de pulso mantidas no recém-nascido com doença das membranas hialinas e com displasia broncopulmonar (doença pulmonar crónica da prematuridade) encontram-se representadas no Quadro V.
Quadro V – Valores de saturação de oxigénio, avaliados por oximetria de pulso, mantidos no recém-nascido com doença das membranas hialinas e displasia broncopulmonar
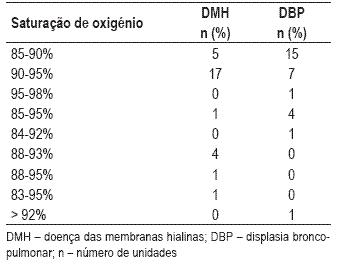
Vinte e três (79%) unidades referiram experiência com a alta de recém-nascidos para o domicílio em oxigenoterapia, oito (28%) com ventilação não invasiva e duas (7%) com ventilação invasiva. O número de recém-nascido de extremo baixo peso admitidos no ano de 2007 nas 19 unidades com apoio perinatal diferenciado variou entre os 3 e os 55 (mediana: 16). A percentagem de doença pulmonar crónica da prematuridade nos sobreviventes no ano 2007, nas 17 unidades com apoio perinatal diferenciado que responderam à questão 18 do inquérito, variou entre os 0% e os 75% (mediana: 10).
Não se verificou associação entre a prevalência de doença pulmonar crónica da prematuridade e o número de admissões de recém–nascidos de extremo baixo peso.
Discussão e conclusões
A taxa de resposta ao inquérito que serviu de base a este estudo foi satisfatória, o que nos permite conhecer as práticas de suporte ventilatório utilizadas nas maioria das unidades de neonatologia nacionais, sobretudo na abordagem do recém-nascido de extremo baixo peso.
Todas as unidades participantes no estudo estão equipadas com ventiladores que permitem ventilação sincronizada. Embora algumas unidades ainda possuam ventiladores que não permitem sincronização, como os ventiladores Sechrist e Infant Star, estes não são usados na ventilação de recém-nascidos de extremo baixo peso. O ventilador para ventilação convencional mais frequente e também mais utilizado é o Draeger Babylog, cujo modelo 8000 plus permite usar o modo de ventilação PSV associado à opção VG (este modo ventilatório não é possível no modelo 8000), um tipo protector de ventilação, uma vez que permite sincronia na inspiração e expiração, garantindo um volume corrente fisiológico. Um número significativo de unidades possui, também, a possibilidade de VAFO. Nem todas as unidades possuem a possibilidade de NCPAP precoce e algumas ainda mantêm como política o uso de ventilação invasiva, mesmo no recém-nascido de extremo baixo peso com evidência de capacidade ventilatória.
Este estudo demonstrou a preferência do NCPAP no recém-nascido de extremo baixo peso com capacidade ventilatória. O NCPAP, particularmente na Escandinávia, é usado preferencialmente à intubação e ventilação assistida, sendo interpretado como um modo ventilatório menos agressivo13. Embora uma metanálise de dois estudos aleatorizados não tenha revelado diferença significativa na incidência de displasia broncopulmonar14, um estudo recente15, comparando duas unidades distintas (Boston e Estocolmo), salientou que o uso de NCPAP desde a sala de partos se associou a menor necessidade de oxigénio suplementar às 40 semanas de idade corrigida.
Relembrando Aly H et al.16, a maioria dos recém-nascidos acima das 27 semanas tolera o NCPAP precoce, não necessitando de ventilação invasiva, enquanto só alguns recém-nascidos abaixo das 27 semanas toleram o NCPAP precoce, necessitando de intubação e de ventilação assistida.
No recém -nascido com necessidade de ventilação invasiva, a maioria das unidades inquiridas usa preferencialmente ventilação sincronizada.
É verdade que as metanálises de estudos comparando ventilação sincronizada versus ventilação convencional não sincronizada em relação a mortalidade (cinco estudos17-21, 1729 doentes), pneumotórax (seis estudos17-22, 1769 doentes), falência da extubação (quatro estudos17,19,21,22, 1056 doentes), hemorragia intraventricular grave (graus III e IV) (cinco estudos17-21, 1729 doentes), dependência de oxigénio aos 28 dias de vida (quatro estudos17,19-21, 805 doentes) e dependência de oxigénio às 36 semanas de idade corrigida (dois estudos17,18, 1310 doentes) não demonstraram benefício da ventilação sincronizada sobre a ventilação convencional não sincronizada. No entanto, a metanálise de quatro estudos17-19,21 (1402 doentes) demonstrou redução significativa na duração da ventilação, com uma diferença média de –34,8 horas na ventilação sincronizada (IC 95%: –62,1 ; –7,4). Também no estudo de Beresford MW et al.18, a incidência de canal arterial patente com necessidade de tratamento médico e/ou cirúrgico foi superior no grupo submetido a ventilação convencional não sincronizada (p < 0,05). Em três estudos23,24a,24b é feita a comparação entre os modos ventilatórios SIPPV e SIMV. As metanálises, incluindo 120 doentes, em relação à falência do desmame ventilatório, falência da extubação, ocorrência de enfisema intersticial ou pneumotórax não demonstraram diferença estatisticamente significativa entre os dois modos ventilatórios. No entanto, a metanálise da duração (em horas) do desmame ventilatório demonstrou uma tendência a menor duração (diferença média –42,38 horas) com o modo SIPPV; no entanto, sem significado estatístico (IC 95%: –94,35; 9,60). De qualquer modo, este resultado sugere para aplicação na prática clínica o uso de SIPPV no desmame ventilatório do recém-nascido pr-termo. Esta ideia é reforçada por outro estudo efectuado por Roze JC et al.25, em que o uso de SIMV com frequência baixa aumentou o consumo de oxigénio e o trabalho respiratório.
O estudo efectuado por Reyes ZC et al.26, que comparou o modo ventilatório SIMV com o modo SIMV+PS em 107 recém-nascidos de extremo baixo peso, não demonstrou diferença significativa em relação a mortalidade, pneumotórax, enfisema intersticial, dependência de oxigénio aos 28 dias e às 36 semanas de idade corrigida, hemorragia intraventricular grave (graus III e IV), patência de canal arterial e dias de ventilação. No entanto, no subgrupo de recém-nascidos com peso ao nascimento 700-1000g, o número de dias de oxigénio suplementar foi inferior no modo SIMV+PS (p = 0,034). Parece haver algum efeito benéfico com os modos ventilatórios PRVC e SIMV+PS, mas ambos foram apenas examinados num único estudo aleatorizado, o que não nos permite concluir acerca da sua eficácia. Mais estudos serão necessários para testar a sua eficácia, de preferência estudos com seguimento a longo prazo.
O presente estudo demonstrou que em algumas unidades se recorre ao uso de estratégias ventilatórias com volumes correntes optimizados, que é possível com alguns ventiladores, e é uma alternativa à ventilação tradicional limitada por pressão. O objectivo é diminuir a hiperdistensão alveolar e atelectasias que se pensa estarem associadas a inflamação e displasia broncopulmonar, sobretudo no recém–nascido pré-termo com grande compliance da parede torácica. A rápida variação da compliance na doença das membranas hialinas, quer por administração de surfactante exógeno, quer por melhoria espontânea da doença, coloca o pulmão em grande risco de volutrauma quando o volume corrente é determinado pela PIP (positive inspiratory pressure) e pela PEEP (positive end expiratory pressure) na ventilação limitada por pressão27. Embora a informação acerca do volume corrente seja escassa no recém-nascido pré-termo, parece variar entre os 4 e os 6 ml/kg27. Esta estratégia de ventilação com volumes correntes optimizados é provavelmente baseada nos resultados da revisão da Cochrane Database of Systematic Reviews, efectuada por McCallion N et al, de 2005, incluindo quatro estudos aleatorizados28-31, com 178 doentes, recrutados nas primeiras 72 horas de vida. Nestes quatro estudos, foram comparados recém-nascidos pré-termo ventilados com volume corrente optimizado (volume controlado ou volume garantido) e recém-nascidos ventilados com ventilação limitada por pressão (SIPPV, IPPV, PSV), sem volume corrente optimizado.
As estratégias com volume corrente optimizado resultaram em significativa redução na duração do tempo de ventilação [WMD–2,93 dias (–4,28; –1,57)], ocorrência de pneumotórax [RR 0,23 (0,07; 0,76), RD –0,11 (–0,20; –0,03), NNT 9] e hemorragia intra ventricular grave (graus III e IV) [RR 0,32 (0,11; 0,90), RD -0,16 ( -0,29; -0,03), NNT 6]. A redução na incidência de displasia broncopulmonar (dependência de oxigénio às 36 semanas de idade corrigida) entre os sobreviventes apresentou menor significado estatístico [RR 0,34 (0,11; 1,05), RD –0,14 (–0,27; 0,00), NNT 7]; no entanto, esta redução não foi significativa nos recém-nascidos de extremo baixo peso.
Não foram verificadas diferenças significativas para falência do modo ventilatório, necessidade de curarização, patência do canal arterial, enfisema intersticial e leucomalacia periventricular.
Comparando as duas estratégias de volume corrente optimizado, o volume garantido (VG) associou-se a uma maior redução no tempo de ventilação e o volume controlado (PRVC) associou-se a uma maior redução da incidência de hemorragia intraventricular grave.
De qualquer modo, o número de estudos e crianças aleatorizadas foi pequeno e mais estudos serão necessários para confirmar o papel da ventilação com volume corrente optimizado na ventilação neonatal.
O baixo uso de VAFO [em quatro (14%) das unidades deste estudo] na doença das membranas hialinas do recém-nascido de extremo baixo peso provavelmente reflecte o resultado da metanálise de 15 estudos aleatorizados no recém-nascido pré-termo, comparando a VAFO e a ventilação convencional (IPPV, SIPPV e SIMV) iniciadas nas primeiras 24 horas de vida, tendo sido demonstrado não haver vantagem significativa da VAFO sobre a ventilação convencional, 11 não tendo sido demonstrado efeito significativo na mortalidade, alterações neurológicas a curto prazo, hemorragia intraventricular, leucomalacia periventricular e apenas uma modesta redução na displasia broncopulmonar nos sobreviventes. Há apenas um estudo aleatorizado relativo ao uso de VAFO no recém-nascido pré-termo com doença das membranas hialinas grave que demonstrou uma significativa diminuição de pneumotórax e enfisema intersticial; no entanto, demonstrou significativo aumento de hemorragia intraventricular32.
A maioria (79%) das unidades nacionais extuba o recém-nascido pré-termo após o desmame da ventilação invasiva, para NCPAP. Embora não tenha sido avaliado no inquérito, existe a noção de que o uso de NCPAP bifásico tem vindo a aumentar na neonatologia. A última revisão da Cochrane efectuada por De Paoli AG et al.12 com o objectivo de determinar que técnica de pressão e que tipo de interface nasal são mais eficazes na diminuição da reintubação após ventilação mecânica ou falência de NCPAP na fase aguda da doença das membranas hialinas, concluiu que o uso binasal de prongs é mais eficaz do que o uso de prong nasal único na prevenção da reintubação. Também a melhoria da função respiratória com prongs bilaterais sugere maior eficácia do que o uso de CPAP nasofaríngeo no tratamento da doença das membranas hialinas. Existe discrepância entre as diversas unidades na utilização de surfactante exógeno. De facto, ainda não está resolvida a questão de qual a estratégia mais adequada, isto é, qual o uso profiláctico de surfactante no pré-termo em risco de desenvolver doença das membranas hialinas versus uso curativo de surfactante na doença estabelecida33. Embora as metanálises dos estudos comparando ambas as estratégias do uso de surfactante tenham demonstrado maior benefício com o uso profiláctico34, a implementação desta estratégia promovida pela Vermont-Oxford Network, nas unidades filiadas na rede, não demonstrou benefício na diminuição da mortalidade, pneumotórax ou displasia broncopulmonar35.
É sabido que o surfactante exógeno melhora a oxigenação e diminui o risco de pneumotórax no recém-nascido pré-termo ventilado com doença das membranas hialinas. No entanto, há recém-nascidos de muito e extremo baixo peso que não desenvolvem doença das membranas hialinas. Jobe AH propõe uma avaliação clínica, seguida de uma intervenção adequada e orientada pelo estado clínico do doente33. Esta proposta parece mais sensata do que a aplicação de um protocolo rígido de NCPAP precoce ouintubação e administração de surfactante.
A monitorização contínua da pressão arterial de dióxido de carbono (PaCO2) não é utilizada por rotina na maioria das unidades portuguesas.
A medição transcutânea apresenta a desvantagem das possíveis queimaduras cutâneas provocada pelo eléctrodo e é mais frequentemente utilizada no recém-nascido de termo ou quase termo durante períodos de instabilidade, necessidade de rápidas modificações no suporte ventilatório, bem como com a VAFO, na qual súbitas variações na PaCO2 devem ser evitadas3.
A capnometria tem-se mostrado um método relativamente fiável de monitorização da PaCO2 através da medição do CO2 no ar expirado no recém-nascido de termo sem patologia pulmonar3. No recém-nascido pré-termo com volumes correntes pequenos, frequência respiratórias elevadas e patologia pulmonar, o valor de PCO2 no ar expirado avaliado por capnometria mostrou correlação com a PaCO2; no entanto, a magnitude desta correlação é limitada3,36,37.
A maioria (79%) das unidades referiu usar parâmetros de função respiratória na correcção da estratégia ventilatória, usando para esse efeito o monitor do ventilador. De facto, os ventiladores actuais incorporam monitorização da função pulmonar, fornecendo informação útil aos clínicos no ajuste dos parâmetros ventilatórios. Embora não exista clara evidência de que o uso dos testes de função pulmonar ou disposição gráfica dos sinais respiratórios melhore a evolução a curto ou longo prazo no recém-nascido pré-termo ventilado, a sua utilização não acarreta riscos e em mãos bem treinadas pode-se tornar um instrumento bastante útil. A sua utilização ajuda, também, a compreender e a demonstrar os efeitos das diferentes intervenções, bem como a interacção entre o doente e o ventilador38.
Este inquérito revelou que a maioria das unidades utiliza valores de saturação de oxigénio de 90%-95% na doença das membranas hialinas e 85%-90% na doença pulmonar crónica. Um estudo recente de Castillo A et al.39, com o objectivo de estabelecer uma relação entre PaO2 e saturação por oximetria de pulso durante as práticas de rotina nas unidades de cuidados intensivos neonatais, demonstrou que PaO2 elevadas (> 80 mmHg) ou baixas (< 40 mmHg) ocorrem raramente no recém-nascido em tratamento com oxigénio suplementar quando a saturação por oximetria de pulso é mantida entre os 85% e os 93%. Uma saturação por oximetria superior a 93% associou-se frequentemente a valores de PaO2 elevados (> 80 mmHg), valores considerados de risco no recém-nascido pré-termo. Em relação à doença pulmonar crónica da prematuridade, um estudo efectuado por Askie LM et al.40 demonstrou não haver benefício em termos de crescimento e alterações do desenvolvimento psicomotor em manter uma saturação entre os 95% e os 98%, em relação a manter uma saturação entre os 91% e os 94%. Inclusive, o grupo de recém-nascidos em que as saturações foram mantidas entre os 95% e os 98% apresentou maior período de dependência de oxigénio, aumentando os custos dos serviços de saúde.
Este estudo revelou que no recém-nascido não ventilado com necessidade de oxigenoterapia a modalidade de administração mais utilizada é o uso de oxigénio na incubadora.
Embora esta não seja a prática mais adequada, evita o desconforto causado pelas sondas, prongs nasais e campânula.
Ao analisar a informação fornecida relativamente a equipamentos de ventilação disponíveis nas diversas unidades de cuidados intensivos neonatais, parece-nos importante repensar a distribuição dos investimentos a nível nacional em equipamentos, em consumíveis e em recursos humanos.
Em conclusão, as estratégias de suporte ventilatório utilizadas na assistência ao recém-nascido de extremo baixo peso na maioria das unidades nacionais reflectem a evidência de estudos multicêntricos aleatorizados.
É necessário mais investimento no uso de NCPAP precoce, preferencialmente com prongs binasal, uso do modo SIPPV no desmame ventilatório, uso de estratégias ventilatórias com volumes correntes optimizados e utilização criteriosa de surfactante exógeno, de modo a assegurar a prática baseada na evidência.
Bibliografia/Bibliography
1. Avery ME, Mead J. Surface properties in relation to atelectasia and hyaline membrane disease. Am J Dis Child 1959; 17:517-523.
2. Fujiwara T, Maeta H, Chida S, Morita T, Watabe Y, Abe T. Artificial surfactant therapy in hyaline membrane disease. Lancet 1980:55-59.
3. Goldsmith JP, Karotkin EH. Introduction to assisted ventilation. In: Goldsmith JP, Karotkin EH (Eds.). Assisted ventilation of the neonate, fourth edition. Saunders Elsevier, Philadelphia 2003:1-14.
4. Liggins GC, Howie RN. A controlled trial of antepartum glucocorticoid treatment for prevention of the respiratory distress syndrome in premature infants. Pediatrics 1972; 50:515-525.
5. Daily WJR, Smith PC. Mechanical ventilation of the newborn infant: I. Curr Probl Pediatr 1971; 1:1-37.
6. Donald I, Lord J. Augmented respiration. Studies in atelectasis neonatorum. Lancet 1953; 1: 9-17.
7. Lorenz JM. The outcome of extreme prematurity. Semin Perinatol 2001; 25: 348-359.
8. Johnson AH, Peacock JL, Greenough A, Marlow N, Limb ES, Marston L et al, for the United Kingdom Oscillation Study Group. High frequency oscillatory ventilation for the prevention of chronic lung disease of prematurity. N Engl J Med 2002; 347:633-642.
9. Greenough A, Dimitriou G, Prendergast M, Milner A. Synchronized mechanical ventilation for respiratory support in newborn infants. Cochrane Database of Systematic Reviews 2008 (23) CD 000456. DOI: 10.1002/14651858. CD000456.pub3.
10. McCallion N, Davis PG, Morley CJ. Volume-targeted versus pressure-limited ventilation in the neonate. Cochrane Database of Systematic Reviews 2005, Issue 3. Art N.º: CD003666. DOI: 10.1002/14651858. CD003666.pub2.
11. Henderson-Smart DJ, Cools F, Bhuta T, Offringa M. Elective high frequency oscillatory ventilation versus conventional ventilation for acute pulmonary dysfunction in preterm infants. Cochrane Database Systematic Review 2007; 18(3): CD000104.
12. De Paoli AG, Davis PG, Faber B, Morley CJ. Devices and pressure sources for administration of nasal continuous positive airway pressure (NCPAP) in preterm neonates. Cochrane Database Systematic Review 2008; 23: CD 002977.
13. Jacobsen T, Gronvall J, Petersen S, Andersen GE. Minitouch treatment of very low birthweight infants. Acta Paediatr 1993; 82:934-938.
14. Subramaniam P, Henderson-Smart D, Davis PJ. Prophylactic nasal continuous positive airway ressure for preventing morbidity and mortality in very preterm infants. The Cochrane Database Systematic Reviews 2005, 20(3):CD001243.
15. Vanpee M, Walfridsson-Schultz U, Katz–Salamon M, Zupanicic JA, Pursley D, Jonsson B. Resuscitation and ventilation strategies for extremely preterm infants: a comparison study between two neonatal centers in Boston and Stockholm. Acta Paediatr 2007; 96:10-16.
16. Aly H, Massaro AN, Patel K, El-Mohandes AA. Is it safer to intubate premature infants in the delivery room? Pediatrics 2005; 115:1660-1665.
17. Baumer JH. International randomised controlled trial of patient triggered ventilation in neonatal respiratory distress syndrome. Arch Dis Child 2000; 82:F5-F10.
18. Beresford MW, Shaw NJ, Manning D. Randomised controlled trial of patient triggered and conventional fast rate ventilation in neonatal respiratory distress syndrome. Arch Dis Child 2000; 82:F14-F18.
19. Chen J-Y, Ling U -P, Chen J-H. Comparison of synchronized and conventional intermittent mandatory ventilation in neonates. Acta Paed Japon 1997; 39: 578-583.
20. Bernstein G, Mannino FL, Heldt GP, Callahan JD, Bull DH, Sola A, et al. Randomized multicenter trial comparing synchronized and conventional intermittent mandatory ventilation in neonates. J Pediatrics 1996; 128: 453-463.
21. Donn SM, Nicks JJ, Becker MA. Flow–synchronized ventilation of preterm infants with respiratory distress syndrome. J Perinatol 1994; 14: 90-94.
22. Chan V, Greenough A. Randomised controlled trial of weaning by patient triggered ventilation or conventional ventilation. Eur J Ped 1993; 152: 51-54.
23. Chan V, Greenough A. Comparison of weaning by patient triggered ventilation or synchronous mandatory intermittent ventilation. Acta Paediatrica 1994; 83: 335-337.
24a e 24b. Dimitriou G, Greenough A, Giffin FJ, Chan V. Synchronous intermittent mandatory ventilation modes versus patient triggered ventilation during weaning. Arch Dis Child Fetal Neonatal Ed 1995; 72:F188-F190.
25. Roze JC, Liet JM, Gournay V, Debillon T, Gaultier C. Oxygen cost of breathing and weaning process in newborn infants. Eur Respir J 1997; 10:2583-2585.
26. Reyes ZC, Claure N, Tauscher MK, D´Ugard C, Vanbuskirk S, Bancalari E. Randomised controlled trial comparing synchronized intermittent mandatory ventilation and synchronized intermittent mandatory ventilation plus pressure support in preterm infants. Pediatrics 2006; 118: 1409-1417.
27. Wood BR. Physiologic Principles. In: Goldsmith JP, Karotkin EH (Eds.). Assisted ventilation of the neonate, fourth edition. Saunders Elsevier, Philadelphia 2003: 15-40.
28. Keszler M, Abubakar K. Volume guarantee: stability of tidal volume and incidence of hypocarbia. Pediatr Pulmonol 2004; 38: 240-245.
29. Lista G, Colnaghi M, Castoldi F, Condo V, Reali R, Compagnoni G, et al. Impact of targeted-volume ventilation on lung inflammatory response in preterm infants with respiratory distress syndrome (RDS). Pediatr Pulmonol 2004; 37: 510-514.
30. Piotrowski A, Sobala W, Kawczynski P. Patient-initiated, pressure regulated, volume-controlled ventilation compared with intermittent mandatory ventilation in neonates: a prospective, randomised study. Intensive Care Med 1997; 23: 975-981.
31. Sinha S, Donn S, Gavey J, McCarty M. Randomised trial of volume controlled versus time cycled, pressure limited ventilation in preterm infants with respiratory distress syndrome. Arch Dis Child Fetal Neonatal 1997; 77: F 202-205.
32. HIFO Study Group. Randomised study of high-frequency oscillatory ventilation in infants with severe respiratory distress. J Pediatr 1993; 122: 609-619.
33. Jobe AH. Surfactant: The basis for clinical treatment strategies. In: Bancalari E, Polin RA, eds. The Newborn lung. Neonatology Questions and Controversies. Saunders Elsevier, Philadelphia 2008: 73-98.
34. Soll RF, Morley C. Prophylactic versus selective use of surfactant for preventing morbidity and mortality in preterm infants. The Cochrane Library, Issue 2. Oxford. Update Software; 2001.
35. Horbar JD, Carpenter JH, Buzas J, Soll RF, Suresh G, Bracken MB, et al. Collaborative quality improvement to promote evidence based surfactant for preterm infants: a cluster randomised trial. Br Med J 2004; 329: 1004.
36. Rocha G, Rocha A, Clemente F, Guedes B, Tavares M, Guimarães H. Valor limitado da capnometria em cuidados intensivos neonatais. Acta Ped Port 2002; 33; 329-333. [ Links ]
37. Bhat YR, Abhishek N. Mainstream end-tidal carbon dioxide monitoring in ventilated neonates. Singapore Med J 2008; 49: 199-203.
38. Gerhardt T, Claure N, Bancalari E. Role of pulmonary function testing in the management of neonates on mechanical ventilation. In: Bancalari E, Polin RA (Eds.). The newborn lung. Neonatology questions and controversies. First edition. Saunders Elsevier, Philadelphia 2008: 419-445.
39. Castillo A, Sola A, Baquero H, Neira F, Alvis R, Deulofeut R, et al. Pulse oxygen saturation levels and arterial oxygen tension values in newborns receiving oxygen therapy in the neonatal intensive care unit: is 85% to 93% an acceptable range? Pediatrics 2008; 121: 882-889.
40. Askie LM, Henderson-Smart DJ, Irwing L, Simpson JM. Oxygen-saturation targets and outcomes in extremely preterm infants. N Engl J Med 2003; 349: 959-967.
Agradecimentos
A todos os elementos das várias unidades participantes que se disponibilizaram para o preenchimento e envio do inquérito.
Unidades participantes no estudo
Região Norte
Centro Hospitalar da Póvoa de Varzim (Elisa Proença); Centro Hospitalar de Vila Nova de Gaia (Conceição Quintas); Hospital de São João, Porto (Gustavo Rocha); Hospital Central e Especializado de Crianças Maria Pia, Porto (Paula Rocha); Hospital Geral de Santo António, Porto (Paula Cristina Fernandes); Hospital de Pedro Hispano, Matosinhos (Teresa Martins); Hospital de São Marcos, Braga (Albina Silva); Hospital de São Pedro, Vila Real (Eurico Gaspar); Hospital Sr.ª de Oliveira, Guimarães (Clara Paz Dias, Fernando Graça); Hospital de Santa Luzia, Viana do Castelo (Beatriz Sousa); Hospital Padre Américo, Vale do Sousa (Ilídio Quelhas); Hospital de São Sebastião, Vila da Feira (Denise Schmit); Maternidade Júlio Dinis, Porto (Augusta Areias).
Região Centro
Hospital Infante Dom Pedro, Aveiro (Paula Rocha); Hospital Pediátrico de Coimbra (José Carlos Peixoto); Hospital de São Teotónio, Viseu (Isabel Andrade); Hospital de Santo André, Leiria (Lina Winckler); Maternidade Bissaya Barreto, Coimbra (Gabriela Mimoso).
Região Sul
Hospital Distrital de Santarém (José Onofre); CUF Descobertas, Lisboa (Graça Gonçalves); Hospital de Dona Estefânia, Lisboa (Micaela Serelha); Hospital de Santa Maria, Lisboa (Lincoln Silva); Hospital São Francisco Xavier, Lisboa (Ana Nunes); Hospital Dr Fernando da Fonseca, Lisboa (Rosalina Barroso); Maternidade Dr. Alfredo da Costa, Lisboa (Israel Macedo); Hospital do Espírito Santo, Évora (Hélder Ornelas); Hospital Distrital de Faro (Ermelinda Mendes).
Regiões autónomas
Hospital Distrital de Ponta Delgada (Fernanda Gomes); Centro Hospitalar do Funchal (José Luís Nunes).
* Comissão de Investigação Científica da Secção de Neonatologia da Sociedade Portuguesa de Pediatria/Portuguese Society of Paediatrics Neonatology Section Scientific
Research Committee
1 Serviço de Neonatologia, Hospital de São João, Porto/Neonatal Unit, Hospital de São João, Porto
2 Unidade de Neonatologia, Hospital de Santa Maria, Lisboa/Neonatal Unit, Hospital de Santa Maria, Lisboa
3 Unidade de Neonatologia, Maternidade Dr. Alfredo da Costa, Lisboa/Neonatal Unit, Maternidade Dr. Alfredo da Costa, Lisboa
4 Unidade de Neonatologia, Maternidade Júlio Dinis, Centro Hospitalar do Porto, Porto/Neonatal Unit, Maternidade Júlio Dinis, Centro Hospitalar do Porto, Porto
Correspondência/Correspondence to:
Gustavo Rocha
Serviço de Neonatologia, Departamento de Pediatria
Hospital de São João, Piso 2
Alameda Professor Hernâni Monteiro
4202-451 Porto
Telefone: 225512100, extensão/extension 1949
Fax: 225512273
e-mail: gusrocha@oninet.pt
Recebido para publicação/received for publication: 08.10.28
Aceite para publicação/accepted for publication: 09.05.18
Inquérito-Ventilação
Este inquérito, elaborado pela Comissão para a Investigação da Secção de Neonatologia da Sociedade Portuguesa de Pediatria, pretende conhecer as práticas correntes de suporte ventilatório neonatal e determinar se reflectem evidência de estudos aleatorizados. Deve ser preenchido por um ou mais médicos que responda(m) pelas práticas da UCIN (unidade de cuidados intensivos neonatais). Em caso de dúvidas, contactar um dos seguintes elementos:
Gustavo Rocha (HSJ–Porto)
Joana Saldanha (HSM – Lisboa)
Israel Macedo (MAC) – Lisboa)
Augusta Areias (MJD – Porto)
1. Que tipo(s) de ventilador estão disponíveis na sua unidade?
a. SLE 2000: sim 〈 não 〈
b. SLE 5000: sim 〈 não 〈
c. Draeger Babylog: sim 〈 não 〈
d. VIP Bird : sim 〈 não 〈
e. Stephanie: sim 〈 não 〈
f. Vyasis AVEA: sim 〈 não 〈
g. Sechrist: sim 〈 não 〈
h. Sensor Medics 3100 A (Oscilação Alfa Frequência): sim 〈 não 〈
outro: ___________________________
2. Que ventilador(es) usa mais frequentemente na ventilação de recém -nascidos (RN) pré-termo de extremo baixo peso (EBP, <1000g)?
3. Tem possibilidade de usar NCPAP (nasalCPAP) na sala de partos?
sim 〈 não 〈
4. Na sala de partos, na assistência ao pré-termo de EBP com alguma capacidade ventilatória, usa preferencialmente:
a. NCPAP: sim 〈 não 〈
b. TET (tubo endotraqueal) e ventilação convencional: sim 〈 não 〈
5. Tem possibilidade de efectuar o transporte do RN de EBP, da sala de partos para a UCIN, com NCPAP?
sim 〈 não 〈
6. Que modalidade ventilatória usa preferencialmente no transporte do RN de EBP da sala de partos para a UCIN?
a. NCPAP: sim 〈 não 〈
b. TET e ventilação convencional: sim 〈 não 〈
c. ventilação espontânea: sim 〈 não 〈
d. outra: especifique ______________________________________________________
7. Na assistência ao pré-termo de EBP na UCIN, usa preferencialmente:
a. NCPAP: sim 〈 não 〈
b. TET e ventilação convencional: sim 〈 não 〈
c. TET e ventilação por oscilação de alta frequência: sim 〈 não 〈
8. No RN de EBP com necessidade de ventilação mecânica, qual(ais) modalidade(s) que usa preferencialmente nas primeiras 24 horas de vida?
a. IPPV: sim 〈 não 〈
b. Alta frequência oscilatória: sim 〈 não 〈
c. SIPPV: sim 〈 não 〈
d. SIMV: sim 〈 não 〈
e. SIMV+PSV: sim 〈 não 〈
f. SIMV+ volume garantido: sim 〈 não 〈
g. PSV+ volume garantido: sim 〈 não 〈
h. SIPPV + volume garantido: sim 〈 não 〈
i. outra: (especifique p.f.): ____________________________________________
9. Na assistência ao pré-termo de EBP, usa preferencialmente:
a. surfactante profi láctico: sim 〈 não 〈
b. surfactante curativo: sim 〈 não 〈
10. Qual a(s) modalidade(s) de “desmame” que mais usa? (se usa mais de uma, p.f. assinale)
a. IPPV: sim 〈 não 〈
b. SIPPV: sim 〈 não 〈
c. SIMV: sim 〈 não 〈
d. SIMV+PSV: sim 〈 não 〈
e. SIMV+ volume garantido: sim 〈 não 〈
f. PSV+ volume garantido: sim 〈 não 〈
g. SIPPV + volume garantido: sim 〈 não 〈
h. CPAP nasal: sim 〈 não 〈
i. CPAP traqueal: sim 〈 não 〈
j. outra: (especifique p.f.): ____________________________________________
11. Que tipo(s) de CPAP nasal utiliza?
ventilador com modo CPAP: sim 〈 não 〈
Infant fl ow driver: sim 〈 não 〈
Modo(s) de aplicação do NCPAP:
Sonda endotraqueal: sim 〈 não 〈
Sonda faríngea: sim 〈 não 〈
Máscara nasal: sim 〈 não 〈
rongs nasais: sim 〈 não 〈
Outro: sim não ; qual: _____________________
12. Usa monitorização contínua de PaCO2?
sim 〈 não 〈;
se sim, qual método? medição transcutânea de CO2 : sim 〈 não 〈
capnometria: sim 〈 não 〈
13. Costuma usar valores de função respiratória para corrigir a estratégia ventilatória?
sim 〈 não 〈
se sim, qual (ais)?:
tidal volume: sim 〈 não 〈
pressão média (paw): sim 〈 não 〈
ventilação minuto: sim 〈 não 〈
curva de pressão: sim 〈 não 〈
curva de fluxo: sim 〈 não 〈
curva de pressão/volume: sim 〈 não 〈
curva de fluxo/volume: sim 〈 não 〈
compliance: sim 〈 não 〈
resistência: sim 〈 não 〈
constante de tempo: sim 〈 não 〈
se sim, usa o monitor do ventilador – sim 〈 não 〈
ou um monitor separado do ventilador – sim 〈 não 〈
14. No RN não ventilado, em oxigenoterapia, qual a modalidade de administração de O2 que utiliza?
Prong nasal: sim 〈 não 〈
Sonda nasolabial (bigode nasal): sim 〈 não 〈
O2 na incubadora: sim 〈 não 〈
O2 por campânula: sim 〈 não 〈
Outro: (especifique)______________________________
15. Que saturação de O2 usa no recém-nascido pré-termo com:
a. Doença membranas hialinas: 75 -80% 80 -85% 85 -90% 90 -95% 95 -98% outra: __________
b. Displasia broncopulmonar: 75 -80% 80 -85% 85 -90% 90 -95% 95 -98% outra: ___________
16. Na alta para o domicílio, tem experiência com:
a. alta com O2: sim 〈 não 〈
b. alta com ventilação invasiva: sim 〈 não 〈
c. alta com ventilação não invasiva: sim 〈 não 〈
17. Quantos recém-nascidos pré-termo < 1000g são admitidos, em média, anualmente na sua unidade?
18. Qual a % de displasia broncopulmonar (28 dias consecutivos de oxigenoterapia + necessidade de oxigenoterapia às 36 semanas de idade corrigida) nos RN pré-termo <1000g, sobreviventes, na vossa UCIN em 2007?
Obrigado pela participação.
Identificação da UCIN : _____________________________













