Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista Portuguesa de Pneumologia
versão impressa ISSN 0873-2159
Rev Port Pneumol v.15 n.4 Lisboa ago. 2009
Modelos experimentais em oncologia: O contributo da cultura de células para o conhecimento da biologia do cancro
Mariana Cruz 1
Margarida Enes 1
Marta Pereira 1
Ana Bela Sarmento Ribeiro 2, 4
Resumo
A cultura de tecidos surgiu no século xx (Harrison, 1907) para estudar o comportamento das células animais em ambiente homeostático e em situações de stress.
A capacidade de estudar as células a nível molecular relaciona-se com a forma como as células podem crescer e ser manipuladas em laboratório. A cultura de células in vitro permitiu estudar crescimento, diferenciação e morte celular e efectuar manipulações genéticas necessárias ao perfeito conhecimento da estrutura e funções dos genes.
A cultura de células estaminais humanas veio colmatar algumas limitações inerentes aos restantes modelos de cultura. Ao que parece, as células estaminais cancerígenas mantêm-se quiescentes nos locais metastáticos até serem activadas por sinais apropriados do microambiente.
Vários estudos revelaram que diferentes tipos de cancros podem surgir da transformação maligna de células estaminais. A eliminação destas células progenitoras tumorais é essencial para o desenvolvimento de novas abordagens terapêuticas mais eficazes em cancros agressivos. Por outro lado, a utilização de células dendríticas modificadas em cultura poderá contribuir para a produção de uma potencial vacina terapêutica eficaz para obter a regressão tumoral.
Palavras-chave: Cultura de células, oncologia, células dendríticas, terapêutica.
Experimental models in oncology: Contribution of cell culture on understanding the biology of cancer
Abstract
In the beginning of the 20th century, tissue culture was started with the aim of studying the behaviour of animal cells in normal and stress conditions. The cell study at molecular level depends on their capacity of growing and how they can be manipulated in laboratory. In vitro cell culture allows us the possibility of studying biological key processes, such as growth, differentiation and cell death, and also to do genetic manipulations essential to the knowledge of structure and genes function. Human stem cells culture provides strategies to circumvent other models’ deficiencies. It seems that cancer stem cells remain quiescent until activation by appropriated micro-environmental stimulation.
Several studies reveal that different cancer types could be due to stem cell malignant transformations. Removal of these cells is essential to the development of more effective cancer therapies for advanced disease. On the other hand, dendritic cells modified in culture may be used as a therapeutic vaccine in order to induce tumour withraw.
Key-words: Cell culture, oncology, dendritic cells, therapy.
Introdução histórica
No século xix, Sydney Ringer, ao desenvolver soluções salinas capazes de assegurar as necessidades vitais de órgãos isolados do organismo, lançou as bases do que viria a ser a cultura de células. Todavia, foi Wihelm Roux quem conseguiu pela primeira vez, em 1885, manter vivas durante vários dias células embrionárias isoladas de pinto numa solução salina aquecida1.
No início do século xx, Ross Harrison planeou e aplicou a metodologia da cultura de tecidos, de modo a estudar o comportamento das células animais quando livres das restrições impostas pelo ambiente em que naturalmente existem em condições de homeostasia, mas tam bém sob o stress de uma experiência laboratorial. Estas técnicas, inicialmente aplicadas a fragmentos de tecidos sólidos, sofreram avanços significativos nas décadas de 40 e 50, altura em que a cultura de células previamente dispersadas passou a ter grande divulgação, impulsionadas pelas pesquisas em virologia devido à necessidade de produzir vacinas antivirais em larga escala, nomeadamente com a vacina Polio Salk, mas também pelas pesquisas iniciadas em oncologia, dada a crescente necessidade de um conhecimento mais profundo nesta área2.
Cultura de células
Princípios básicos
Há algumas décadas, a cultura de células era vista como algo esotérico, cuja finalidade e aplicabilidade práticas não se conseguia adivinhar. Actualmente, é uma técnica largamente reconhecida e rotineiramente utilizada no laboratório, particularmente em investigação.
Para o sucesso da cultura de células, o cumprimento das regras e cuidados de assepsia é fundamental, uma vez que cerca de 70% dos problemas que surgem são devidos a contaminações3.
A cultura de células animais (cultura de tecidos ou de células sanguíneas/hematopoiéticas ou outras) inicia-se pela dispersão das células obtidas a partir de um fragmento de tecido (hematopoiético, muscular, epitelial ou outro) num meio nutritivo apropriado, colocado em frasco ou placa de cultura, após o que se verifica que a maioria das células adere à superfície sólida e cresce em monocamada ou em suspensão. A obtenção de uma população ou cultura de células é possível de várias formas, das quais se indicam duas:
– Crescimento ou migração de células de um fragmento de tecido – onde a selecção se baseia na capacidade virtual de as células migrarem da amostra de tecido;
– Dispersão celular – cuja selecção resulta da capacidade de as células sobreviverem à metodologia aplicada e que pode ser a desagregação enzimática ou mecânica do tecido.
Comparativamente ao primeiro método, a dispersão celular, apesar de mais trabalhosa, permite obter, em menos tempo, um maior número de células representativas de todo o tecido3.
Para a desagregação enzimática a tripsina é a enzima mais usada, uma vez que é bem tolerada pela maioria das células e eficaz na maioria dos tecidos e a sua actividade residual pode ser neutralizada pelo soro do meio de cultura ou por um inibidor sintético adicionado.
As desvantagens deste método são sobretudo a possível lesão celular e a eventual ineficácia em determinados tecidos, particularmente quando apresentam matriz rica em colagénio e fibrose, sendo necessário, neste caso, utilizar outras enzimas, como a colagenase, a pronase e a dispase, isoladas ou em associação3.
A desagregação mecânica pode ser feita por compressão das células contra uma peneira com malha de diâmetro sucessivamente menor, passando as células através de uma seringa e agulha ou simplesmente pipetando repetidamente. Esta técnica tem a vantagem de ser mais rápida do que a dissociação enzimática, embora cause mais lesões mecânicas às celulas3.
A cultura de células pode ser feita em monocamada ou em suspensão. Na cultura em monocamada, as células vão aderir a um substrato e propagam-se. É o método mais usado e tem como condição essencial a adesão ao substrato, ancoragem. Esta dependência da ancoragem é um pré-requisito indispensável à proliferação celular, nesta metodologia. A cultura em suspensão é usada para células que sobrevivem e proliferam sem necessidade de adesão (independente da ancoragem). É o caso das células hematopoiéticas, das linhas celulares transformadas ou das células derivadas de alguns tumores malignos de órgãos sólidos3.
A Fig. 1 resume a forma de obtenção de culturas celulares primárias e secundárias (linhas celulares) a partir de um fragmento de tecido. Uma cultura celular secundária é uma linha celular resultante da manutenção da cultura celular primária.
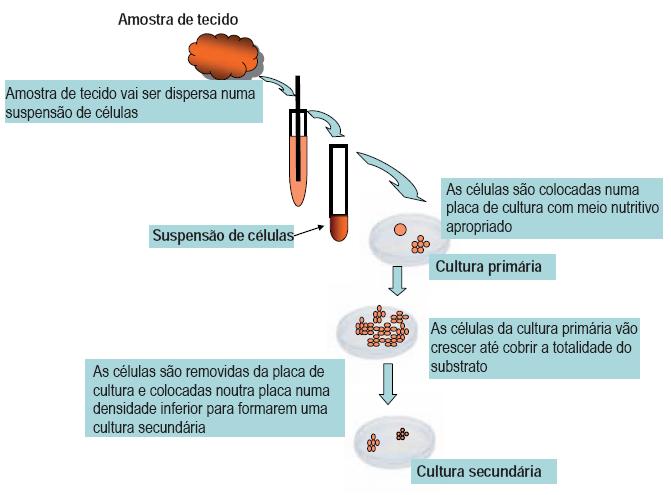
Fig. 1 – Obtenção de uma linha celular a partir de um tecido. As células obtidas por desagregação do tecido são colocadas em cultura com os nutrientes adequados (cultura primária). Posteriormente, são feitas subculturas com baixa densidade celular para obter culturas secundárias e estabelecer uma determinada linha celular
Quando a cultura primária se mantém por algumas horas, as células com capacidade de proliferar aumentam em número, enquanto as que não sobrevivem às condições usadas morrem; outras há que sobrevivem, mas não proliferam. Assim que toda a camada de substrato da cultura for ocupada e as células confluírem, estabelecendo contacto umas com as outras, surge a necessidade de proceder a subculturas sucessivas.
Nestas, a fracção de crescimento é mais elevada, ocorrendo a selecção de células com capacidade proliferativa em detrimento das outras, que são eliminadas. Assim, de uma cultura muito heterogénea, contendo vários tipos de células do tecido original, emerge uma linha de células mais homogénea. Obtém-se desta forma uma linha celular por subcultura de uma cultura primária, à qual é necessário renovar periodicamente o meio de cultura. Quando apenas é seleccionada uma linhagem celular, designa-se por célula strain3.
Para a manutenção das células em cultura é necessário que a incubação ocorra numa atmosfera apropriada e controlada quanto à temperatura, à humidade e à composição da fase gasosa. A maioria requer uma atmosfera pobre em oxigénio, embora variável de acordo com as necessidades específicas das células em causa. A concentração de CO2, superior à da atmosfera normal, é igualmente fundamental para o sucesso das culturas celulares, sendo frequentemente necessário adicionar este gás à atmosfera em que as células se encontram3.
O meio de cultura escolhido é igualmente fundamental e indispensável, uma vez que é este que fornece nutrientes, hormonas, factores de crescimento e outros substratos essenciais à expressão de funções especializadas das células, sustentando o seu crescimento contínuo, substituindo e reproduzindo, o melhor possível, as condições in vivo, uma vez que as culturas de células se apresentam como alternativa aos estudos em modelos animais, reproduzindo in vitro as condições in vivo 3.
Diferenciação celular
As primeiras células de um embrião são células estaminais totipotentes, com a capacidade de originar todas as células do organismo.
Estas células primordiais vão diferenciar–se em células multipotentes, com diferenciação mais restrita, que dão origem a células estaminais teciduais. Todas as células estaminais têm a capacidade de se dividir, originado células estaminais adicionais e células comprometidas com a diferenciação; estas últimas podem eventualmente parar de se dividir e entrar em apoptose4,5. Assim, todas as células do nosso organismo têm origem em células estaminais organoespecíficas que se diferenciam nos tipos celulares que compõem cada órgão. Estas células estaminais tecidoespecíficas distinguem-se das células estaminais embrionárias pelo facto de a sua diferenciação ficar limitada aos tipos celulares de um determinado órgão (Fig. 2)3.
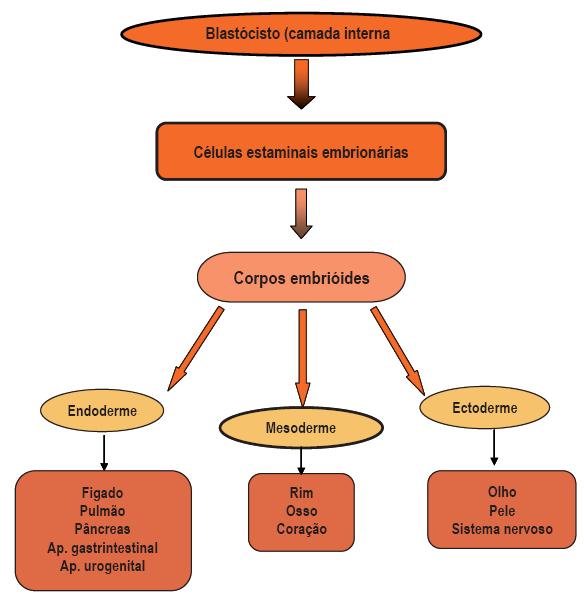
Fig. 2 – Diagrama esquemático das possíveis vias de diferenciação das células estaminais embrionárias (cee). As cee podem dar origem a três camadas germinativas, endoderme, mesoderme e ectoderme, durante o desenvolvimento embrionário. Destas camadas vão originar-se as células que constituem os tecidos/órgãos do organismo.
(Adaptado e modifi cado de Mimeault M, et al., 2006 )
A diferenciação celular é o processo que conduz à expressão fenotípica das propriedades que caracterizam uma célula madura in vivo, a partir duma célula indiferenciada. Este processo nem sempre está completo ou é irreversível. Além disso, com a diferenciação, a capacidade de divisão celular diminui.
No entanto, em muitas células estes dois processos são incompatíveis, o que porém não acontece em alguns tipos de células tumorais3.
O compromisso com determinada diferenciação implica a progressão inexorável de uma célula estaminal para uma linha celular definida e particular e, portanto, com um potencial de diferenciação limitado3. Alguns estudos recentes comprovam que algumas células estaminais adultas podem dar origem a tecidos distintos daqueles de onde foram obtidas, desde que as condições experimentais sejam particulares. Este processo designa-se por transdiferenciação3.
A diferenciação terminal reflecte o processo segundo o qual a célula progrediu para uma linhagem particular até ao momento em que o fenótipo maduro se encontra estabelecido, e a partir do qual não é possível progredir mais. A desdiferenciação corresponde à perda irreversível das características fenotípicas de uma célula madura. Refere-se à perda da diferenciação do tecido, tal como sucede quando este se torna maligno ou cresce em cultura, tratando-se de um fenómeno adaptativo3.
Identificação celular
Muitas funções celulares especializadas são igualmente expressas in vitro, o que é de grande relevo na cultura de células. De facto, se as propriedades das células diferenciadas em cultura forem perdidas, torna–se complicado relacionar essas células com as células funcionais do tecido de onde foram extraídas. É necessário usar marcadores estáveis.
A identidade de uma cultura é definida pela sua linhagem in vivo, isto é, hematopoiética, glial, entre outras, mas também pelo seu estádio de diferenciação (posição na linhagem), ou seja, se é célula estaminal, célula precursora de linhagem tissular ou célula madura diferenciada. A fonte da cultura também determina o tipo de componentes tissulares/celulares que devem estar presentes.
Assim, linhas celulares derivadas de tecido embrionário devem conter células estaminais e células precursoras de linhagem e serem capazes de um maior nível de autorenovação do que as culturas derivadas de tecido adulto3.
Ao contrário da cultura de células, a cultura de órgãos tem oferecido grandes dificuldades relacionadas sobretudo com a impossibilidade prática de se reproduzir um elevado número de culturas idênticas e pela heterogeneidade da amostra, essencial para a manutenção do fenótipo do tecido. A realização destas culturas exige um elevado nível de conhecimento e experiência, grande dispêndio de meios e de material para produção de pequenas quantidades de tecido com elevada instabilidade celular. Por estas razões, recorre-se geralmente à cultura de células. No entanto, as culturas de órgãos têm vantagens relativamente aos estudos in vivo, nomeadamente quanto ao controlo do ambiente envolvente, à caracterização e à homogeneização da amostra e ao custo inferior3.
A alteração de uma cultura celular, que dá origem a linhas celulares contínuas e imortalizadas, é designada por transformação in vitro, e pode ocorrer espontaneamente, ser induzida quimicamente ou recorrendo a vírus.
Este processo está, contudo, associado a um aumento da tumorigénese. De facto, a maioria das células de linhas contínuas tem propriedades idênticas às das células malignas, como por exemplo a diminuição da necessidade de factores de crescimento3.
Aplicações da cultura de células em oncologia
Cultura de células estaminais
A cultura de células estaminais humanas, apesar de levantar questões éticas e legais, vem colmatar algumas limitações inerentes aos restantes modelos de cultura de células.
Contudo, a aplicação das pesquisas efectuadas com estas células nos diferentes campos da medicina, desde a prevenção ao diagnóstico, passando pelo tratamento, obriga a que se aprofundem os conhecimentos sobre as suas propriedades biológicas5.
As células estaminais são células indiferenciadas, com capacidade de divisão e renovação ilimitada, que podem originar várias linhas celulares, ou células progenitoras de linhagem, contribuindo assim para a homeostasia celular e para a reparação tecidular após uma lesão. Assim, dão origem a células estaminais adicionais, de forma a manter o seu pool e a células-filhas comprometidas com a diferenciação nos vários tipos celulares do organismo4. Estudos efectuados em embriões permitiram identificar diferentes tipos de células estaminais existentes em tecidos fetais, no sangue do cordão umbilical e em nichos celulares específicos de muitos tecidos/órgãos de mamíferos adultos; exemplos destes locais são a medula óssea, o cérebro, o olho, a pele, o coração, os rins, o tubo digestivo, o pâncreas, o fígado, a mama, os ovários, a próstata, os testículos e o pulmão6.
No entanto, as células estaminais com potencial mais abrangente são as embrionárias. Estas células derivam da massa interna do blastócisto e vão dar origem aos 276 tipos de células diferentes do corpo humano. São células pluripotentes, e não totipotentes, como é o caso do zigoto.
À medida que o desenvolvimento do organismo evolui, o potencial pluripotente diminui, ficando consignado ao tecido de onde as células provêm, que se diferenciam preferencialmente em células do mesmo7, 8.
Algumas células estaminais, como as hematopoiéticas, têm uma elevada taxa de replicação, de forma a assegurarem um número elevado de leucócitos, eritrócitos e plaquetas. Já as células estaminais da pele e do cólon, por exemplo, apresentam um crescimento mais lento, mas constante. Há outras, nomeadamente as células estaminais adultas, que se mantêm quiescentes por períodos de tempo mais ou menos longos, tornando-se activas quando estimuladas por hormonas/factores de crescimento ou por lesão dos tecidos4, 6.
Em virtude das diferentes propriedades que caracterizam os vários tipos de células estaminais, temos que considerar as vantagens e as desvantagens da sua utilização em cultura. As vantagens das células estaminais embrionárias são: possibilidade de se isolar uma população celular pura com pluripotência e crescimento indefinido, onde a elevada expressão de telomerases é uma evidência6.
As desvantagens que apresentam são: a presença de marcas imunológicas do tecido/órgão dador, a necessidade de se controlar o crescimento para evitar o aparecimento de clones celulares malignos, a necessidade de se controlar a diferenciação ao longo da via apropriada e a expressão de genes embrionários/fetais3, 7, 8.
Por outro lado, as células estaminais somáticas podem ser utilizadas para transplantes autólogos sem reacção imunológica, expressam genes adultos, têm capacidade de desdiferenciação em células pluripotentes e apresentam desenvolvimento plástico/flexível.
As grandes desvantagens destas células estaminais relacionam-se com a difícil obtenção de populações celulares puras, a ausência de crescimento indefinido in vitro, a capacidade de desencadearem reacções alogénicas e a dificuldade de manutenção num estado indiferenciado em cultura durante longos períodos
de tempo. Este último aspecto dificulta a sua utilização com objectivos terapêuticos, em virtude da senescência celular3, 7, 8.
As células estaminais podem ser obtidas a partir do sangue do cordão umbilical, da medula óssea e do sangue periférico, sendo este último método o mais utilizado actualmente.
Apesar de a colheita a partir da medula óssea ser a mais invasiva, é, em contrapartida, a que permite obter maior quantidade de células estaminais3, 9.
O sangue do cordão umbilical tem a vantagem de conter maior número de células hematopoiéticas por unidade de volume, comparativamente com o sangue periférico e a medula óssea. A colheita, feita após o nascimento, é indolor e sem risco, quer para o recém-nascido quer para a mãe, e as células estão imediatamente disponíveis para transplante. Este método está associado a menor incidência de doença aguda do enxerto contra hospedeiro, a maior tolerância em termos de compatibilidade HLA e a menor risco de complicações infecciosas9.
A colheita de células estaminais do sangue periférico tem a vantagem de ser um método pouco invasivo e que permite contornar o pequeno número de células existentes em circulação pela colheita de maior quantidade de sangue e/ou cultura das células. Outra possibilidade de aumentar o número de células estaminais no sangue periférico é a sua mobilização, à periferia, da medula, por acção de factores de crescimento3.
A utilização de células estaminais no tratamento de múltiplas doenças, a terapia celular, tem sido particularmente interessante em várias áreas médicas e oncológicas em geral3, 7, 8, 10.
A utilização de células estaminais na investigação, quer em investigação básica, quer aplicada, tem permitido o estudo dos factores e mecanismos genéticos que determinam a diferenciação celular e a especialização dos tecidos. Permite ainda a identificação da origem bioquímica e molecular de algumas
doenças resultantes da divisão celular anormal ou da deficiência nos mecanismos de diferenciação. A sua utilização tem permitido também o desenvolvimento de novos fármacos dirigidos aos defeitos celulares e moleculares e, neste sentido, podem ainda ser usadas como modelos celulares para testar o efeito ou a toxicidade de fármacos, quer em substituição quer como complemento dos sistemas in vitro, ou dos modelos animais3.
Cultura de células tumorais
A cultura de células tumorais, sobretudo no caso de tumores humanos espontâneos, apresenta problemas semelhantes aos da cultura de células especializadas do tecido normal. As células tumorais têm que ser separadas das células do tecido conjuntivo normal, preferencialmente usando um meio de cultura apropriado para células neoplásicas. Esta dificuldade acentua-se quando o propósito é cultivar um tipo específico de células.
De facto, as neoplasias são geralmente compostas por uma grande variedade de células, tornando assim mais difícil a representatividade de reprodutibilidade da amostra.
O problema da selectividade é particularmente importante quando as amostras são recolhidas de metástases secundárias. Estas, apesar de crescerem melhor, podem não ser representativas do tumor primário ou mesmo das outras localizações secundárias do tumor. No entanto, as características dos tumores com uma grande autonomia e capacidade de dar origem a linhas celulares imortais fazem com que seja possível uma vasta investigação, independentemente da incerteza quanto à relação entre o tumor estudado e aquele que lhe deu origem3.
É provável que uma parte das células neoplásicas em cultura tenha uma esperança média de vida limitada devido a alterações genéticas de novo, à diferenciação terminal ou à senescência natural. Além disso, a diluição da cultura, ao reduzir o número de células e, consequentemente, a interacção celular, pode comprometer a sua sobrevivência.
Por outro lado, a capacidade letal do tumor relaciona-se com a sua capacidade de infiltração e de crescimento descontrolado, que pode residir num pequeno grupo de células estaminais transformadas, tão pequeno que a diluição subsequente à remoção do tecido original impeça a sua sobrevivência3.
Por outro lado, o cancro resulta da desregulação da proliferação e da apoptose, bem como da falência dos mecanismos reguladores da diferenciação celular normal. Há evidências de uma relação inversa entre a capacidade de diferenciação e o grau de malignidade, facto que justifica a aplicação de medidas terapêuticas que induzem as células tumorais a diferenciar-se. Aparentemente, as células tumorais podem manter a capacidades de responder a indutores de diferenciação, o que nem sempre se verifica em células normais.
Uma vez que as células tumorais são capazes de se diferenciarem in vitro, é de certa forma inesperado que não o façam in vivo, a não ser que o processo de diferenciação não esteja completo e continue a ser possível. Outra explicação relaciona-se com a existência de um compartimento de células estaminais insensíveis ao feedback inibitório ou outras formas de regulação, resultando numa proliferação descontrolada, independentemente da diferenciação celular3.
Neste sentido, a contribuição de vários estudos utilizando a cultura de células tem sido uma ferramenta importante, ou pelo menos complementar, na clínica oncológica. De facto, este modelo experimental tem permitido o estudo dos mecanismos moleculares envolvidos na carcinogénese e a identificação de marcadores de diagnóstico e prognóstico, úteis para a decisão terapêutica (por exemplo, o receptor Herb-2 e o cancro da mama, a translocação 9,22 e a LMC e a LLA, as mutações no receptor do factor de crescimento da epiderme [EGF-R] e o cancro do pulmão)3, 10.
Todavia, para que a cultura de células seja aceite como uma fonte de marcadores de prognóstico e da eficácia terapêutica, têm que se considerar diversas regras. Assim, é importante a standardização dos métodos usados, as várias análises, a definição precisa dos subgrupos de doentes e a definição dos objectivos, bem como das condições económicas e logísticas3.
Somente desta forma se pode aceitar a cultura de células como modelo útil para a investigação de novos marcadores de diagnóstico, orientação terapêutica e avaliação do prognóstico de inúmeras patologias do foro oncológico3.
Cultura de células tumorais em pneumologia
O cancro do pulmão é um problema importante de saúde pública mundial, sendo responsável por uma das maiores taxas de mortalidade por cancro em ambos os sexos.
No carcinoma pulmonar de não pequenas células (CPNPC), o tipo de cancro pulmonar que apresenta a maior tendência para metastizar e recidivar, uma das principais razões para a elevada mortalidade é o facto de o diagnóstico ser efectuado num estádio avançado da doença, o que, associado às comorbilidades relacionadas com a idade dos doentes (mais de 50% tem mais de 65 anos e cerca de 30% mais de 70 anos aquando do diagnóstico), condiciona a eficácia e a tolerabilidade à quimioterapia actualmente disponível11,12.
O desenvolvimento de técnicas e metodologias que facilitem o diagnóstico precoce e, ao mesmo tempo, a orientação da terapêutica para alvos moleculares de forma mais individualizada/personalizada, constituirá um progresso substancial no combate a este tipo de cancro, com benefícios claros na sobrevivência e na qualidade de vida dos doentes11,13.
A cultura de células poderá constituir um valioso auxiliar à prática clínica em pneumologia oncológica, uma vez que permitirá o conhecimento e a compreensão das alterações genéticas e do comportamento biológico do cancro do pulmão. Abre-se, assim, caminho à identificação de marcadores moleculares de diagnóstico, à identificação de novos alvos terapêuticos e ao desenvolvimento de novos fármacos, dirigidos especificamente às vias de transdução de sinal intracelular, relacionadas com a proliferação, a diferenciação e a morte celular das células cancerosas14,15,16.
A sobreexpressão do receptor do factor de crescimento epidérmico (EGFR), frequente em diversas neoplasias malignas sólidas, onde está implicada na proliferação celular, na angiogénese e na metastização, é comum no CPNPC e relaciona-se com a resistência à quimioterapia e ao mau prognóstico, pelo que é um alvo terapêutico importante no tratamento desta patologia17.
A cultura de células de linhas celulares de CPNPC tem-se mostrado um modelo muito útil para estudar a acção e a resposta a novos agentes terapêuticos, como aos inibidores da tirosina quinase (ITC), particularmente o anti-EGFR erlotinib, aprovado em 2004 pela em 2005 pela Agência Europeia de Medicamentos, para o tratamento de CPNCP em estádios avançados, após pelo menos uma linha de quimioterapia. A mesma metodologia revela-se igualmente útil para estudos relacionados com a resistência à quimioterapia e a identificação de novas abordagens diagnósticas, facilitando também o estadiamento e o planeamento da terapêutica com maior exactidão13,18,19.
A cultura de células tem também sido de grande utilidade em estudos de metastização. Como é sabido, o desenvolvimento e o crescimento dos tumores sólidos está dependente da neoangiogénese, um processo iniciado pela libertação de factores pró-angiogénicos pelo próprio tumor20. Deste modo, a inibição deste processo constitui uma estratégia terapêutica-chave e uma promessa de optimismo para o tratamento do cancro do pulmão. Os estudos efectuados recorrendo ao modelo da cultura de células permitiram identificar os mecanismos de acção, com elevada especificidade, no processo da angiogénese de várias moléculas, algumas das quais estão já aprovadas para o tratamento destes cancros, como por exemplo o anticorpo monoclonal Bevacizumab20.
Cultura de células dendríticas
As células dendríticas (CD) são células apresentadoras de antigénio. Um dos principais papéis destas células é o processamento e a apresentação de antigénios a outras células do sistema imunitário, um passo crucial no desenvolvimento de uma resposta imunitária adequada, desencadeando a activação de células T, cujo receptor é específico para o antigénio particular que está a ser apresentado.
A resposta imunitária resultante, mediada pelos linfócitos T citotóxicos, é o principal meio pelo qual as células tumorais podem ser destruídas pelo organismo, uma vez que produzem antigénios que podem ser reconhecidos e destruídos por este mecanismo.
A ideia de utilizar o sistema imunitário como arma contra o cancro tem motivado múltiplos trabalhos de investigação nas últimas décadas. Actualmente explora-se a administração de células dendríticas modificadas em cultura como uma potencial vacina terapêutica para obter regressão tumoral, isoladamente ou em combinação com as terapêuticas actuais.
Na sua maioria, estas vacinas são produzidas a partir de células, obtidas por recolha de sangue periférico, posteriormente cultivadas e expostas a antigénios tumorais21,22,23.
Os antigénios tumorais variam substancialmente entre os diferentes tipos de cancro e para cada doente em particular. O que se pretende é criar uma vacina a partir de antigénios tumorais específicos de um doente, assegurando que a resposta imunitária, se ocorrer, seja dirigida às células tumorais desse indivíduo. A eficácia será tanto maior quanto mais precisa for a relação entre a vacina e o hospedeiro21.
Actualmente, há três métodos para expor as CD aos antigénios tumorais ex-vivo:
– Peptide-pulsing utilizando antigénios isolados, determinados previamente; é o método mais directo;
– Exposição das CD aos fragmentos das células tumorais do próprio doente, o que permite o contacto com todos os antigénios existentes;
– Fusão ex-vivo das CD com as células tumorais do doente, ultrapassando o processo de ingestão e colocando à disposição da célula apresentadora todos os antigénios contidos na célula tumoral21,22.
O recurso a células tumorais (por fusão ou após lise) como fonte de antigénios é preferível à utilização de antigénios tumorais definidos, uma vez que aumenta a probabilidade de um maior número de células do tumor ser reconhecido e destruído23, 24.
Para além dos métodos que expõem as CD ao antigénio directamente, também é possível transferir os genes que codificam aos antigénios específicos do tumor. Assim, consegue-se uma produção e uma disponibilidade contínuas de peptídeos antigénicos, através de uma fonte intracelular. Isto obtém-se pela transferência do ARN tumoral ou pela utilização de vectores virais21,22,25-28.
Os adenovírus são usados frequentemente, podendo também recorrer-se aos poxvírus, herpes vírus e lentivírus, entre outros. Neste caso, o vírus infecta as CD, inserindo nestas o gene desejado, permitindo a produção e a apresentação contínua do antigénio. A eficácia pode ser aumentada se o vector viral for simultaneamente utilizado para transferir genes que codificam citocinas estimuladoras dos linfócito T citotóxicos, como a IL12 e a IL 222.
Estes métodos têm sido utilizados na produção de vacinas, de uso experimental, para linfomas, melanomas, gliomas malignos, carcinomas da próstata, de células renais, carcinoma da mama, do pâncreas, colorrectal e carcinoma do pulmão de pequenas células.
Apesar de resultados preliminares ainda pouco significativos, tem-se verificado um aumento moderado da sobrevida e da qualidade de vida em muitos casos, com ausência de efeitos secundários relevantes22,23,26,28-36.
Em resumo, podemos afirmar que há ainda muitas limitações ao uso generalizado destas vacinas, que impedem o seu sucesso absoluto.
Em muitos casos, não se identificou ainda um antigénio tumoral eficaz, ou não é possível colher a quantidade de tecido tumoral suficiente para a preparação antigénica33.
O fenómeno de escape tumoral ocorre por selecção natural das células neoplásicas, altamente mutagénicas, que conseguem escapar ao sistema imunitário. É provável que, nestas condições, respondam de forma anómala, o que, entre outros efeitos, pode provocar a autodestruição dos linfócitos10.
É portanto necessário prosseguir os estudos e melhorar as técnicas, para que a produção de vacinas terapêuticas a partir de cultura de células dendríticas possa vir a ser, com sucesso, uma rotina no tratamento do doente oncológico37.
Em conclusão, por tudo o que foi exposto, podemos afirmar que o desenvolvimento de modelos experimentais utilizando a cultura de células tem dado um importante contributo para a melhor compreensão da oncogénese, nomeadamente no cancro do pulmão, permitindo um diagnóstico precoce e a instituição de terapêuticas dirigidas e mais eficazes. Contudo, para que a técnica da cultura de células possa ser aceite na prática clínica como uma ferramenta útil e capaz de fornecer informações de valor diagnóstico, e sobretudo o prognóstico para o desenvolvimento de novas terapêuticas em oncologia, têm de ser cumpridas várias regras, entre elas a standardização dos métodos, dos grupos de doentes a análise e das condições logísticas, sem esquecer as económicas. Só assim a cultura de células poderá constituir um modelo útil em oncologia.
Bibliografia
1. Bruce Alberts, Bray D, Lewis J. Biologia molecular da célula. 3.ª edição; Porto Alegre. Editora Artes Médicas, 1997.
2. Susan Lindee M. The culture of cell culture. Science 2007; 316(5831):1568-1569.
3. R. Ian Freshney. Culture of animal cells – A manual of basic technique. Second edition. Alan R Liss, Inc.; New York, 1987.
4. Michael Dean. Cancer stem cells: redefining the paradigm of cancer treatment strategies. Molecular Interventions 2006; 6:140-148.
5. Stem cells and the future of regenerative medicine – Free executive summary. 2002; National Academy of Sciences. http://www.nap.edu/catalog/10195.html.
6. Murielle Mimeault, Batra Surinder K. Concise Review. Recent advances on the significance of stem cells in tissue regeneration and cancer therapies. Stem cells 2006; 24(11): 2319-2345.
7. Tannishtha Reya, Morrison SJ, Clarke MF, Weissman IL. Stem cells, cancer and cancer stem cells. Nature 2001; 414:105-111.
8. Cedar SH. The function of stem cells and their future roles in health care. Br J Nurs 2006;15(2):104-107.
9. Margarida Vieira, Gomes A, Castelo-Branco G, Santos R. Células estaminais em obstetrícia e ginecologia, Parte I: conceitos gerais e aplicações. www.crioestaminal.pt/web/eng/pdfs.
10. Monica L Guzman, Jordan CT. Considerations for targeting malignant stem cells in leukemia. Cancer Control 2004;11:97-104.
11. Socinski MA, Crowell R, Hensing TE, et al. Treatment of non small cell lung cancer stage IV – ACCP Evidence Based Pratice Guidelines. Chest 2007; 132: 277-89.
12. Barata F, Costa T, Figueiredo A. Erlotinib e matástases cerebrais. Rev Port Pneumol 2008; XIV(supl 3):S35-S42. [ Links ]
13. Philip C Hoffman, Mauer AM, Vokes EE. Lung cancer. Lancet 2000;355:479-485.
14. Ana Ferreira Alves, Liebermann M. Inibidores da tirosina-cinase no CPNPC avançado: A propósito de um caso clínico. Rev Port Pneumol 2008;14(supl 3):S23-S28. [ Links ]
15. NCCN Clinical Practice Guidelines in Oncology. Non-Small Cell Lung Cancer. Version 2. 2008.
16. Kim ES, et al. Epidermal growth receptor biology (IMC-C225). Cur Op Onc 2001;13(6):506-513.
17. Teresa Guimarães, Castro A, Cortesão N, Ferreira J, João F. Erlotinib no controlo tumoral prolongado do carcinona do pulmão de não pequenas células avançado (CPNPC). Rev Port Pneumol 2008;14(supl 3):S9-S15. [ Links ]
18. Chin TM, Quinlan MP, Singh A, Sequist LV, Lynch TJ, Haber DA, Sharma SV, Settleman J. Reduced erlotinib sensitivity of epidermal growth factor receptor-mutant non-small cell lung cancer following cisplatin exposure: A cell culture model of second-line erlotinib treatment. Clin Cancer Res 2008; 14(21):6867-6876.
19. Araújo A, Soares M, Azevedo I, Araújo A. Erlotinib na segunda linha de tratamento do cancro do pulmão de não pequenas células – Caso clínico. Rev Port Pneumol 2008;14(supl 3):S17-S22. [ Links ]
20. Roy S Herbst, Onn A, Sandler A. Angiogenesis and Lung Cancer: Prognostic and therapeutic implications. J Clin Oncol 2005;23:3243-3256.
21. Jonathan M Ng. Designing a Vaccine for cancer: a look into dendritic cell cancer vaccine. McMaster Educater 2004; 3:13-18.
22. Mulé JJ. Dendritic cell-based vaccines for the treatment of cancer. Michigan Oncology Journal, Summer 1998.
23. Kyte JA, Gaudernack G. Immuno-gene therapy of cancer with tumor-mRNA transfected dendritic cells. Cancer Immunology Immunother 2006 (Epub ahead of print).
24. Gilboa E, Nair SK, Lyerly HK. Immunotherapy of cancer with dendritic cell-based vaccines. Cancer Immunology Immunother 1998;46(2):82-87.
25. Bohnenkamp H. Process development for the generation of matured monocyte-derived dendritic cells suitable for clinical aplication. www.Fz-juelich.de/ibt/cell/matured-dendritic-cells.2006.
26. Vieweg J. Dendritic cell therapy for GU malignancies. State of the science – Genitourinary 2002; 14; (www.webtie.org/SOTS/Meetings/Genitourinary/SUO_12_13_14_2002/lectures.htm).
27. Wang B, He J, Lui C, Chang LJ. An effective cancer vaccine modality: lentiviral modification of dendritic cells expressing multiple cancer-specific antigens. Vaccine 2006;24: 3477-3489.
28. Khan JA, Yaqin S. Dendritic cell therapy with improved outcome in glioma multiformr – A case report. J Zhejiang University Sc B 2006;7:114-117.
29. Ribas A. Genetically modified dendritic cells for cancer immunotherapy. Curr Gene Therapy 2005; 5(6): 619-628.
30. Fong L, Engleman EG. Dendritic cells in cancer immunotherapy. Annual Rev Immunol 2000; 18:245-273.
31. Small EJ, Fratesi P, Reese DM, Strang G. Immunotherapy of hormone-refractory prostate cancer with antigen-loaded dendritic cells. J Clinical Oncol 2000;18:3894-3903.
32. Nestle FO, Alijagic S, Gilliet M, Sun Y. Vaccinations of melanoma patients with peptide or tumor lysate-pulsed dendritic cells. Nat Med 1998; 4(3):328-332.
33. Timmerman JM, Levy R. Dendritic cell vaccines for cancer immunotherapy. Annual Rev Medicine 1999;50: 507-529.
34. Lesterhuis WJ, Vries LJ, Schuurhuis DH. Vaccination of colorectal cancer patients with CEA–loaded dendritic cells: antigen specific T cell responses in DTH skin test. Annual Oncology 2006;17: 974-980.
35. Santin AD, Bellone S, Underwood LJ, et al. Dendritic cell-based immunotherapy for ovarian cancer. Minerva Ginecol 2002;54(2):133-144.
36. Liu G, Black KL, Yu JS. Sensitization of malignant glioma to chemotherapy through dendritic cell vaccination. Expert Rev Vaccines 2006;5(2): 233-247.
37. Farkas A, Conrad C, Tonel G. Current state and perspectives of dendritic cell vaccination in cancer immunotherapy. Skin Pharmacol Physiol 2006;19:124-131.
1 Aluna do 6.º ano de Medicina da Faculdade de Medicina da Universidade de Coimbra 2007-2008
2 Professora da Faculdade de Medicina da Universidade de Coimbra
3 Disciplina de Fisiopatologia, mestrado integrado em Medicina Dentária.
4 Instituto de Bioquímica e disciplina de Biologia Molecular Aplicada. Mestrado integrado em Medicina
Recebido para publicação/received for publication: 08.08.08
Aceite para publicação/accepted for publication: 09.02.05













