Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Jornal Português de Gastrenterologia
versão impressa ISSN 0872-8178
J Port Gastrenterol. vol.21 no.2 Lisboa abr. 2014
https://doi.org/10.1016/j.jpg.2013.11.002
ARTIGO DE REVISÃO
Ecoendoscopia digestiva na prática clínica parte IIa - utilidade na avaliação do pâncreas
Digestive endoscopic ultrasound in clinical practice part IIa - utility in the evaluation of pancreas
Catarina Graça Rodriguesa,∗, Eduardo Pereirab, Ana Caldeirab, Antonieta Santosb, Helena Sousac e António Banhudob
a Serviço de Gastrenterologia, Hospital Professor Doutor Fernando Fonseca, Amadora, Lisboa, Portugal
b Serviço de Gastrenterologia, Hospital Amato Lusitano, Castelo Branco, Portugal
c Serviço de Gastrenterologia, Centro Hospitalar do Barlavento Algarvio, Portimão, Portugal
*Autor para correspondência
RESUMO
Desde a altura em que foi desenvolvida, na década de 80, a ecoendoscopia tem vindo a assumir uma importância crescente no diagnóstico de várias doenças pancreáticas benignas e malignas. O papel que detém atualmente na abordagem da patologia pancreática veio confirmar a razão histórica da sua implementação. Pela proximidade do transdutor e reduzida interferência acústica, a ecoendoscopia fornece imagens ultrassonográficas de alta resolução do pâncreas e com grande detalhe anatómico, acrescentando à informação obtida por tomografia computorizada ou por ressonância magnética aspetos essenciais na investigação dos doentes com suspeita de patologia pancreática. A ecoendoscopia tem, além disso, a capacidade única de guiar a punção aspirativa de lesões pancreáticas e estruturas adjacentes para obtenção de um diagnóstico cito-histológico. Nos últimos anos, a aplicação à ecoendoscopia de novas modalidades da ultrassonografia, como a elastografia e o uso de contrastes, tem revelado resultados promissores e está a ampliar as potencialidades desta técnica.
Na sequência de artigos de revisão sobre ecoendoscopia, este primeiro capítulo da segunda parte pretende abordar as principais indicações desta técnica no diagnóstico da patologia do pâncreas, bem como os achados endossonográficos que a caracterizam.
Palavras-Chave: Ecoendoscopia;Punção aspirativa por agulha fina guiada por ecoendoscopia; Tumores pancreáticos; Quistos pancreáticos; Pancreatite
SUMMARY
Since it was developed in the 80s, endoscopic ultrasound (EUS) has taken on na important role in the diagnosis of benign and malignant pancreatic disease, confirming the historical reasons for its implementation. Due to the proximity of the transducer and reduced acoustic interference, EUS provides high-resolution ultrasound images of the pancreas with subtle anatomical detail and adds complementary information to both computed tomography or magnetic resonance in the investigation of patients with suspected pancreatic disease. EUS has the unique ability to obtain specimens of the pancreas and peripancreatic structures for cytohistological diagnosis. In recent years, newly developed ultrasound modalities associated to EUS, like elastography and contrast enhancement, have shown promising results and might increase the diagnostic value of this technique.
This first chapter of the second part of a series of review articles on EUS aims to address the main indications of this endoscopic technique in the diagnosis of pancreatic disease, as well as the typical ultrasound findings in this setting.
Keywords: Endosonography; Endoscopic ultrasound-guided fine needle aspiration; Pancreatic neoplasms; Pancreatic cysts; Pancreatitis
Introdução
A ecoendoscopia (EE) permite avaliar toda a espessura da parede gastrointestinal e discriminar as suas diferentes camadas histológicas através da respetiva correspondência ultrassonográfica, assumindo um papel único na caracterização das lesões parietais e no estadiamento locoregional das neoplasias gastrointestinais (Ecoendoscopia digestiva na prática clínica - avaliação da parede gastrointestinal, GE 2011 vol.18). As outras indicações advêm da sua capacidade de fornecer imagens de alta resolução das estruturas adjacentes à parede digestiva, nomeadamente do pâncreas.
A possibilidade de posicionar o transdutor muito próximo da área pancreática minimiza os efeitos de artefacto que são produzidos pela interposição de ar luminal digestivo, que constituem uma das principais limitações da abordagem ultrassonográfica transparietal convencional. As sondas de alta frequência utilizadas fornecem imagens de alta resolução espacial, permitindo identificar estruturas milimétricas.
A opção pela modalidade de abordagem linear ou radial depende das particularidades anátomo-clínicas a avaliar, da experiência do operador e da disponibilidade do equipamento. No entanto, é aceite que a ecoendoscopia linear permite uma melhor caracterização de alguns detalhes anatómicos do pâncreas, além de proporcionar a colheita de material para cito-histologia através de punção aspirativa com agulha fina (PAAF). Desde a sua introdução, em 1992, que a punção aspirativa com agulha fina guiada por ecoendoscopia (PAAF-EE) se tem evidenciado como um procedimento eficaz e seguro, encontrando-se atualmente incluída em grande parte dos algoritmos de diagnóstico e estadiamento de lesões pancreáticas.
A EE é considerada uma técnica minimamente invasiva, apresentando uma reduzida taxa de complicações (1-3%), associadas na maioria à realização de PAAF (perfuração, infeção, hemorragia, pancreatite, disseminação tumoral)1,2. Tem como principais limitações o facto de ser operador dependente e ter uma baixa reprodutibilidade.
Lesões sólidas do pâncreas
A natureza das lesões sólidas do pâncreas é vasta. As entidades malignas compreendem o adenocarcinoma ductal (ADC), os tumores neuroendócrinos (TNE), o linfoma pancreático, as metástases de tumores extrapancreáticos, o carcinoma de células acinares, a neoplasia pseudopapilar sólida e, ainda, as neoplasias quísticas com componente sólido. As lesões benignas incluem os pseudotumores inflamatórios, que podem ocorrer no contexto de pancreatite crónica, pancreatite focal ou pancreatite autoimune (PAI), e as lesões quísticas complexas.
A aplicação clínica da EE na abordagem das lesões sólidas do pâncreas tem sido avaliada segundo a sua capacidade na deteção e diagnóstico, bem como no estadiamento e determinação da ressecabilidade das mesmas.
Estudos comparativos datados de há 2 décadas reportam uma maior sensibilidade da EE na deteção de lesões sólidas do pâncreas (94-99%) comparativamente com a ultrassonografia abdominal (67%), tomografia computorizada (TC) (69-77%) e ressonância magnética (RM) (83%), uma superioridade mais notória no caso das lesões com menos de 3 cm (sensibilidade 93-100% para a EE, 50-89% para a TC e 67% para a RM)3-6. A EE permite detetar e puncionar lesões com menos de 1 cm7. O seu valor preditivo negativo (VPN) aproxima-se dos 100%, sendo os falsos negativos geralmente resultantes de aspetos infiltrativos difusos das lesões tumorais, coexistência de pancreatite crónica ou episódio recente (< 4 semanas) de pancreatite aguda8.
Em contraste com a elevada sensibilidade, a EE apresenta uma especificidade diagnóstica relativamente baixa, porque as características da imagem ultrassonográfica convencional em modo B não permitem diferenciar tumores pancreáticos malignos de massas inflamatórias pseudotumorais. No entanto, a realização de PAAF-EE possibilita o diagnóstico diferencial na maioria dos casos9.
A EE pode ser utilizada no estadiamento loco-regional das lesões malignas do pâncreas (sistema TNM, American Joint Committee on Cancer), ao permitir avaliar a sua relação com os órgãos e as estruturas vasculares adjacentes, aspeto crítico na determinação do estádio T e da ressecabilidade tumoral, e a existência de linfadenopatias malignas peripancreáticas. A validade dos estudos existentes acerca do valor da EE neste contexto é, contudo, limitada, sendo os resultados heterogéneos. Em geral, admite-se que a EE é superior à TC no estadiamento T e na avaliação da invasão vascular do confluente esplenoportal, e equivalente na determinação do estadiamento N e na predição da ressecabilidade tumoral6,10.
Na última década a disponibilidade da alta definição e a capacidade de aquisição volumétrica da TC helicoidal multicorte revolucionou a resolução da imagem pancreática por TC, elevando a sensibilidade global da técnica para 97-100% e a predição de ressecabilidade para quase 100% na avaliação das lesões sólidas11. Igualmente as novas modalidades da RM associam-se a taxas de sensibilidade de 83-87% e especificidade de 81-100%11, emergindo como uma alternativa à TC no estudo do pâncreas, embora mais dispendiosa. O valor da tomografia de emissão de positrões acoplada à tomografia computorizada (PET-TC) foi avaliado numa meta-análise recente, que reporta uma sensibilidade e especificidade diagnósticas de 81-90% e 83- 93%, respetivamente12. Embora o seu valor no diagnóstico diferencial dos tumores pancreáticos seja reduzido, a PETTC com contraste (18F-fluorodeoxyglucose) apresenta uma acuidade superior a 80% na determinação da invasão local e de 94% na identificação de metástases distantes. Além da capacidade na avaliação da resposta ao tratamento, tem uma elevada sensibilidade no diagnóstico da recorrência pós-operatória, superior à TC13-15. Considerando as potencialidades emergentes da PET-TC, também o seu valor no estadiamento N tem sido avaliado, revelando uma sensibilidade de 46-71% e uma especificidade de 63-100%16.
Na prática clínica, a TC de última geração realizada segundo protocolo pancreático (multifásico) é o melhor método de imagem inicial em caso de suspeita de lesão pancreática focal, por se encontrar amplamente disponível e por permitir diagnosticar, bem como estadiar e predizer a ressecabilidade da maioria das lesões. A RM é especialmente útil na deteção e caracterização de massas pancreáticas que não alteram o contorno pancreático e de pequenas metástases hepáticas, peritoneais e do epíploon17. A realização da EE deverá ser considerada em 2 circunstâncias principais e consensuais: para confirmar a ausência de lesões pancreáticas segundo outros métodos de imagem (TC/RM), perante forte suspeita clínica, ou clarificar imagens equívocas e inconclusivas por estes detetadas; e nas situações de irressecabilidade tumoral, para obtenção de um diagnóstico cito-histológico através de PAAF-EE. Em caso de lesões potencialmente ressecáveis (15-20%), a necessidade de diagnóstico definitivo pré-operatório continua em debate, sobretudo no caso das massas localizadas no corpo distal e cauda, pelo risco de disseminação peritoneal ou implantação tumoral na parede gástrica. Este risco é, no entanto, significativamente inferior ao da PAAF guiada por TC, estando apenas relatados alguns casos isolados (0,5-3% )1,2,18. Quando utilizada no estadiamento loco-regional de lesões com indicação duvidosa para resseção (borderline ressectable), a EE pode detetar disseminação metastática previamente insuspeita em mais de 10% dos casos, evitando assim a cirurgia19. Se o estudo inicial por TC ou RM evidenciar metástases à distância, a EE não está formalmente indicada e a punção lesional poderá ser realizada por via percutânea.
O papel da PAAF-EE no diagnóstico das lesões sólidas do pâncreas foi avaliado numa meta-análise recente, que reporta uma sensibilidade, especificidade, valor preditivo positivo (VPP) e VPN para malignidade de 85-91%, 94-98%, 98-99% e 65-72%, respetivamente20. Este último valor significa que uma PAAF negativa para malignidade não permite excluir em definitivo essa possibilidade, pelo que está recomendada a sua repetição se persistir a suspeita clínica21. O diagnóstico diferencial entre lesão maligna e pseudotumor inflamatório continua a ser uma das grandes limitações da técnica22.
A avaliação da qualidade da amostra no local do procedimento por um citopatologista (Rapid On-Site Cytologic Evaluation - ROSE) aumenta globalmente a sensibilidade e a acuidade diagnóstica da PAAF-EE em 10-15% e pode diminuir o número de passagens necessárias, embora nem todos os estudos o tenham demonstrado23-26. Encontra-se por determinar o papel do citotécnico experiente ou do endossonografista com treino em citopatologia, na impossibilidade da presença do citopatologista. A seleção do calibre da agulha de PAAF depende das características e da localização da lesão a puncionar, sendo a sua acuidade e segurança globalmente similares. Dados recentes da literatura conferem à agulha de 25 gauge (G) uma vantagem na qualidade da amostra menor contaminação e uma sensibilidade superior no diagnóstico de malignidade pancreática comparativamente com a agulha 22G (93 versus 85%), no entanto, sem qualquer diferença quanto à acuidade diagnóstica, número de passagens necessárias e complicações27,28. Uma vantagem técnica indiscutível da agulha 25G é a sua aplicação nas lesões sólidas do processo uncinado.
Encontram-se em avaliação as novas agulhas desenhadas para obter fragmentos de biopsia (como as agulhas ProCoreTM 19, 22 e 25 G), desenvolvidas para ultrapassar as limitações técnicas das agulhas tru-cut (19 G), mas os resultados iniciais são comparáveis aos das agulhas de PAAF29,30. Além disso, o material obtido com as agulhas de PAAF pode ser enviado para preparação citobloco (cellblock) em complemento aos esfregaços, proporcionando uma análise histológica e estudos de imuno-histoquímica, genética e citometria de fluxo, particularmente úteis na suspeita de TNE, linfoma ou PAI.
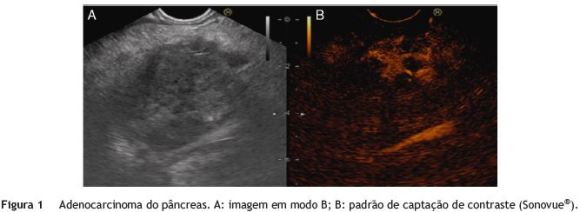
A elastografia e o contraste endovenoso têm vindo a ser aplicados à EE, com o objetivo de colmatar o VPN limitado da PAAF. A elastografia-EE permite estimar a elasticidade dos tecidos em tempo real. A sua utilização baseia-se no princípio de que os tecidos malignos apresentam uma maior dureza. Os primeiros dados publicados referem-se a uma avaliação qualitativa, que utiliza uma escala de cores para representar diferentes graus de dureza tecidual. Recentemente, foi desenvolvida a elastografia quantitativa ou de 2.a geração que fornece um resultado numérico comparativo, tornando a interpretação dos resultados menos subjetiva. Estudos iniciais reportam uma acuidade superior a 85% na diferenciação entre lesões pancreáticas malignas e benignas, comparável à PAAF-EE, embora os valores cut-off de referência careçam de validação31,32. A elastografia-EE pode contribuir para o diagnóstico diferencial entre ADC e pancreatite crónica (sensibilidade 100%, especificidade 96%) e entre ADC e TNE (sensibilidade 100%, especificidade 88%)31. Por sua vez, a administração de contraste endovenoso (hexafluoreto de enxofre, Sonovue®) (fig. 1) permite analisar o padrão de microvascularização das lesões. O ADC tem uma aparência hipovascular, contrariamente aos TNE e às lesões de pancreatite crónica e autoimune, que têm aparência hiper ou isovascular33. O achado de uma massa hipocaptante exibe uma sensibilidade de 94% e especificidade de 89% no diagnóstico de ADC do pâncreas34. A análise quantitativa da captação de contraste pode vir a aumentar a acuidade da técnica, particularmente no diagnóstico diferencial entre ADC e pancreatite crónica34. Outras aplicações possíveis dos agentes de contraste incluem a avaliação das estruturas vasculares perilesionais, permitindo melhorar a acuidade da EE no estadiamento T, e a deteção de lesões de pequenas dimensões não identificadas por EE em modo B, particularmente nos doentes com pancreatite crónica ou com próteses biliares. Embora não possam substituir a PAAFEE, estas 2 modalidades podem contribuir para a tomada de decisões clínicas na abordagem de casos com cito-histologia negativa para malignidade e podem ser utilizadas para guiar e potenciar os resultados da PAAF-EE de lesões pancreáticas e de gânglios linfáticos, permitindo selecionar as áreas suspeitas a puncionar35,36.
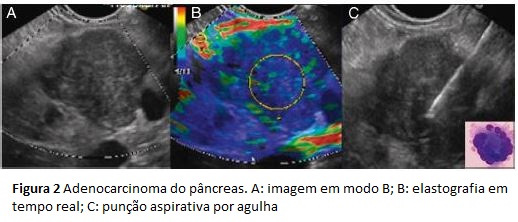
O ADC compreende 90% das neoplasias sólidas do pâncreas. Localiza-se mais frequentemente na região cefálica. O aspeto ecomorfológico mais representativo deste tumor é o de uma massa heterogénea, hipoecóica e com margens irregulares (fig. 2), tendo como achados preditivos a dilatação do ducto pancreático principal e a presença de um halo hipoecóico periductal (sinal hipoecóico periductal)37.
Dada a elevada sensibilidade da angio-TC na avaliação da invasão arterial, a EE deve ter o papel de confirmar o grau de envolvimento vascular já determinado por este método de imagem, após exclusão de metastização à distância38. Os tumores irressecáveis ou borderline ressectable podem ser incluídos em protocolos de terapêutica neoadjuvante em validação e com diferentes finalidades39. Nestes casos é mandatório o diagnóstico cito-histopatológico prévio obtido por PAAF-EE. Igualmente, a presença de linfadenopatias malignas pode justificar a realização de terapêutica neoadjuvante. As características ecomorfológicas dos gânglios linfáticos associadas a malignidade são a forma arredondada, dimensão superior a 5mm, ecotextura hipoecóica e margens bem definidas. Quando presentes em conjunto, apresentam uma acuidade diagnóstica de 80%, o que ocorre em apenas 25% dos gânglios malignos, podendo ser necessário recorrer à PAAF para confirmação cito-histológica37. A EE possibilita, também, a identificação e punção de bolsas de efusões peritoneais e pleurais, lesões nodulares hepáticas e adenopatias à distância.
Um estudo com um número limitado de doentes comparou a eficácia da EE e da TC na determinação da ressecabilidade pós-terapêutica neoadjuvante do ADC localmente avançado e mostrou uma acuidade idêntica (89 e 75%, respetivamente)40.
Os TNE totalizam 3-5% das neoplasias sólidas pancreáticas. Com frequência, as suas características ecomorfológicas são discriminativas, sendo tipicamente homogéneos, hipoecóicos, com margens bem delimitadas e hipervasculares (fig. 3). O seu diâmetro médio é inferior a 1,5 cm, mas podem atingir grandes dimensões, particularmente no caso dos tumores não funcionantes. Variantes morfológicas incluem lesões isoecóicas ou hiperecóicas, com calcificações e aspetos de degenerescência quística. Alguns achados ecomorfológicos podem predizer malignidade, nomeadamente a existência de uma área central ecogénica e irregular, áreas quísticas ou a dilatação obstrutiva do sistema ductal pancreático41. O diagnóstico pode ser confirmado por PAAF-EE e estudo imuno-histoquímico, que se caracteriza pela marcação com sinaptofisina e cromogranina A. A análise molecular com quantificação do Ki-67 tem provado utilidade na avaliação do comportamento maligno dos TNE, sendo preditiva da sobrevida aos 5 anos42. O sistema de estadiamento é idêntico ao dos tumores pancreáticos exócrinos.
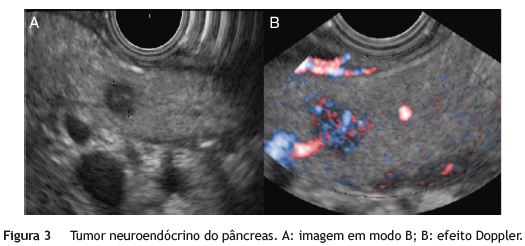
A EE tem uma acuidade diagnóstica global de 57-89% para os TNE da área pancreato-duodenal. A sensibilidade varia entre 80-90% para os tumores de localização pancreática, e entre 30-50% para os tumores de localização extrapancreática43-47. Assim, é útil na suspeita clínica de TNE cuja localização primária não foi identificada pelos métodos de imagem convencionais (TC), permitindo detetar a quase totalidade dos insulinomas e também dos gastrinomas, exceto quando estes se localizam na parede duodenal, em que apresentam geralmente dimensões mais reduzidas48. Comparativamente à cintigrafia com 111In-Pentatreótido-OctreoscanTM, a EE tem uma sensibilidade diagnóstica superior, além de permitir a caracterização citohistológica do tumor primário e de eventuais metástases49. O uso de contraste para deteção do padrão hipervascular lesional é um valioso método para localizar e diagnosticar pequenos TNE50.
O linfoma primário do pâncreas, que corresponde geralmente a um linfoma não Hodgkin (LNH) de grandes células B, representa 0,5% das neoplasias sólidas do pâncreas e 3% dos casos de LNH extranodal51. O envolvimento pancreático secundário é mais comum, ocorrendo em cerca de 1/3 dos doentes com LNH52. Assume tipicamente a forma de uma massa homogénea e hipoecóica, bem circunscrita, localizada na cabeça do pâncreas, regra geral sem invasão das estruturas vasculares e sem dilatação do ducto pancreático principal53. Quando o padrão é infiltrativo pode confundir-se com aspetos da pancreatite aguda. Coexistem, habitualmente, múltiplas linfadenopatias peripancreáticas, que têm uma localização caraterística inferior às veias renais54. O diagnóstico pode ser confirmado pela PAAF-EE, mediante análise por citometria de fluxo e/ou estudo imunohistoquímico. Em caso de suspeita clínica deverá ser enviado material para citobloco ou ser utilizadas agulhas que permitem obter fragmentos de biopsia.
O carcinoma de células acinares representa 1% das neoplasias sólidas do pâncreas, atingindo tipicamente homens na 6.a ou 7.a décadas da vida. Apresenta-se, habitualmente, como uma massa volumosa localizada no corpo ou cauda, encapsulada e com um padrão de crescimento que pode ser acinar ou sólido. O diagnóstico depende da presença de grânulos de zimogénio (coloração ácido periódico Schiff [PAS]) e análise imuno-histoquímica com marcação para a tripsina, quimiotripsina, lipase, amilase e fosfolipase A255. As células tumorais podem produzir marcadores que mimetizam os TNE, conduzindo frequentemente a erros diagnósticos56.
Em aproximadamente 1% dos casos, as neoplasias sólidas ressecadas correspondem a metástases pancreáticas, mais frequentemente de tumores do rim (carcinoma de células renais), mas também do pulmão, mama, cólon, melanoma, sarcoma e ovário57. Estas lesões podem aparecer vários anos após o diagnóstico do tumor primário, pelo que devem ser sempre consideradas quando há antecedentes de neoplasia maligna. A ecomorfologia é muito variada, podendo corresponder a lesões de natureza sólida e/ou quística, com ecogenicidade variável, muitas vezes hipervasculares, e podem apresentar-se na forma de uma lesão única, localizada preferencialmente no segmento da cabeça, lesões múltiplas ou com um padrão de infiltração difusa58. A PAAF-EE contribui, geralmente, para o diagnóstico definitivo.
Nos últimos anos, tem vindo a ser discutida a implementação de um programa de rastreio para os indivíduos com risco familiar de carcinoma pancreático (história familiar, síndrome de Peutz-Jeghers, Familial Atypical Multiple Mole Melanoma Syndrome, mutações no gene BRCA2, síndrome de Lynch, pancreatite hereditária), eventualmente baseado na EE, tendo em conta a elevada acuidade desta técnica na avaliação do pâncreas e ao fato de não utilizar radiação ionizante. Contudo, a evidência que suporta o rastreio e vigilância nestes indivíduos de elevado risco é limitada a estudos observacionais, permanecendo por determinar a efetividade desta estratégia em termos clínicos e económicos59-61. Além disso, não há consenso quanto à idade em que se deve iniciar a vigilância, ao intervalo ótimo entre as avaliações, bem como aos métodos de imagem a utilizar. A abordagem das várias lesões que possam ser identificadas (vigilância versus cirurgia) constitui, igualmente, um grande desafio. No momento atual, o rastreio do carcinoma pancreático em indivíduos de elevado risco só deverá ser realizado em centros especializados, sob orientação de equipas multidisciplinares e preferencialmente no contexto de protocolos de investigação62.
Lesões quísticas do pâncreas
As lesões quísticas do pâncreas são, muitas vezes, detetadas de forma incidental, estimando-se uma prevalência acima de 3% nos estudos por TC e de 20% por RM63-65. Estudos baseados em autópsia reportam a existência de lesões quísticas pancreáticas infracentimétricas em até 24% dos indivíduos66.
Correspondem a um vasto espetro de entidades, com um comportamento biológico variável e, nalguns casos, com uma história natural pouco conhecida. Cerca de 50-60% são de natureza neoplásica67. Quatro entidades totalizam 90% destas lesões: neoplasia quística serosa (NQS), neoplasia mucinosa papilar intraductal (NMPI), neoplasia quística mucinosa (NQM) e neoplasia sólida pseudopapilar (NSP). As neoplasias mucinosas (NQM/NMPI) revestem-se de particular importância pelo seu potencial comportamento maligno68. Os restantes 10% incluem o cistadenocarcinoma, a variante quística dos TNE e do carcinoma de células acinares, o hamartoma quístico, o teratoma quístico ou quisto dermoide, o quisto epidermoide/baço acessório e os quistos metastáticos. Raramente podem ser identificados tumores não epiteliais, como o linfangioma e o sarcoma69. Entre as lesões quísticas não neoplásicas destacam-se o pseudoquisto (PQ), mais comum, que corresponde a uma coleção líquida inflamatória não revestida por epitélio, e o quisto linfoepitelial, de retenção ou congénito.
A caracterização das lesões quísticas pancreáticas visa discriminar as lesões que devem ser abordadas cirurgicamente e as lesões que requerem vigilância. Na prática, importa identificar os quistos neoplásicos e determinar o seu potencial de malignidade. A EE está em posição privilegiada para avaliação destas lesões por permitir a aquisição de imagens de elevada resolução dos quistos e do restante parênquima pancreático, e possibilitar a colheita do conteúdo quístico por PAAF-EE, devendo ser considerada após estudo dirigido por TC multicorte e, preferencialmente, RM com pancreato-RM.
A subdivisão das lesões quísticas pancreáticas segundo a sua dimensão contribui para a decisão interdisciplinar da abordagem das mesmas. A EE tem um papel particularmente importante na avaliação dos quistos com dimensões entre 1-3 cm (questionável se < 2 cm) dado que a eventual vigilância não invasiva (TC/RM) deve ser precedida da confirmação da natureza mucinosa da lesão por PAAF70. Além disso, a realização de EE justifica-se sempre que a TC ou RM coloque a possibilidade da presença de um componente sólido ou de dilatação focal ou difusa do ducto pancreático principal.
Os detalhes ecomorfológicos das lesões quísticas pancreáticas apresentam uma acuidade de 50-73% na determinação da sua natureza71, pelo que devem ser conjugados com os aspetos anamnésicos e os biomarcadores obtidos por análise do fluido quístico (citologia, marcadores tumorais, amilase, mucinas e análise do DNA). O valor de CEA no fluido quístico pode ser útil na determinação da etiologia mucinosa, não permitindo distinguir entre NQM e NMPI ou avaliar o risco de malignidade72,73. Um valor de antigénio carcinoembrionário (CEA) < 5 ng/ml é indicativo da presença de NQS ou PQ com um VPP de 94% e uma acuidade de 70%, enquanto um valor de > 800 ng/ml é a favor de natureza mucinosa com um VPP de 94% e uma acuidade de 79%39. A quantidade de fluido necessária para o seu doseamento é de 1,0 mL, pelo que os quistos a puncionar deverão ter uma dimensão mínima de 1 cm, e preferencialmente mais do que 2 cm. Um valor elevado de amilase constitui um indicador de comunicação ductal, e sugere tratar-se de um PQ ou NMPI. A presença de mutações do gene K-ras é considerada altamente específica para a deteção de lesões mucinosas, embora com baixa sensibilidade. A citologia tem uma sensibilidade de apenas 50% para o diagnóstico de malignidade. A PAAF-EE das lesões quísticas pancreáticas está associada a uma baixa taxa de complicações (2-5%), que incluem a hemorragia, mais frequente nas NQS e TNE dada sua natureza vascular, infeção e pancreatite aguda. A infeção intraquística é, hoje, um evento raro dada a recomendada profilaxia antibiótica74.
O pseudoquisto é mais comum no sexo masculino. Está quase sempre associado a história de pancreatite aguda ou crónica, consumo de álcool, traumatismo abdominal ou sinais imagiológicos de pancreatite crónica75. O aspeto ecomorfológico mais habitual é o de uma coleção arredondada, unilocular, sem septos ou nódulos murais (fig. 4). Em 10-20% dos casos tem uma aparência multilocular76. A parede pode ser praticamente impercetível ou apresentar-se uniformemente espessada, correspondendo a tecido de granulação e fibrótico não epitelizado. Uma característica altamente específica do PQ é a presença de detritos no seu interior, identificados por EE como material hiperecóico mobilizável com a mudança de posição do doente. Este achado pode ser confundido com o aspeto granular da mucina de algumas NQM. Tipicamente o PQ apresenta comunicação com o ducto pancreático, que nem sempre é identificada pela EE38. Através da PAAF-EE pode ser recolhido um conteúdo líquido que tem baixa viscosidade e uma elevada concentração de amilase, excluindo-se virtualmente o seu diagnóstico quando o este valor é < 250 UI/L39.
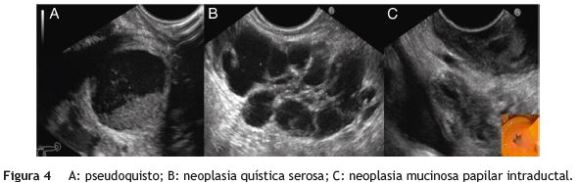
A neoplasia quística serosa, ou cistadenoma seroso, corresponde a 30% das lesões quísticas neoplásicas e a 16% dos quistos neoplásicos ressecados77. O pico de incidência ocorre na 6.a década de vida e tem maior prevalência no sexo feminino. A sua localização pancreática não tem predileção segmentar78. É habitualmente assintomática, exceto quando tem dimensões superiores a 4 cm, o que pode condicionar sintomas por efeito compressivo. Embora seja considerada uma lesão benigna, a sua transformação maligna é possível, ainda que extremamente rara, estando publicados com alguns casos de cistadenocarcinoma78. Tipicamente tem um padrão ecomorfológico multiquístico, com quistos menores que 2 cm. Pode existir uma área microquística constituída por um agregado de microquistos de 2-3mm cada e em número superior a 679. Os espaços quísticos estão separados por septos fibrosos hipervasculares, que podem coalescer numa cicatriz estrelada central, por vezes calcificada, presente em até 30% das lesões (fig. 4). A presença desta cicatriz constitui um achado patognomónico, mas é identificada por EE em apenas 11% dos casos80. Em 30% dos casos a NQS assume uma aparência pseudosólida, em «favo de mel», devido a uma densa septação que produz inúmeras interfaces entre os pequenos quistos81. A variante oligo ou macroquística ocorre em mais de 10% dos casos e caracteriza-se por um número reduzido de espaços quísticos e septos e ausência de componente microquístico, pelo que se confunde facilmente com a NQM80. Os doentes com síndrome de Von Hippel-Lindau têm frequentemente NQS múltiplas de padrão oligoquístico. Habitualmente, a NQS tem contornos lobulados, reduzida diferenciação com o parênquima pancreático adjacente, não tem evidência de parede e não comunica com o ducto pancreático.
A PAAF-EE não é necessária nas lesões com detalhes ecomorfológicos caraterísticos de NQS, devendo ser reservada para diferenciar a variante macroquística da NQM, mediante avaliação dos biomarcadores do fluido quístico. A punção deve ser dirigida ao compartimento de maiores dimensões. O fluido recolhido não é viscoso e apresenta um componente celular cuboide com citoplasma rico em glicogénio e cromatina densa. Está recomendada uma abordagem conservadora, mas na presença de sintomas ou se existir incapacidade de excluir o potencial de malignidade das formas macroquísticas deve ser considerada a resseção cirúrgica.
A neoplasia quística mucinosa, ou cistadenoma mucinoso, corresponde a 25% dos quistos neoplásicos do pâncreas ressecados77. Ocorre quase exclusivamente no sexo feminino e tem um pico de incidência na 4.a e 5.a décadas de vida. Localiza-se mais frequentemente no corpo e cauda do pâncreas. É considerada uma lesão pré-maligna, apresentando uma incidência de carcinoma invasivo de 12-29%82. São considerados fatores preditivos de malignidade a idade avançada, dimensão quística superior a 4 cm e presença de espessamento parietal, nódulos murais ou calcificações periféricas83. Não está descrita malignidade em NQM com dimensões < 4 cm e sem nódulos murais.
Habitualmente, apresenta-se como uma lesão única, arredondada, unilocular, bem definida e sem comunicação com o ducto pancreático. No entanto, pode ser multilocular, com múltiplos macroquistos (1-2 cm cada e em número inferior a 6) divididos por septos, dando o aspeto de «quistos em quisto». A parede pode apresentar calcificações em «casca de ovo», características da NQM e preditivas de malignidade, embora presentes em apenas 10-25% dos casos84. O conteúdo é mucoide e quando é mais espesso pode condicionar alguma ecogenicidade granular interior. O revestimento é constituído por uma camada de células epiteliais produtoras de mucina, que podem exibir graus variáveis de atipia, de adenoma a carcinoma invasivo, e um estroma semelhante ao ovárico85.
Dada a idade relativamente jovem da maioria dos doentes, o risco de progressão para malignidade e a localização frequente no corpo ou cauda, está recomendada a resseção cirúrgica, sobretudo na presença de aspetos preditivos de malignidade86.
A neoplasia mucinosa papilar intraductal é reconhecida como uma entidade que engloba diferentes aspetos epidemiológicos e clínicos. Pode ter origem no epitélio do ducto pancreático principal (neoplasia mucinosa papilar intraductal do ducto principal [NMPI-DP]), nos ductos secundários (neoplasia mucinosa papilar intraductal dos ductos secundários [NMPI-DS]) ou em ambos (NMPI-misto ou combinado), constituindo 3 subtipos específicos com diferente potencial de malignidade.
A NMPI-DP ocorre mais frequentemente no sexo masculino, entre a 6.a e a 7.a décadas de vida. A sintomatologia mais comum é a dor abdominal e a perda ponderal, mas pode manifestar-se num contexto de pancreatite recorrente ou ser identificada incidentalmente. Localiza-se em 2/3 dos casos na cabeça do pâncreas, envolvendo também, com frequência, o processo uncinado87,88. A EE identifica uma dilatação segmentar ou difusa do ducto pancreático principal (> 6 mm), sem causa obstrutiva evidente. Pode observar-se um espessamento mural ductal e defeitos de preenchimento devido à presença de mucina, estando o pâncreas aumentado ou atrófico. Neste caso e na presença de calcificações, impõe-se o diagnóstico diferencial com a pancreatite crónica. A observação endoscópica da papila duodenal deve ser realizada de forma sistemática com o objetivo de despistar a extrusão papilar de mucina, conhecido como «papila em olho ou boca de peixe», sinal patognomónico da NMPI-DP ou do tipo misto, embora presente em apenas 1/3 dos casos (fig. 4). A resseção é recomendada a todos os doentes com condições para cirurgia, tendo em conta a elevada incidência de malignidade e de carcinoma invasivo, respetivamente de 60 e 40%89.
A NMPI-DS é o tipo mais frequente de lesões quísticas neoplásicas do pâncreas sendo, habitualmente, assintomática. Pode apresentar-se como um quisto infracentimétrico isolado ou, mais frequentemente, como uma lesão multiquística com uma coleção de quistos dispostos em «cacho de uvas» que comunicam com o sistema ductal, correspondendo à dilatação de múltiplos ductos secundários preenchidos por mucina. Caracteristicamente apresenta um aspeto «quisto a quisto», de contorno irregular e forma não arredondada. Outras variantes incluem a morfologia tubular digitiforme ou a dilatação clubbed-like dos ductos secundários, determinando um aspeto pleomórfico, quando associados. A comunicação com o sistema ductal pode não ser visível, confundindo-se com a NQM89. Em 21-41% dos casos é multifocal, o que constitui um sinal de grande especificidade para o diagnóstico da NMPI-DS.
A abordagem da NMPI-DS deve ter em conta a possibilidade de concomitância de ADC e o seu potencial de malignidade, sendo que aproximadamente 25,5% destas lesões sofrem transformação maligna, com um risco de 20% do seu desenvolvimento num período de 10 anos. Neste contexto recomenda-se cirurgia na presença de sintomas, quando a lesão tem um componente sólido ou nódulo mural, quando há envolvimento do ducto principal (dilatação > 1 cm, mucina intraductal ou espessamento parietal), ou em caso de citologia suspeita ou positiva para malignidade89. Apesar de controverso, o critério dimensional tem vindo a ser desvalorizado, exceto em doentes jovens, em que a cirurgia deve ser considerada na presença de um quisto com dimensões superiores a 2-3 cm, pelo risco cumulativo de malignidade78. A decisão deve ser, no entanto, individualizada e dependente das condições clínicas do doente e da localização da lesão74. Em caso de vigilância a TC deve ser preterida à pancreato-RM, que apresenta uma maior acuidade na identificação de nódulos e comunicação ductal, sem aplicação de radiação ionizante.
A neoplasia pseudopapilar sólida corresponde a 1-2% das lesões quísticas neoplásicas e a 4% dos quistos neoplásicos ressecados77. Atinge tipicamente jovens do sexo feminino na 2.a ou 3.a décadas de vida90. Pode localizar-se em qualquer segmento pancreático, sendo mais frequente na cauda e ocorrendo apenas ocasionalmente na cabeça. O seu crescimento indolente poderá ser responsável pelo diagnóstico frequentemente tardio e incidental, apresentando um diâmetro médio de 6 cm no momento do diagnóstico91. Presumivelmente tem inicialmente uma natureza sólida e sofre degenerescência progressiva, acabando por assumir uma aparência quística. É geralmente hipoecóica, de ecotextura heterogénea e bem delimitada (cápsula fibrosa). É maligna em 10-15% dos casos e pode sofrer metastização, embora o envolvimento ganglionar seja excecional92. O estudo citopatológico por PAAF-EE é habitualmente diagnóstico, ao revelar um aspeto papilar ramificado com estroma mixoide, havendo imunomarcação para o CD 56 e vimentina. Está recomendada a sua resseção cirúrgica.
Pancreatite crónica
A EE tem um papel importante no diagnóstico de pancreatite crónica, sobretudo das formas mais ligeiras da doença, que não são identificadas pelos métodos de imagem convencionais e para as quais os testes funcionais pancreáticos apresentam uma sensibilidade relativamente baixa, com a vantagem sobre a colangiopancreatografia retrógrada endoscópica (CPRE) de ser minimamente invasiva. A sua especificidade neste contexto é, contudo, limitada (60%)93-96.
Várias características ultrassonográficas parenquimatosas (focos hiperecóicos com ou sem cone de sombra, faixas hiperecóicas, áreas ou lóbulos hipoecóicos, quistos) e ductais (dilatação ou irregularidade do contorno do ducto pancreático principal, hiperecogenicidade da parede do ducto pancreático principal, dilatação dos ramos secundários, cálculos intraductais) são consideradas preditivas de alterações de pancreatite crónica (tabela 1)97. Permanece controverso o significado de outras características, como a lobularidade das margens do parênquima e a atrofia glandular, esta última frequentemente considerada como critério diagnóstico na TC e na RM.
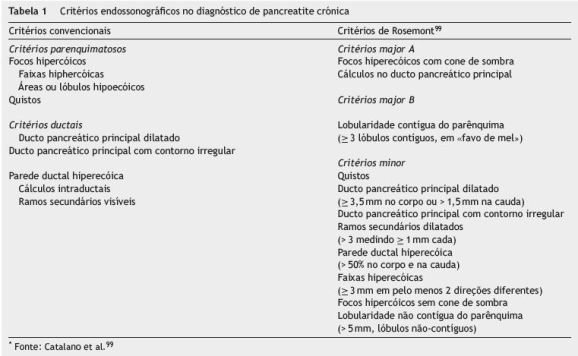
Em geral, a deteção de calcificações parenquimatosas e/ou cálculos intraductais constitui um achado muito específico de pancreatite crónica. Na sua ausência, o diagnóstico depende do número de critérios ultrassonográficos observados (tabela 2). O cut-off mais frequentemente utilizado é a presença de pelo menos 3 critérios para a pancreatite crónica em geral e de pelo menos 7 critérios para a pancreatite crónica moderada a grave, de acordo com classificação de Cambridge (VPP > 85%). A presença de 2 ou menos critérios tem um VPN > 85% para a pancreatite crónica moderada a grave98.

Catalano et al. procuraram avaliar a importância relativa das diferentes características ultrassonográficas no diagnóstico de pancreatite crónica e dividiram-nas em critérios major e minor - classificação de Rosemont (tabelas 1 e 2)99. Este sistema classificativo permite uma melhor estratificação diagnóstica, no entanto, não existem estudos que confirmem a sua superioridade relativamente aos critérios convencionais.
Estudos de concordância intraobservador na interpretação das características ultrassonográficas de pancreatite crónica mostraram resultados superiores aos publicados referentes à CPRE, mas a concordância interobservador é inferior. Os resultados são melhores se considerarmos o diagnóstico final ao invés das características individualmente97,100,101.
A PAAF não aumenta de forma significativa a especificidade dos achados da EE e não é realizada por rotina nos doentes com suspeita de pancreatite crónica. O rendimento diagnóstico da biópsia tru-cut é igualmente baixo e a sua realização não é recomendada dadas as complicações potenciais102. Por isso, nos doentes com probabilidade diagnóstica intermédia/indeterminada deve ser tida em consideração a existência de fatores de risco, como a ingestão alcoólica excessiva, o tabagismo ou a história familiar, e deve ser realizado um estudo complementar com colangiografia por ressonância magnética (CPRM), testes funcionais pancreáticos ou CPRE. Em conjunto, a EE e a CPRM com administração de secretina constituem a melhor combinação de acuidade e segurança, apresentando uma sensibilidade de 98% (quando pelo menos um dos testes não é normal) e uma especificidade de 100% (quando existem alterações em ambos os testes) no diagnóstico de pancreatite crónica94. A deteção precoce da pancreatite crónica permite atuar sobre as suas causas e com isso prevenir ou pelo menos atrasar a evolução da doença, e atuar sobre a sintomatologia do doente.
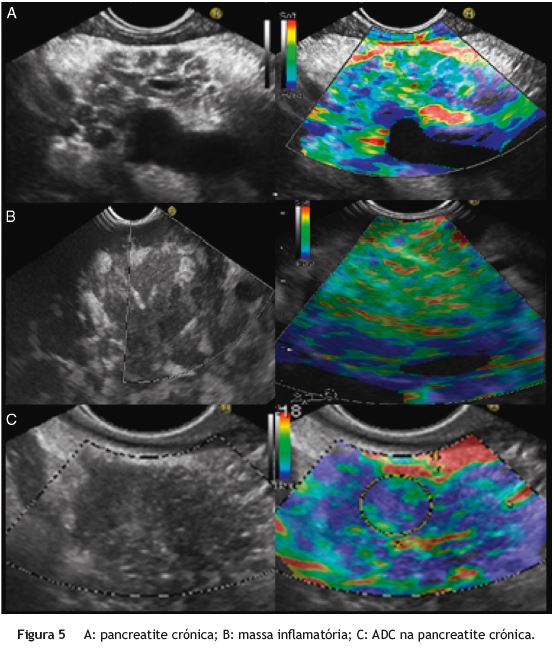
Episódios de agudização de pancreatite crónica ou fenómenos de pancreatite focal podem resultar na formação de uma massa inflamatória pseudotumoral, indistinguível do ADC do pâncreas nos exames de imagem. Embora seja superior à TC e à RM, a EE apresenta uma acuidade baixa na diferenciação entre lesões sólidas benignas e malignas, particularmente nos doentes com pancreatite crónica avançada, devido à sobreposição dos achados ultrassonográficos nas 2 condições clínicas, ou com pancreatite crónica calcificante, uma vez que a sombra acústica produzida pelas calcificações pode obscurecer parcialmente a glândula. A PAAF aumenta a acuidade global da técnica, mas a sensibilidade para malignidade é inferior nos doentes com pancreatite crónica (54-74%) comparativamente com aqueles em que o restante parênquima pancreático é normal (89-91%). Além disso, o número médio de passagens necessárias para estabelecer o diagnóstico definitivo é superior no primeiro grupo de doentes103-106. A introdução da elastografia e dos agentes de contraste aplicados à EE poderá vir a ser particularmente importante neste contexto (fig. 5)32,35.
Encontra-se atualmente em debate a indicação para vigilância regular dos doentes com pancreatite crónica, pelo facto de esta constituir um fator de risco para carcinoma pancreático107, não existindo até ao momento recomendações formais para rastreio destes doentes, nem evidência de benefício clínico.
Pancreatite aguda
Os achados endossonográficos na pancreatite aguda são variáveis e inespecíficos. O pâncreas pode ter um aspeto normal ou apresentar-se ligeiramente aumentado e hipoecóico devido ao edema, e com áreas focais hipoecóicas indicativas de necrose parenquimatosa. Podem coexistir aspetos de inflamação extrapancreática, como edema da parede duodenal e coleções líquidas peripancreáticas.
Dados preliminares sugerem um papel da EE na avaliação de fatores preditivos da evolução da pancreatite aguda108, mas mais estudos são necessários para confirmação deste potencial valor prognóstico.
Uma das principais aplicações da EE neste contexto é a investigação etiológica da pancreatite aguda idiopática (10%), particularmente na suspeita de etiologia biliar, quando a ultrassonografia abdominal e a TC não documentam a existência de litíase. A EE é comparável à CPRM na deteção de coledocolitíase109,110, mas é superior na deteção de microlitíase (< 3mm) e lama biliar111. Os microcálculos apresentam-se como focos hiperecóicos flutuantes, sem cone de sombra, e a lama biliar como conteúdo ecóico móvel no interior da vesícula ou da via biliar. Tem vindo a ser sugerida uma abordagem baseada na EE para seleção dos doentes candidatos a CPRE e papilotomia, com o objetivo de reduzir o risco de complicações. No entanto, os dados que suportam a adoção desta estratégia de triagem no contexto da pancreatite aguda são, ainda, limitados112.
A EE apresenta, adicionalmente, uma elevada sensibilidade na identificação de causas menos frequentes de pancreatite aguda, como tumores não visualizados por outros métodos de imagem, sendo que 5-7% dos tumores pancreáticos apresentam-se na forma de pancreatite aguda113, pancreas divisum e pancreatite crónica. As alterações inflamatórias presentes durante o episódio agudo podem prejudicar a aquisição de imagens adequadas do pâncreas, pelo que se recomenda um intervalo de pelo menos 4-6 semanas antes da realização de EE para estas indicações.
O valor da avaliação por EE após um episódio único de pancreatite aguda idiopática permanece controverso. A EE tem um elevado rendimento diagnóstico (30-60%) e uma baixa taxa de complicações114,115, contudo, apenas 20-50% dos doentes desenvolvem sintomas recorrentes116 e pode ser difícil estabelecer uma relação causal entre alguns achados anormais da EE e o episódio de pancreatite aguda. A implementação de uma estratégia baseada na EE na avaliação destes doentes depende, por isso, da disponibilidade da técnica e da experiência do centro. A CPRE e a manometria do esfíncter de Oddi devem ser reservadas para os doentes com pancreatite aguda recorrente e resultados negativos na EE, especialmente se previamente colecistectomizados117.
Pancreatite autoimune
A PAI é uma doença inflamatória do pâncreas que tem vindo a ser reconhecida de forma crescente118. A apresentação clínica é variável (dor abdominal, insuficiência pancreática ou icterícia obstrutiva indolor), e pode mimetizar o carcinoma pancreático, sendo identificada em 3-5% das peças operatórias dos doentes submetidos a duodenopancreatectomia por suspeita tumoral119,120. O diagnóstico requer geralmente um elevado grau de suspeição e é estabelecido com base numa combinação de critérios clínicos, serológicos, imagiológicos e histológicos121-124.
Existem dois tipos de PAI: o tipo 1 ou pancreatite esclerosante linfoplasmocitária, mais comum, e o tipo 2 ou pancreatite crónica ducticêntrica idiopática. A PAI tipo 1 atinge mais frequentemente indivíduos do sexo masculino e com uma idade superior a 50 anos. É considerada uma manifestação pancreática de uma doença autoimune sistémica, podendo cursar com envolvimento de outros órgãos (colangite esclerosante, fibrose retroperitoneal, envolvimento renal, aumento dimensional das glândulas salivares) e com a presença de autoanticorpos séricos, que são inespecíficos. A maioria dos doentes apresenta títulos elevados de IgG4. Contudo, elevação destes títulos pode ser observada em doentes com outras patologias pancreáticas. Gahzaale et al. investigaram o papel diagnóstico da IgG4 na PAI e reportaram uma sensibilidade de 76%, uma especificidade de 93% e um VPP de 36% para um cut-off de 140 mg/dL; se o cut-off for 280 mg/dl a sensibilidade desce para 53%, mas a especificidade e o VPP sobem para 99 e 75%, respetivamente125. Histopatologicamente, o pâncreas apresenta um denso infiltrado inflamatório periductal constituído sobretudo por linfócitos e plasmócitos IgG4-positivos, marcada fibrose intersticial, graus variáveis de atrofia acinar e lesões de flebite obliterativa. A PAI tipo 2 atinge doentes de ambos os sexos em igual proporção e com um maior espectro de idades. Com frequência, os níveis séricos de IgG4 são normais. Morfologicamente caracteriza-se pela existência de lesões epiteliais granulocíticas. Está descrita uma associação com a doença inflamatória intestinal, que está presente em 16% dos doentes126.
Classicamente, os métodos de imagem seccionais mostram um pâncreas focal ou difusamente aumentado e de aspeto «pseudocapsulado». O estudo por CPRM/CPRE revela um wirsung de calibre estreito e irregular, com uma ou mais estenoses segmentares. Características semelhantes são observadas na EE em que o pâncreas se apresenta focal ou difusamente aumentado, hipoecóico/com margens hipoecóicas e sem dilatação do sistema ductal127,128. Uma massa inflamatória focal hipoecóica pode estar presente, localizada mais frequentemente na porção cefálica e com um aspeto ultra-sonográfico indistinguível do ADC, por vezes associada à presença de uma estenose da porção intrapancreática da via biliar e adenopatias peripancreáticas.
A PAI deve ser incluída no diagnóstico diferencial dos doentes com uma lesão sólida do pâncreas, por forma a evitar uma resseção cirúrgica desnecessária. A PAAF-EE é particularmente útil para excluir malignidade129,130 e pode estabelecer o diagnóstico definitivo de PAI ao permitir obter amostras de tamanho adequado para avaliação histopatológica e análise imuno-histoquímica131. De outro modo, a presença de fragmentos de estroma de elevada celularidade com um infiltrado linfocitário pode, em conjunto com os dados clínicos e os achados radiológicos, sugerir o diagnóstico de PAI.
Nos casos em que a PAAF-EE é negativa para malignidade e em que não é possível estabelecer o diagnóstico definitivo de PAI, a elastografia-EE e o contraste-EE podem contribuir para alterar o algoritmo de decisão: caracteristicamente, na PAI a elastografia mostra um padrão único de dureza homogénea de todo o órgão, distinguindo-se do padrão de dureza homogénea circunscrito à lesão nos doentes com ADC do pâncreas132, e o estudo com contraste revela um padrão de hipervascularização difusa, enquanto as lesões de ADC são hipocaptantes133.
Se o conjunto dos dados clínicos e morfológicos suportarem o diagnóstico de PAI, pode-se considerar a realização de uma prova terapêutica com corticosteroides (0,5 mg/Kg de prednisona durante 2 semanas). No entanto, esta conduta não é geralmente recomendada e só deve ser adotada por pancreatologistas em doentes cuidadosamente selecionados e após uma investigação diagnóstica negativa para malignidade que inclua a realização de PAAF-EE122,124.
Conclusão
Apesar do contínuo desenvolvimento tecnológico dos métodos de imagem seccionais, a EE continua a deter um papel importante na abordagem diagnóstica da patologia pancreática benigna e maligna.
A EE está indicada na deteção de tumores pancreáticos de pequenas dimensões, insuficientemente identificados por TC ou RM, na localização pré-operatória de TNE pancreáticos, e na caracterização cito-histológica tumoral, quando indicada. O valor da PAAF-EE na diferenciação entre lesões sólidas benignas e malignas é indiscutível, mas permanece controversa a sua necessidade na avaliação pré-operatória dos doentes com suspeita de ADC pancreático. No momento atual, a PAAF-EE está formalmente indicada nos doentes propostos para terapêutica paliativa ou sempre que se considere a possibilidade de realizar terapêutica neoadjuvante. A EE como indicação para o estadiamento loco-regional também permanece controversa, como consequência de resultados inconsistentes e evidência contraditória, estando longe de ser consensual.
As neoplasias quísticas, cada vez mais detetadas, têm significativas diferenças no potencial de malignidade. A EE contribui de forma significativa para a sua diferenciação, de acordo com detalhes estruturais e com as características do fluido quístico obtido por PAAF-EE. No entanto, continua incerta a abordagem mais adequada dos pequenos quistos assintomáticos e incidentalmente identificados. O desconhecimento da história natural de alguns subtipos de lesões quísticas condicionam a prática clínica e a consensualidade dos algoritmos de abordagem.
A EE é mais sensível que a CPRM e igualmente sensível, mas mais segura que a CPRE na deteção de alterações subtis nas formas ligeiras de pancreatite crónica, contribuindo de forma decisiva para o diagnóstico precoce desta entidade, que é desafiante. Representa, além disso, a modalidade com maior acuidade no diagnóstico de microlitíase biliar e pode ter impacto na abordagem de doentes com pancreatite aguda idiopática, permitindo selecionar os doentes que beneficiarão da realização de CPRE. Nos casos de suspeita de PAI a EE pode acrescentar informação útil, ao demonstrar características morfológicas sugestivas e um padrão elastográfico e de captação de contraste típicos da doença, e deve ser utilizada para excluir malignidade por PAAF.
As potencialidades da EE neste âmbito poderão vir a ser ampliadas com a aplicação da elastografia e os agentes de contraste.
Atualmente, o maior desafio na área da EE pancreática é a expansão do seu potencial terapêutico, a ser abordado na parte III desta sequência de artigos de revisão.
Bibliografia
1. Wiersema MJ, Vilmann P, Giovaninni M, Chang KJ, Wiersema LM. Endosonography-guided fine-needle aspiration biopsy: Diagnostic accuracy and complication assessment. Gastroenterology. 1997;112:1087-95. [ Links ]
2. Al-Haddad M, Wallace MB, Woodward TA, Gross SA, Hodgens CM, Toton RD, et al. The safety of fine-needle aspiration guided by endoscopic ultrasound: A prospective study. Endoscopy. 2008;40:204-8. [ Links ]
3. Müller MF, Meyenberger C, Bertschinger P, Schaer R, Marincek B. Pancreatic tumors: Evaluation with endoscopic US, CT, and MR imaging. Radiology. 1994;190:745-51. [ Links ]
4. Rosch T, Lorenz R, Braig C, Feuerbach S, Siewert JR, Schusdziarra V, et al. Endoscopic ultrasound in pancreatic tumor diagnosis. Gastrointest Endosc. 1991;37:347-52. [ Links ]
5. Midwinter MJ, Beveridge, Wilsdon JB, Benett MK, Baudoi CJ, Charnley EM. Correlation between spiral computed tomography, endoscopic ultrasonography and findings at operation in pancreatic and ampullary tumors. Br J Surg. 1999;86:189-93.
6. Dewitt J, Devereaux BM, Lehman GA, Sherman S, Imperiale TF. Comparison of endoscopic ultrasound and computed tomography for the preoperative evaluation of pancreatic cancer: A systematic review. Clin Gastroenterol Hepatol. 2006;4:717-25. [ Links ]
7. Uehara H, Ikezawa K, Kawada N, Fukutake N, Katayama K, Takakura R, et al. Diagnostic accuracy of endoscopic ultrasound-guided fine needle aspiration for suspected pancreatic malignancy in relation to the size of lesions. J Gastroenterol Hepatol. 2011;26:1256-61. [ Links ]
8. Klapman JB, Chang KJ, Lee JG, Nguyen P. Negative predictive value of endoscopic ultrasound in a large series of patients with a clinical suspicion of pancreatic cancer. Am J Gastroenterol. 2005;100:2658-61. [ Links ]
9. Fusaroli P, Kypraios D, Caletti G, Eloubeidi MA. Pancreaticobiliary endoscopic ultrasound: A systematic review of the levels of evidence, performance and outcomes. World J Gastroenterol. 2012;18:4243-56. [ Links ]
10. Soriano A, Castells A, Ayuso C, Ayuso JR, de Caralt MT, Ginès MA, et al. Preoperative staging and tumor resectability assessment of pancreatic cancer: Prospective study comparing endoscopic ultrasonography, helical computed tomography, magnetic resonance imaging, and angiography. Am J Gastroenterol. 2004;99:492-501. [ Links ]
11. Miller FH, Rini NJ, Keppke AL. MRI of adenocarcinoma of the pancreas. Am J Roentgenol. 2006;187:W365-74. [ Links ]
12. Tang S, Huang G, Liu J, Liu T, Treven L, Song S, et al. Usefulness of 18F-FDG PET, combined FDG-PET/CT and EUS in diagnosing primary pancreatic carcinoma: A meta-analysis. Eur J Radiol. 2011;78:142-50. [ Links ]
13. Farma JM, Santillan AA, Melis M, Walters J, Belinc D, Chen DT, et al. PET/CT fusion scan enhances CT staging in patients with pancreatic neoplasms. Ann Surg Oncol. 2008;15:2465-71. [ Links ]
14. Pestalozzi BC, Clavien PA, Hany TF. Contrast-enhanced 18F-FDG PET/CT: 1-stop-shop imaging for assessing the resectability of pancreatic cancer. J Nucl Med. 2008;49: 1408-13. [ Links ]
15. Asagi A, Ohta K, Nasu J, Tanada M, Yamamoto K, Inoue T, et al. Utility of contrast-enhanced FDG-PET/CT in the clinical management of pancreatic cancer: Impact on diagnosis, staging, evaluation of treatment response, and detection of recurrence. Pancreas. 2013;42:11-9. [ Links ]
16. Pakzad F, Groves AM, Ell PJ. The role of positron emission tomography in the management of pancreatic cancer. Semin Nucl Med. 2006;36:248-56. [ Links ]
17. Michl P, Pauls S, Gress TM. Evidence-based diagnosis and staging of pancreatic cancer. Best Pract Res Clin Gastroenterol. 2006;20:227-51. [ Links ]
18. Wegener M, Pfaffenbach B, Adamek RJ. Endosonographically guided transduodenal and transgastral fine-needle aspiration puncture of focal pancreatic lesions. Bildgebung. 1995;62:110-5. [ Links ]
19. Dewitt J, Jowell P, Leblanc J, McHenry L, McGreevy K, Cramer H, et al. EUS-guided FNA of pancreatic metastases: A multicentre experience. Gastrointest Endosc. 2005;61:689-96. [ Links ]
20. Hewitt MJ, McPhail MJ, Possamai L, Dhar A, Vlavianos P, Monahan KJ. EUS-guided FNA for diagnosis of solid pancreatic neoplasms: A meta-analysis. Gastrointest Endosc. 2012;75:319-31. [ Links ]
21. Eloubeidi MA, Varadarajulu S, Desai S, Wilcox CM. Value of repeat endoscopic ultrasound-guided fine needle aspiration for suspected pancreatic cancer. J Gastroenterol Hepatol. 2008;23:567-70. [ Links ]
22. Hartwig W, Schneider L, Diener MK, Bergmann F, Büchler MW, Werner J. Preoperative tissue diagnosis for tumours of the pancreas. Br J Surg. 2009;96:5-20. [ Links ]
23. Hébert-Magee S, Bae S, Varadarajulu S, Ramesh J, Forst AR, Eloubeidi MA, et al. The presence of a cytopathologist increases the diagnostic accuracy of endoscopic ultrasound-guided fine needle aspiration cytology for pancreatic adenocarcinoma: A meta-analysis. Cytopathology. 2013;24: 159-71. [ Links ]
24. Olson MT, Ali SZ. Cytotechnologist on-site evaluation of pancreas fine needle aspiration adequacy: Comparison with cytopathologists and correlation with the final interpretation. Acta Cytol. 2012;56:340-6. [ Links ]
25. Erickson RA, Sayage-Rabie L, Beissner RS. Factors predicting the number of EUS guided fine needle passes for diagnosis of pancreatic malignancies. Gastrointest Endosc. 2000;51:184-90. [ Links ]
26. Iglesias-Garcia J, Dominguez-Munoz JE, Abdulkader I, Larino- Noia J, Eugenyeva E, Lozano-Leon A, et al. Influence of on-site cytopathology evaluation on the diagnostic accuracy of endoscopic ultrasound-guided fine needle aspiration (EUS-FNA) of solid pancreatic masses. Am J Gastroenterol. 2011;106:1705-10. [ Links ]
27. Madhoun MF, Wani SB, Rastogi A, Early D, Gaddam S, Tierney WM, et al. The diagnostic accuracy of 22-gauge and 25-gauge needles in endoscopic ultrasound-guided fine needle aspiration of solid pancreatic lesions: A meta-analysis. Endoscopy. 2013;45, 86-82. [ Links ]
28. Affolter KE, Schmidt RL, Matynia AP, Adler DG, Factor RE. Needle size has only a limited effect on outcomes in EUS-guided fine needle aspiration: A systematic review and meta-analysis. Dig Dis Sci. 2013;58:1026-34. [ Links ]
29. Bang JY, Hebert-Magee S, Trevino J, Ramesh J, Varadarajulu S. Randomized trial comparing the 22-gauge aspiration and 22-gauge biopsy needles for EUS-guided sampling of solid pancreatic mass lesions. Gastrointest Endosc. 2012;76:321-7. [ Links ]
30. Iglesias-Garcia J, Abdulkader I, Larino-Noia J. Differential diagnosis of solid pancreatic masses: Do ProCore histology needles improve the diagnostic yield of standard cytology needles? Gastrointest Endosc. 2012;75:AB203. [ Links ]
31. Iglesias-Garcia J, Larino-Noia J, Abdulkader I, Forteza J, Enrique Dominguez-Munoz J. EUS elastography for the characterization of solid pancreatic masses. Gastrointest Endosc. 2009;70:1101-8. [ Links ]
32. Saftoiu A, Vilmann P, Gorunescu F, Janssen J, Hocke M, Larsen M, et al. Accuracy of endoscopic ultrasound elastography used for differential diagnosis of focal pancreatic masses: A multicenter study. Endoscopy. 2011;43:596-603. [ Links ]
33. Ishikawa T, Itoh A, Kawashima H, Ohno E, Matsubara H, Itoh Y, et al. Usefulness of EUS combined with contrast-enhancement in the differential diagnosis of malignant versus benign and preoperative localization of pancreatic endocrine tumors. Gastrointest Endosc. 2010;71:951-9. [ Links ]
34. Gong T, Hu D, Zhu Q. Contrast-enhanced EUS for differential diagnosis of pancreatic mass lesions: A meta-analysis. Gastrointest Endosc. 2012;76:301-9. [ Links ]
35. Napoleon B, Alvarez-Sanchez MV, Gincoul R, Pujol B, Lefort C, Lepilliez V, et al. Contrast-enhanced harmonic endoscopic ultrasound in solid lesions of the pancreas: Results of a pilot study. Endoscopy. 2010;42:564-70. [ Links ]
36. Giovannini M, Thomas B, Erwan B, Christian P, Fabrice C, Benjamin E, et al. Endoscopic ultrasound elastography for evaluation of lymph nodes and pancreatic masses: A multicenter study. World J Gastroenterol. 2009;15:1587-93. [ Links ]
37. Buthani MS, Hawes RH, Hoffman BJ. A comparison of the accuracy of echo features during endoscopic ultrasound (EUS) ans EUS-guided fine-needle aspiration for diagnosis of malignant lymph node invasion. Gastrointes Endosc. 1997;45: 474-9. [ Links ]
38. Buchs NC, Chilcott M, Poletti PA, Buhler LH, Morel P. Vascular invasion in pancreatic cancer: Imaging modalities, preoperative diagnosis and surgical management. World J of Gastroenterol. 2010;16:818-31. [ Links ]
39. Heinemann V, Haas M, Boeck S. Neoadjuvant treatment of borderline resectable and non-resectable pancreatic cancer. Annals of Oncology. 2013. Epub ahead of print. [ Links ]
40. Loeser C, Romagnuolo J, Hawes R, Hoffman B, Nelson R, Morse M, et al. EUS compared with ct for restaging of pancreatic cancer after neoadjuvant therapy. Gastrointestinal Endosc. 2011;73, 4SAB252. [ Links ]
41. Sugiyama M, Abe N, Izumisato Y, Yamaguchi Y, Yamato T, Tokuhara M, et al. Differential diagnosis of benign versus malignant nonfunctioning islet cell tumors of the pancreas: The roles of EUS and ERCP. Gastrointest Endosc. 2002;55:115-9. [ Links ]
42. Dumonceau JM, Polkowski M, Larghi A, Vilmann P, Giovannini M, Frossard JL, et al. Indications, results, and clinical impact of endoscopic ultrasound (EUS)-guided sampling in gastroenterology: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline. Endoscopy. 2011;43:897-912. [ Links ]
43. Rosch T, Lightdale CJ, Botet JF, Boyce GA, Sivak MV, Yasuda K, et al. Localization of pancreatic endocrine tumors by endoscopic ultrasonography. N Engl J Med. 1992;326:1721-6. [ Links ]
44. Sotoudehmanesh R, Hedayat A, Shirazian N, Shahraeeni S, Ainechi S, Zeinali F, et al. Endoscopic ultrasonography (EUS) in the localization of insulinoma. Endocrine. 2007;31: 238-41. [ Links ]
45. de Angelis C, Repici A, Arena V, Pellicano R, Rizzetto M. Preoperative endoscopic ultrasonography in decision making and management for pancreatic endocrine tumors: A 6-year experience. Endoscopy. 1998;30:A182-6. [ Links ]
46. Schumacher B, Lübke HJ, Frieling T, Strohmeyer G, Starke AA. Prospective study on the detection of insulinomas by endoscopic ultrasonography. Endoscopy. 1996;28:273-6. [ Links ]
47. Anderson MA, Carpenter S, Thompson NW, Nostrant TT, Elta GH, Scheiman JM. Endoscopic ultrasound is highly accurate and directs management in patients with neuroendocrine tumors of the pancreas. Am J Gastroenterol. 2000;95:2271-7. [ Links ]
48. McLean AM, Fairclough PD. Endoscopic ultrasound in the localisation of pancreatic islet cell tumors. Best Pract Res Clin Endocrinol Metab. 2005;19:177-93. [ Links ]
49. Zimmer T, Stolzel U, Bader M, Koppenhagen K, Hamm B, Buhr H, et al. Endoscopic ultrasonography and somatostatin receptor scintigraphy in the preoperative localisation of insulinomas and gastrinomas. Gut. 1996;39:562-8. [ Links ]
50. de Angelis C, Pellicano R, Rizzetto M, Repici A. Role of endoscopy in the management of gastroenteropancreatic neuroendocrine tumours. Minerva Gastroenterol Dietol. 2011;57:129-37. [ Links ]
51. Merkle EM, Bender GN, Brambs HJ. Imaging findings in pancreatic lymphoma: Differential aspects. AJR Am J Roentgenol. 2000;174:671-5. [ Links ]
52. Behrns KE, Sarr MG, Strickler JG. Pancreatic lymphoma: is it a surgical disease? Pancreas. 1994;9:662-7. [ Links ]
53. Flamenbaum M, Pujol B, Souquet JC, Cassan P. Endoscopic ultrasonography of a pancreatic lymphoma. Endoscopy. 1998;30:S43. [ Links ]
54. Cario E, Rünzi M, Metz K, Layer P, Goebell H. Diagnostic dilemma in pancreatic lymphoma. Int J Pancreatol. 1997;22:67-71. [ Links ]
55. Oliva E, Álvarez T, Young RH. Acinar cell carcinoma of the pancreas: A clinicopathologic and immunohistochemical study. Am J Surg Pathol. 2005;29:143-56. [ Links ]
56. Stelow EB, Bardales RH, Shami VM, Woon C, Presley A, Mallery S, et al. Cytology of pancreatic acinar cell carcinoma. Diagn Cytopathol. 2006;34:367-72. [ Links ]
57. Eidt S, Jergas M, Schmidt R, Siedek M. Metastasis to the pâncreas ---- an indication for pancreatic resection? Langenbecks Arch Surg. 2007;392:539-42. [ Links ]
58. Tsitouridis I, Diamantopoulou A, Michaelides M, Arvanity M, Papaioannou S. Pancreatic metastases: CT and MRI findings. Diagn Interv Radiol. 2010;16:45-51. [ Links ]
59. Rubenstein JH, Scheiman JM, Anderson MA. A clinical and economic evaluation of endoscopic ultrasound for patients at high risk for familial pancreatic adenocarcinoma. Pancreatology. 2007;7:514-25. [ Links ]
60. Langer P, Kann PH, Fendrich V, Habbe N, Schneider M, Sina M, et al. Five years of prospective screening of high-risk individuals from families with familial pancreatic cancer. Gut. 2009;58:1410-8. [ Links ]
61. Canto MI, Goggins M, Hruban RH, Petersen GM, Giardiello FM, Yeo C, et al. Screening for early pancreatic neoplasia in high.risk individuals: A prospective controlled study. Clin Gastroenterol Hepatol. 2006;4:766-81. [ Links ]
62. Canto MI, Harinck F, Hruban RH, Offerhaus GJ, Poley JW, Kamel I, et al. International Cancer of the Pancreas Screening (CAPS) Consortium summit on the management of patients with increased risk for familial pancreatic cancer. Gut. 2013;62:339-47. [ Links ]
63. Ip IK, Mortele KJ, Prevedello LM, Khorasani R. Focal cystic pancreatic lesions: Assessing variation in radiologists management recommendations. Radiology. 2011;259:136-41. [ Links ]
64. Laffan TA, Horton KM, Klein AP, Berlanstein B, Siegelman SS, Kawamoto S, et al. Prevalence of unsuspected pancreatic cysts on MDCT. Am J Roentgenol. 2008;191(3):802-7. [ Links ]
65. de Jong K, Nio CY, Mearadji B, Phoa SS, Engelbrecht MR, Dijkgraaf MG, et al. Disappointing interobserver agreement among radiologists for a classifying diagnosis of pancreatic cysts using magnetic resonance imaging. Pancreas. 2012;41(2):278-82. [ Links ]
66. Kimura W, Nagai H, Kuroda A, Muto T, Esakit Y. Analysis of small cystic lesions of the pancreas. Int J Pancreatol. 1995;18:197-206. [ Links ]
67. Simeone DM. SSAT/AGA/ASGE state of the art conferenceon cystic neoplasms of the pancreas. J Gastrointest Surg. 2008;12:1475-7. [ Links ]
68. Kosmahl M, Pauser U, Peters K, Sipos B, Lüttges J, Kremer B, et al. Cystic neoplasms of the pancreas and tumor-like lesions with cystic features: A review of 418 cases and a classification proposal. Virchows Arch. 2004;445:168-78. [ Links ]
69. Bosman FT, Carneiro F, Hruban RH, Theise ND. WHO classification of tumors of the digestive system. 4 th ed. Lyon: International Agency for Research on Cancer; 2010. [ Links ]
70. Tanaka M, Chari S, Adsay V, Castillo CF, Falconi M, Shimizu M, et al. International consensus guidelines for management of intraductal papillary mucinous neoplasms and mucinous cystic neoplasms of the pancreas. Pancreatology. 2006;6:17-32. [ Links ]
71. Ahmad NA, Kochman ML, Brensinger C, Brugge WR, Faigel DO, Gress FG, et al. Interobserver agreement among endosonographers for the diagnosis of neoplastic versus non-neoplastic pancreatic cystic lesions. Gastrointest Endosc. 2003;58:59-64. [ Links ]
72. Park WG, Mascarenhas R, Palaez-Luna M, Smyrk TC, OKane D, Clain JE, et al. Diagnostic performance of cyst fluid carcinoembryonic antigen and amylase in histologically confirmed pancreatic cysts. Pancreas. 2011;40:42-5. [ Links ]
73. Cizginer S, Turner B, Bilge AR, Karaca C, Pitman MB, Brugge WR. Cyst fluid carcinoembryonic antigen is an accurate diagnostic marker of pancreatic mucinous cysts. Pancreas. 2011;40:1024-8. [ Links ]
74. Polkowsk Mi, Larghi A, Weynand B, Boustière C, Giovannin M, Pujol B, et al. Learning, techniques, and complications of endoscopic ultrasound (EUS)-guided sampling in gastroenterology: European Society of Gastrointestinal Endoscopy (ESGE) Technical Guideline. Endoscopy. 2012;44:190-205. [ Links ]
75. Singhal D, Kakodkar R, Sud R, Chaudhary A. Issues in management of pancreatic pseudocysts. JOP. 2006;7:502-7. [ Links ]
76. Gonzalez OE, Murphy E, Brugge W, Deshpande V. Pseudocyst of the pancreas: The role of cytology and special stains for mucin. Cancer. 2009;117:101-7. [ Links ]
77. Valsangkar NP, Morales-Oyarvide V, Thayer SP, Ferrone CR, Wargo JA, Warshaw, et al. 851 resected cystic tumors of the pancreas: A 33-year experience at the Massachusetts General Hospital. Surgery. 2012;152(1):S4-12.
78. Lee L, Clancy T, Kadiyala V, Suleiman S, Conwell DL. Interdisciplinary management of cystic neoplasms of the pancreas. Gastroenterol Res Pract. 2012. Article 513163. [ Links ]
79. Kubo H, Nakamura K, Itaba S, Yoshinaga S, Kinukawa N, Sadamoto Y, et al. Differential diagnosis of cystic tumors of the pancreas by endoscopic ultrasonography. Endoscopy. 2009;41:684-9. [ Links ]
80. OToole D, Palazzo L, Hammel P, Ben Yaghlene L, Couvelard A, Felce-Dachez M, et al. Macrocystic pancreatic cystadenoma: The role of EUS and cyst fluid analysis in distinguishing mucinous and serous lesions. Gastrointest Endosc. 2004;59:823-9. [ Links ]
81. Petrone MC, Arcidiacono PG. Role of endosocopic ultrasound in the diagnosis of cystic tumours of the pancreas. Dig Liver Dis. 2008;40:847-53. [ Links ]
82. Sakorafas GH, Smyriniotis V, Reid-Lombardo KM, Sarr MG. Primary pancreatic cystic neoplasms revisited: Part II. Mucinous cystic neoplasms. Surgical Oncology. 2011;20:e93-101. [ Links ]
83. Crippa S, Salvia R, Warshaw AL, Dominguez I, Bassi C, Falconi M, et al. Mucinous cystic neoplasm the pancreas is not an aggessive entity: Lessons from 163 resected patients. Ann Surg. 2008;247:571-9. [ Links ]
84. Barresi L, Tarantino I, Granata A, Curcio G, Traina M. Pancreatic cystic lesions: How endoscopic ultrasound morphology and endoscopic ultrasound fine needle aspiration help unlock the diagnostic puzzle. World J Gastrointest Endosc. 2012;16:247-59. [ Links ]
85. Rockacy M, Khalid A. Update on pancreatic cyst fluid analysis. Annals of Gastroenterology. 2012;26:1-6. [ Links ]
86. Yoon WJ, Brugge WR. Pancreatic cystic neoplasms: Diagnosis and management. Gastroenterol Clin North Am. 2012;41:103-18. [ Links ]
87. Jennifer E, Verbesey JE, Munson JL. Pancreatic cystic neoplasms. Surg Clin North Am. 2010;90:411-25. [ Links ]
88. Hutchins GF, Draganov PV. Cystic neoplasms of the pancreas: A diagnostic challenge. World J Gastroenterol. 2009;15:48-54. [ Links ]
89. Tanaka M, Castillo FC, Adsay V, Chari S, Falconi M, Jang JY, et al. International consensus guidelines 2012 for the management of IPMN and MCN of the pancreas. Pancreatology. 2012;12:183-97. [ Links ]
90. Martin RC, Klimstra DS, Brennan MF, Conlon KC. Solidpseudopapillary tumor of the pancreas: A surgical enigma? Ann Surg Oncol. 2002;9:35-40. [ Links ]
91. Papavramidis T, Papavramidis S. Solid pseudopapillarytumors of the pancreas: Review of 718 patients reported in english literature. J Am Coll Surg. 2005;200:965-72. [ Links ]
92. Tipton SG, Smyrk TC, Sarr MG, Thompson GB. Malignant potential of solid pseudopapillary neoplasm of the pancreas. Br J Surg. 2006;93:733-7. [ Links ]
93. Hollerbach S, Klamann A, Topalidis T, Schmiegel WH. Endoscopic ultrasonography (EUS) and fine-needle aspiration (FNA) cytology for diagnosis of chronic pancreatitis. Endoscopy. 2001;33:824-31. [ Links ]
94. Pungpapong S, Wallace MB, Woodward TA, Noh KW, Raimondo M. Accuracy of endoscopic ultrasonography and magnetic resonance cholangiopancreatography for the diagnosis of chronic pancreatitis: A prospective comparison study. J Clin Gastroenterol. 2007;41:88-93. [ Links ]
95. Kahl S, Glasbrenner B, Leodolter A, Pross M, Schulz HU, Malfertheiner P. EUS in the diagnosis of early chronic pancreatitis: A prospective follow-up study. Gastrointest Endos. 2002;55:507-11. [ Links ]
96. Clain JE, Person RK. Diagnosis of chronic pancreatitis: Is a gold standard necessary? Surg Clin North Am. 1999;79:829-45. [ Links ]
97. Sahai AV, Zimmerman M, Aabakken L, Tarnasky PR, Cunningham JT, van Velse A, et al. Prospective assessment of the ability of endoscopic ultrasound to diagnose, exclude, or establish the severity of chronic pancreatitis found by endoscopic retrograde cholangiopancreatography. Gastrointest Endosc. 1998;48:18-25. [ Links ]
98. Wiersema MJ, Hawes RH, Lehman GA, Kochman ML, Sherman S, Kopecky KK. Prospective evaluation of endoscopic ultrasonography and endoscopic retrograde cholangiopancreatography in patients with chronic abdominal pain of suspected pancreatic origin. Endoscopy. 1993;25:555-64. [ Links ]
99. Catalano MF, Sahai A, Levy M, Romagnuolo J, Wiersema M, Brugge W, et al. EUS-based criteria for the diagnosis of chronic pancreatitis: The Rosemont classification. Gastrointest Endosc. 2009;69:1251-61. [ Links ]
100. Lieb JG, Palma DT, Garvan CW, Leblanc JK, Romagnuolo J, Farrell JJ, et al. Intraobserver agreement among endosonographers for endoscopic ultrasound features of chronic pancreatitis: A blinded multicenter study. Pancreas. 2011;40:177-80. [ Links ]
101. Wallace MB, Hawes RH, Durkalski V, Chak A, Mallery S, Catalano MF, et al. The reliability of EUS for the diagnosis of chronic pancreatitis: Interobserver agreement among experienced endosonographers. Gastrointest Endosc. 2001;53:294-9. [ Links ]
102. DeWitt J, McGreevy K, LeBlanc J, McHenry L, Cummings O, Sherman S. EUS-guided Trucut biopsy of suspected nonfocal chronic pancreatitis. Gastrointest Endosc. 2005;62: 76-84. [ Links ]
103. Fritscher-Ravens A, Brand L, Knöfel WT, Bobrowski C, Topalidis T, Thonke F, et al. Comparison of endoscopic ultrasound-guided fine needle aspiration for focal pancreatic lesions in patients with normal parenchyma and chronic pancreatitis. Am J Gastroenterol. 2002;97:2768-75. [ Links ]
104. Varadarajulu S, Tamhane A, Eloubeidi MA. Yield of EUS-guided FNA of pancreatic masses in the presence or the absence of chronic pancreatitis. Gastrointest Endosc. 2005;62:728-36. [ Links ]
105. Krishna NB, Mehra M, Reddy AV, Agarwal B. EUS/EUSFNA for suspected pancreatic cancer: Influence of chronic pancreatitis and clinical presentation with or without obstructive jaundice on performance characteristics. Gastrointest Endosc. 2009;70:70-9. [ Links ]
106. Takahashi K, Yamao K, Okubo K, Sawaki A, Mizuno N, Ashida R, et al. Differential diagnosis of pancreatic cancer and focal pancreatitis by using EUS-guided FNA. Gastrointest Endosc. 2005;61:76-9. [ Links ]
107. Lowenfels AB, Maisonneuve P, Cavallini G, Ammann RW, Lankisch PG, Andersen JR, et al. Pancreatitis and the risk of cancer. N Engl J Med. 1993;328:1433-7. [ Links ]
108. Sotoudehmanesh R, Hooshyar A, Kolahdoozan S, Zeinali F, Shahraeeni S, Keshtkar AA. Prognostic value of endoscopic ultrasound in acute pancreatitis. Pancreatology. 2010;10:702-6. [ Links ]
109. Verma D, Kapadia A, Eisen GM, Adler DG. EUS vs MRCP for detection of choledocholithiasis. Gastrointest Endosc. 2006;64:248-54. [ Links ]
110. Ledro-Cano D. Suspected choledocholithiasis: Endoscopic ultrasound or magnetic resonance cholangio-pancreatography? A systematic review. Eur J Gastroenterol Hepatol. 2007;19:1007-11. [ Links ]
111. Kondo S, Isayama H, Akahane M. Detection of common bile duct stones: Comparison between endoscopic ultrasonography, magnetic resonance cholangiography and helical-computedtomographic cholangiography. Eur J Radiol. 2005;54:271-5. [ Links ]
112. Liu CL, Fan ST, Lo CM, Tso WK, Wong Y, Poon RT, et al. Comparison of early endoscopic ultrasonography and endoscopic retrograde cholangiopancreatography in the management of acute biliary pancreatitis: A prospective randomized study. Clin Gastroenterol Hepatol. 2005;3:1238-44. [ Links ]
113. Mujica VR, Barkin JS, Go VL, Study Group Participants. Acute pancreatitis secondary to pancreatic carcinoma. Pancreas. 2000;21:329-32. [ Links ]
114. Yusoff IF, Raymond G, Sahai AV. A prospective comparison of the yield of EUS in primary vs recurrent idiopathic acute pancreatitis. Gastrointest Endosc. 2004;60:673-8. [ Links ]
115. Tandon M, Topazian M. Endoscopic ultrasound in idiopathic acute pancreatitis. Am J Gastroenterol. 2001;96:705-9. [ Links ]
116. Gullo L, Migliori M, Pezzilli R, Olah A, Farkas G, Levy P, et al. Na update on recurrent acute pancreatitis: Data from five European countries. Am J Gastroenterol. 2002;97:1959-62.
117. Wilcox MC, Varadarajulu S, Eloubeidi M. Role of endoscopic evaluation in idiopathic pancreatitis: A systematic review. Gastrointest Endosc. 2006;63:1037-45. [ Links ]
118. Sah RP, Pannala R, Chari ST, Sugumar A, Clain JE, Levy MJ, et al. Prevalence, diagnosis and profile of autoimmune pancreatitis presenting with features of acute or chronic pancreatitis. Clin Gastroenterol Hepatol. 2010;8:91-6. [ Links ]
119. Lara LP, Chari ST. Autoimmune pancreatitis. Curr Gastroenterol Rep. 2005;7:101-6. [ Links ]
120. Wolfson D, Barkin JS, Chari ST, Clain JE, Bell Jr RH, Alexakis N, et al. Management of pancreatic masses. Pancreas. 2005;31:203-17. [ Links ]
121. Chari ST, Smyrk TC, Levy MJ, Topazian MD, Takahashi N, Zhang L, et al. Diagnosis of autoimmune pancreatitis: The Mayo Clinic experience. Clin Gastroenterol Hepatol. 2006;4:1010-6. [ Links ]
122. Otsuki M, Chung JB, Okazaki K, Kim MH, Kamisawa T, Kawa S, et al. Asian diagnostic criteria for autoimmune pancreatitis: Consensus of the Japan-Korea Symposium on autoimmune pancreatitis. J Gastroenterol. 2008;43:403-8. [ Links ]
123. Okazaki K, Kawa S, Kamisawa T, Ito T, Inui K, Irie H, et al. Japanese clinical guidelines for autoimmune pancreatitis. Pancreas. 2009;38:849-66. [ Links ]
124. Shimosegawa T, Chari ST, Frulloni L, Kamisawa T, Kawa S, Mino- Kenudson M, et al. International Consensus Diagnostic Criteria for Autoimmune Pancreatitis: Guidelines of the International Association of Pancreatology. Pancreas. 2011;40:352-8. [ Links ]
125. Ghazale A, Chari ST, Smyrk TC, Levy MJ, Topazian MD, Takahashi N, et al. Value of serum IgG4 in the diagnosis of autoimmune pancreatitis and in distinguishing it from pancreatic cancer. Am J Gastroenterol. 2007;102:1646-53. [ Links ]
126. Kamisawa T, Chari ST, Giday SA, Kim MH, Chung JB, Lee KT, et al. Clinical profile of autoimmune pancreatitis and its histological subtypes: An international multicenter survey. Pancreas. 2011;40:809-14. [ Links ]
127. Farrel JJ, Garbel J, Sahani D, Brugge WR. EUS findings in patients with autoimmune pancreatitis. Gastrointest Endos. 2004;60:927-36. [ Links ]
128. Hoki N, Mizuno N, Sawaki A, Tajika M, Takayama R, Shimizu Y, et al. Diagnosis of autoimmune pancreatitis using endoscopic ultrasonography. J Gastroenterol. 2009;44:154-9. [ Links ]
129. Ishikawa T, Itoh A, Kawashima H, Ohno E, Matsubara H, Itoh Y, et al. Endoscopic ultrasound-guided fine needle aspiration in the differentiation of type 1 and type 2 autoimmune pancreatitis. World J Gastroenterol. 2012;18:3883-8. [ Links ]
130. Imai K, Matsubayashi H, Fukutomi A, Uesaka K, Sasaki K, Ono H. Endoscopic ultrasonography-guided fine needle aspiration biopsy using 22-gauge needle in diagnosis of autoimmune pancreatitis. Dig Liver Dis. 2011;43:869-74. [ Links ]
131. Kanno A, Ishida K, Hamada S, Fujishima F, Unno J, Kume K, et al. Diagnosis of autoimmune pancreatitis by EUS-FNA by using a 22-gauge needle based on the International Consensus Diagnostic Criteria. Gastrointest Endosc. 2012;76:594-602. [ Links ]
132. Dietrich CF, Hirche TO, Ott M, Ignee A. Real-time tissue elastography in the diagnosis of autoimmune pancreatitis. Endoscopy. 2009;41:710-20. [ Links ]
133. Hocke M, Ignee A, Dietrich CF. Contrast-enhanced endoscopic ultrasound in the diagnosis of autoimmune pancreatitis. Endoscopy. 2011;43:163-5. [ Links ]
*Autor para correspondência
Correio eletrónico: catarinagr@hotmail.com (C.G. Rodrigues).
Conflito de interesses
Os autores declaram não haver conflito de interesses.
Recebido a 10 de junho de 2013; aceite a 24 de novembro de 2013













