Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Nascer e Crescer
versão impressa ISSN 0872-0754versão On-line ISSN 2183-9417
Nascer e Crescer vol.26 no.4 Porto 2017
ARTIGOS ORIGINAIS | ORIGINAL ARTICLES
Provas de provocação oral a fármacos em Pediatria - casuística 2015
Oral challenge to drugs in Pediatrics – Casuistry 2015
Mónica André CosteiraI; Dinis SousaI; Joana FerreiraI; Carla FerreiraI; Armandina SilvaI; Marta SantalhaI; Paula AlendouroII; Águeda MatosI; Alberto CostaI
I Department of Pediatrics, Hospital da Senhora da Oliveira. 4835-044 Guimarães, Portugal. monicasnacosteira@gmail.com; dinissousa88@gmail.com; joanaferreira.med@gmail.com; carlamf85@hotmail.com; armandinapf@gmail.com; msantalha@gmail.com; aguedaguim@gmail.com; agcosta40@gmail.com
II Department of Immunoallergology, Hospital da Senhora da Oliveira. 4835-044 Guimarães, Portugal. paulalendouro@sapo.pt
RESUMO
Introdução: A suspeita de alergia a fármacos em idade pediátrica é um motivo frequente de consulta, que contudo raramente se confirma. Desta forma, a prova de provocação oral (PPO) assume um papel significativo na abordagem diagnóstica.
Objetivos: Caracterizar a população pediátrica da consulta de um hospital de nível II, que realizou PPO a fármacos, avaliar os fármacos implicados e analisar os casos cujas PPO foram positivas.
Material e métodos: Análise retrospetiva dos processos clínicos dos doentes com idade inferior a 18 anos que realizaram PPO a fármacos no período compreendido entre 1 de janeiro e 31 de dezembro de 2015.
Resultados: A amostra incluiu 58 doentes, 53,4% do sexo masculino, sendo a mediana de idades cinco anos. A maioria foi referenciada a partir do serviço de urgência (39,7%) e da consulta externa (36,2%). A amoxicilina foi o fármaco suspeito em 46,6 %, associada com ácido clavulânico em 34,5%. Cerca de 93,1% apresentaram manifestações mucocutâneas, 5,2% gastrointestinais e mucocutâneas e 1,7% respiratórias e mucocutâneas. Em 20,7 % dos casos as manifestações surgiram nas primeiras 24h. As PPO foram positivas em três doentes e os fármacos responsáveis foram a amoxicilina (dois casos) e o ibuprofeno (um caso).
Conclusões: Sendo a alergia a fármacos rara em crianças e tendo em conta a sua repercussão na decisão terapêutica em casos de situações infeciosas, é de extrema relevância a referenciação para esclarecimento diagnóstico.
Palavras-chave: Alergia; fármacos; prova de provocação oral
ABSTRACT
Introduction: Suspected drug allergy in the pediatric population is a frequent reason for consultation. However, it is rarely confirmed. Thus, the oral challenge (OC) assumes a significant role in the diagnostic approach.
Objectives: Characterize a pediatric population of a level II hospital submitted to OC to drugs, assess which drugs where implicated and analyze the cases in which the OC was positive.
Materials and methods: Clinical records of the patients submitted to OC to drugs in the period of January 1st to December 31st 2015, younger than 18 years.
Results: The sample included 58 patients, 53.4% male. The median age was five years. Most were referred from the emergency room (39.7%) and the outpatient clinic (36.2%). Amoxicillin was the suspected drug in 46.6% and when associated with clavulanic acid in 34.5%. About 93.1% had mucocutaneous manifestations, 5.2% gastrointestinal and mucocutaneous and 1.7% respiratory and mucocutaneous. In 20.7% of the cases, symptoms occurred during the first 24 hours. In three patients the OC was positive and the responsible drug was amoxicillin in two cases and ibuprofen in one.
Conclusions: Allergy to drugs is rare in children but, considering its relevance in the management of infectious situations, it becomes important to refer all suspected cases to clarify the diagnosis.
Keywords: Allergy; drugs; oral challenge
INTRODUÇÃO
A alergia medicamentosa é uma suspeita comum em idade pediátrica, contudo raramente confirmada. A maioria das reações nas crianças é atribuída aos beta-lactâmicos (BL), seguidos pelos anti-inflamatórios não esteroides e antibióticos não BL.1
Estas reações de hipersensibilidade podem ser imediatas ou não imediatas. As imediatas ocorrem habitualmente até uma hora após a toma do fármaco e são mediadas por anticorpos específicos da classe IgE. As não imediatas surgem mais de uma hora após a toma do fármaco e podem ser mediadas por células T.3
O diagnóstico definitivo é importante para instituir o tratamento adequado e as medidas preventivas corretas. A abordagem diagnóstica passa pela realização de uma história clínica completa. Perante suspeita de reação IgE mediada é útil a realização dos testes cutâneos por picada (TC) ou intradérmicos (ID), pesquisa de IgE específicas ou teste de ativação dos basófilos.5,6 Se houver suspeita de reação mediada por células T, justifica-se o teste de ativação dos linfócitos ou testes ID/ epicutâneos de leitura tardia.5-7 Os epicutâneos são especialmente úteis para diagnosticar hipersensibilidade não-imediata a anti-convulsivantes e AINEs. Os TC são pouco sensíveis e os ID são dolorosos e pouco tolerados por crianças pequenas.1
A prova de provocação oral (PPO) assume um papel fundamental no diagnóstico destas situações, permitindo confirmar ou excluir a alergia ao fármaco e encontrar tratamentos alternativos, sendo o gold standard para verificação da tolerância.4 Embora os vários protocolos sejam discutíveis, é consensual que esta prova seja sempre realizada em ambiente hospitalar sob vigilância clínica. Devem ser usadas doses crescentes, com intervalos de tempo variáveis, desde 30 minutos na fase inicial a uma semana. Está preconizado que no caso de reações não imediatas e sem anafilaxia pode ser realizada a PPO, sem realização de testes cutâneos prévios.1
OBJETIVO
Este trabalho teve como objetivo caraterizar a população pediátrica que realizou PPO a fármacos, aprofundando os casos em que as provas foram positivas.
MATERIAL E METÓDOS
Procedemos a uma análise retrospetiva dos processos clínicos dos doentes que realizaram PPO a fármacos no período de 1 de janeiro a 31 de dezembro de 2015. Foram incluídas as seguintes variáveis: sexo, idade, origem da referenciação, antecedentes pessoais de atopia, antecedentes familares de atopia, fármaco(s) suspeito(s), manifestações clínicas, intervalo de tempo entre a toma do fármaco e o início dos sintomas, pesquisa de IgE específicas, realização de testes epicutâneos e/ou intradérmicos, resultado da PPO.
Por se tratar de um estudo retrospetivo, o protocolo utilizado na realização das PPO nesta amostra de doentes foi heterogéneo, não sendo possível uniformizá-lo.
Para análise descritiva dos dados foi utilizado o programa informático Statistical Package for the Social Sciences® (SPSS), versão 22.0.
RESULTADOS
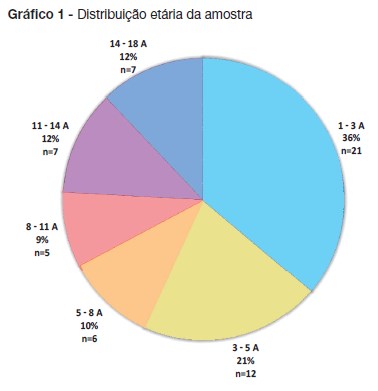
A amostra incluiu 58 doentes, 53,4% do sexo masculino (n=31). A mediana de idades foi cinco anos (idade mínima 1 ano e máxima 17 anos) (gráfico 1).
Foram referenciados ao serviço de urgência 39,7% (n=23), da consulta externa 36,2% (n=21), dos cuidados de saúde primários 22,3% (n=13) e do internamento 1,7% (n=1).
Os antecedentes pessoais de atopia eram positivos em 25,9% (n=15) dos doentes e negativos nos restantes. Os antecedentes familiares de atopia eram positivos na maioria, 48,3% (n= 28), negativos em 41,4 % (n=24) sendo a informação desconhecida em 10,3 % (n=6).
No que diz respeito aos fármacos, a amoxicilina foi o fármaco suspeito em 46,6 % da amostra e a amoxicilina associada a ácido clavulânico em 34,5%. Os restantes fármacos suspeitos foram o ibuprofeno, azitromicina, paracetamol, cefaclor, ceftriaxone, ambroxol, amoxicilina/cotrimoxazol e paracetamol/ibuprofeno (tabela 1).
Grande parte da amostra (93,1% (n= 54)) apresentou manifestações mucocutâneas. A associação de manifestações gastrointestinais e mucocutâneas esteve presente em 5,2% (n=3) dos doentes e a combinação de manifestações respiratórias e mucocutâneas foi encontrada em 1,7% dos casos (n=1) (gráfico 2 e tabela 2). Não houve nenhum caso de anafilaxia.
Em 20,7 % dos casos (n=12) as manifestações surgiram nas primeiras 24 horas, sendo que em 6,9 % dos casos (n =4) a reação ocorreu na primeira hora. A média de dias entre a toma do fármaco e as manifestações clínicas foi de 4,2 dias.
Foram pesquisadas IgE específicas para o fármaco em causa em 25,9 % dos casos (n=15). Todas as IgE específicas pesquisadas foram relativas à amoxicilina, havendo um caso positivo. Em 17,2 % (n=10) foram realizados testes epicutâneos ou ID, tendo havido 1 caso de teste ID que foi positivo para a azitromicina.
Não foram utilizados os TC por picada em nenhum dos doentes.
As PPO foram positivas em 5,2% (n= 3), sendo os fármacos responsáveis pela alergia a amoxicilina e o ibuprofeno (tabela 3).
DISCUSSÃO
As manifestações clínicas na alergia a fármacos podem ser diversas e muitas vezes semelhantes a outras patologias comuns em idade pediátrica, como se verifica nos exantemas bacterianos e víricos.1 O diagnóstico pode tornar-se um verdadeiro desafio, sobretudo em idades mais jovens, em que há maior frequência de exantemas de etiologia infeciosa. Desta forma, é compreensível que a maioria da amostra seja composta por crianças abaixo dos cinco anos.
Os fármacos suspeitos mais comuns foram os antibióticos, nomeadamente os beta-lactâmicos, o que está de acordo com o descrito na literatura.1
As manifestações mucocutâneas foram as mais comuns, sendo a maioria das reações tardias, o que também é compatível com a literatura. O edema facial no caso de alergia ao ibuprofeno está descrito na literatura e é relativamente característico dos AINEs em idade pediátrica.1
A maioria das crianças não fez testes epicutâneos ou pesquisa de IgE específicas séricas, o que é suportado pela literatura.1
A PPO assume um papel fundamental no diagnóstico da alergia medicamentosa. Dos 58 casos suspeitos de alergia medicamentosa este diagnóstico foi excluído em 53 casos. Esta é uma abordagem segura quando realizada em meio hospitalar. Na nossa amostra não houve registo de nenhuma reação grave, nomeadamente anafilaxia.
No caso particular dos doentes com alergia à penicilina, existe um risco aumentado de reações adversas às cefalosporinas, pelo que a sua tolerância também deve ser testada, tal como foi efetuado nos casos apresentados.2
CONCLUSÕES
A verdadeira alergia medicamentosa é rara em idade pediátrica. No nosso estudo, foi comprovada em 5% dos casos pelas PPO. Apesar de rara, a sua suspeita é comum, sobretudo no que diz respeito aos beta-lactâmicos.
As manifestações clínicas são diversas, sendo as reações mais comuns os exantemas maculopapulares não imediatos e a urticária. Deste modo, o principal diagnóstico diferencial é a infeção vírica.
Tendo em conta a repercussão em decisões terapêuticas posteriores, torna-se importante a referenciação destas crianças para esclarecimento diagnóstico. Deste modo, a prova de provocação oral assume um papel essencial na confirmação ou exclusão da hipersensibilidade, sendo aceitável a sua realização mesmo sem testes cutâneos prévios em crianças com exantemas maculopapulares não severos ou urticária não imediata, tal como foi objetivado na presente casuística.
REFERÊNCIAS BIBLIOGRÁFICAS
1. KGomes ER, Brockow K, Kuyucu S, Saretta F, Mori F, Blanca-Lopez N et al. Drug hypersensivity in children: report from the pediatric task force of the EAACI Drug Allergy Interest Group. Allergy 71. 2016; 149-61. [ Links ]
2. Park MA, Koch CA, Klemawesch P, Joshi A, Li JT. Increased adverse drug reactions to cephalosporins in penicilin allergy patients with positive penicillin skin test. Int Arch Allergy Immunol. 2010; 153:268-73. [ Links ]
3. Blanca M, Romano A, Torres MJ, Férnandez J, Mayorga C, Rodriguez J et al. Update on the evaluation of hypersensitivity reactions to betalactams. Allergy 2009; 64:183–93. [ Links ]
4. Demoly P, Adkinson NF, Brockow K, Castells M, Chiriac AM, Greenberger PA et al. International Consensus on drug allergy. Allergy 69. 2014: 420-37. [ Links ]
5. Mayorga C, Celik G, Rouzaire P, Whitaker P, Bonadonna P, Rodrigues-Cernadas J et al. In vitro tests for drug hypersensitivity reactions na ENDA/ EAACI Drug Allergy Interest Group position paper. Allergy 2016; doi: 10.1111/all.12886. [ Links ]
6. Brockow K, Romano A, Blanca M, Ring J, Pichler W, Demoly P et al. General considerations for skin test procedures in the diagnosis of drug hypersensitivity. Allergy 2002; 57:45-51. [ Links ]
7. Romano A, Blanca M, Torres MJ, Bircher A, Aberer W, Brockow K et al. Diagnosis of non imediate reactions to beta-lactam antibiotics. Allergy 2004; 59:1153-60. [ Links ]
8. Demoly P, Romano A, Botelho C, Bousquet-Rouanet L, Gaeta F, Silva R et al. Determining the negative predictive value of provocation tests with beta-lactams. Allergy 65. 2010; 327-32. [ Links ]
CORRESPONDENCE TO
Mónica André Costeira
Department of Pediatrics
Hospital da Senhora da Oliveira
Rua dos Cutileiros, 4835-044 Creixomil, Guimarães
Email: monicasnacosteira@gmail.com
Received for publication: 29.08.2016 Accepted in revised form: 06.03.2017














