Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Arquivos de Medicina
versão On-line ISSN 2183-2447
Arq Med vol.25 no.3 Porto jun. 2011
CASOS CLÍNICOS/ SÉRIE DE CASOS
Metemoglobinemia: Revisão a Propósito de um Caso
Methemoglobinemia: case report and review
Claúdia Carvalho1,2, Natália Ribeiro1, Carlos Lima Alves1,3, Helena Gomes1, António Sarmento1,3
1Serviço de Doenças Infecciosas do Hospital São João, Porto
2Departamento de Higiene e Epidemiologia da Faculdade de Medicina da Universidade do Porto
3Faculdade de Medicina da Universidade do Porto
RESUMO
A metemoglobina é uma forma de hemoglobina caracterizada pela presença do ferro no estado férrico, incapaz de se ligar ao oxigénio. Quando a sua concentração ultrapassa os valores normais podem surgir sintomas decorrentes de uma entrega inadequada de oxigénio aos tecidos. Doentes jovens e sem anemia são geralmente assintomáticos com níveis a inferiores a 15%. Níveis de 20-30% causam sintomas como cefaleias, alteração do estado de consciência, tonturas ou síncope e níveis superiores a 50% podem ser fatais. A metemoglobinemia é na maioria das vezes iatrogénica. A presença de cianose apesar de uma pressão parcial de oxigénio normal na gasometria ou a disparidade entre a saturação arterial de oxigénio medida por oximetria de pulso e por gasometria arterial são pistas importantes para o diagnóstico. O tratamento vai depender sobretudo dos níveis de metemoglobina e da sintomatologia apresentada. Nos casos ligeiros a suspensão do agente oxidante e a administração de oxigénio suplementar são suficientes, mas na presença de sintomas moderados/graves deve considerar-se a utilização de azul-de-metileno e o suporte transfusional. Em casos específicos a cimetidina pode fazer parte das opções terapêuticas. A exsanguinotransfusão e a administração de oxigénio hiperbárico têm sido utilizadas excepcionalmente. Neste trabalho descreve-se um caso de metemoglobinemia secundária a dapsona, utilizada na profilaxia de pneumocistose numa doente com infecção pelo VIH (vírus da imunodeficiência humana) e revêem-se aspectos fundamentais da patofisiologia, etiologia, diagnóstico e tratamento. O nosso objectivo é contribuir para lembrar uma patologia associada a importante morbilidade e potencialmente fatal, para a qual existe tratamento eficaz.
Palavras-chave: metemoglobinemia; dapsona; vih
ABSTRACT
Methemoglobin is a derivative of hemoglobin characterized by the presence of iron in the ferric state, unable to bind oxygen. Methemoglobinemia occurs due to either increased methemoglobin production or decreased reduction and results in a functional anemia that may be fatal. Young and healthy patients who are not anaemic usually have no symptoms if methemoglobin levels are below 15%. levels of 20-30% may cause mental status changes, headache, fatigue, dizziness, and syncope. Levels greater than 50% may result in dysrhythmias, seizures, coma, and death. Acquired methemoglobinemia is a fairly common, yet often unrecognized condition and commonly prescribed drugs are usually implicated. Methemoglobinemia should be considered in the presence of cyanosis despite a normal partial arterial pressure of oxygen (pa O2) or when disparity between different techniques to measure oxygen saturation, namely pulse oximetry and arterial blood gases is detected. Treatment options depend mostly of methemoglobin levels and the severity of symptoms. In mild cases the interruption of the offender may suffice but in symptomatic patients blue methilene and red blood cells transfusion should be considered. Exsanguination and hyperbaric oxygen have been used in exceptionally severe cases. Methemoglobinemia is a potencially fatal condition that can be reverted once diagnosed and treated. We describe a case of methemoglobin secondary to dapsone in a patient infected with HIV. physiopathology, etiology, diagnosis and treatment of methemoglobinemia are reviewed.
Key-words: methemoglobin; dapsone; hiv
Introdução
A metemoglobinemia é uma forma de anemia funcional que pode ser causada por fármacos de prescrição comum, como por exemplo os nitratos, a dapsona e a benzocaína (utilizada como spray anestésico).
Descrição do caso
Doente do sexo feminino, nacionalidade portuguesa, 35 anos de idade, com diagnóstico de infecção VIH em 2005, recorreu a 1 Outubro de 2007 ao Hospital de Dia de Doenças Infecciosas do Hospital são João por um quadro de febre, dispneia progressiva e tosse não produtiva com cinco dias de evolução. A doente havia abandonado terapêutica antiretrovírica cerca de 5 meses antes. Em 4/09/07 a determinação de linfócitos t CD4+ era de 145/mm3. A doente encontrava-se desde há 16 dias medicada com dapsona (100mg peros/dia) para profilaxia de pneumonia por Pneumocystis jirovecii. Apresentava história de alergia a trimetoprim/sulfametoxazol, penicilina, marisco e morangos. Na admissão apresentava-se consciente, colaborante e orientada. pálida. Sem cianose. Pressão arterial: 80/50mmHg, frequência cardíaca:100 bpm, temperatura auricular 39.6ºC, frequência respiratória de 30 cpm. A saturação de oxigénio medida por oximetria de pulso era de 86%. A auscultação cardíaca e pulmonar era normal e o restante exame objectivo não revelava alterações. Com suplementação de oxigénio por máscara de alto débito a doente apresentava saturação de oxigénio de 89% em oximetria de pulso e a gasometria arterial efectuada revelou: pH 7.437, paCO2 31 mmHg, paO2 336 mmHg, saturação O2: 97%. A co-oximetria mostrou uma fracção de metemoglobina (FMethHb) de 11%, oxihemoglobina (FO2Hb) de 86%, desoxihemoglobina (FHHb) de 2,6% e uma fracção de carboxihemoglobina (FCOHb) de 0%. Analiticamente apresentava: hemoglobina 9.5 g/dl, leucócitos 3140/mm3, plaquetas 144000/mm3. A aminotransferese de aspartato (Ast) e a aminotransferese de alanina (Alt) encontravam-se elevadas; 79 U/l e 115U/l respectivamente (normal entre 10-31U/l), bem como a desidrogenase láctica: 489 U/l (normal entre 135 – 225 U/l). Os valores séricos de bilirrubina, ureia e creatinina encontravam-se dentro dos parâmetros da normalidade. A radiografia torácica revelou um infiltrado intersticial bilateral difuso. A doente foi internada com o diagnóstico de presunção de pneumocistose e metemoglobinemia, presumivelmente secundária a dapsona. A doente iniciou tratamento com pentamidina e recebeu suporte transfusional com três unidades de glóbulos rubros. por bradicardia sintomática a terapêutica com pentamidina foi interrompida e a doente completou tratamento de pneumocistose com atovaquona. A confirmação de pneumocistose foi feita pela identificação do Pneumocystis jirovecii por técnica de imunofluorescência em amostras de lavado broncoalveolar. A evolução foi favorável, com redução progressiva da metemoglobinemia para 1% ao 5º dia de internamento. A doente teve alta assintomática e aos seis meses de seguimento mantinha-se assintomática, sob tratamento profiláctico com atovaquona.
Metemoglobina
Definição
Cada subunidade do tetrâmero da molécula de hemoglobina é constituída por uma cadeia de globina e um grupo heme que consiste numa porfirina complexada a um átomo de ferro ferroso (Fe2+). A metemoglobina é um derivado da hemoglobina caracterizada pela presença do ferro no estado férrico (Fe3+) em vez do estado ferroso normal (Fe2+)1.
Formação da metemoglobina
Durante a formação da oxihemoglobina a partir da desoxihemoglobina e de moléculas de oxigénio, um electrão é parcialmente transferido da molécula de ferro para o oxigénio, formando-se um complexo férrico/anião superóxido (Fe3+/O2-). Na reacção de desoxigenação a maior parte do oxigénio abandona o complexo na forma de oxigénio molecular, de modo que o electrão que havia sido emprestado regressa à molécula de ferro. Porém, uma pequena quantidade de oxigénio sai na forma de radical superóxido (O2-), deixando o ferro no estado férrico (metemoglobina). Este processo de auto -oxidação (ilustrado na Figura 1) ocorre espontaneamente em indivíduos normais, convertendo diariamente cerca de 0,5 a 3% da hemoglobina em metemoglobina2,3. A metemoglobina é também gerada em reacções de oxidação em que participam compostos endógenos como o óxido nítrico e peróxido de hidrogénio ou compostos exógenos, por acção directa ou por intermédio de metabolitos.

Redução da metemoglobina
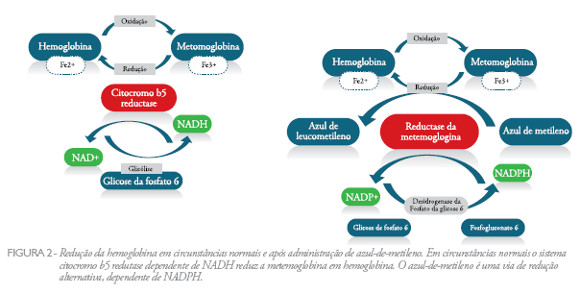
Uma vez formada, a acumulação de metemoglobinemia é prevenida pela acção de vários mecanismos que reduzem a metemoglobina a hemoglobina, numa cadeia de transferência de electrões (ilustrado na Figura 2
). O mecanismo fisiológico mais importante (responsável por 95% da redução da metemoglobina) é levado a cabo pela citocromo b5 reductase, previamente conhecida como diaforase, numa reacção dependente de NADH (dinucleotídeo de nicotinamida adenina). A citocromo b5 reductase encontra-se ligada de forma não covalente a um dinucleotídeo de flavina e adenina (FAD) que actua como aceitador de electrões. Assim, o NADH gerado pela glicólise reduz o FAD que por sua vez reduz a citocromo b5 reductase. A citocromo b5 reductase transfere os electrões para a metemoglobina, que ao reduzir o ferro ao estado ferroso se transforma em hemoglobina4. Uma via alternativa para a redução da metemoglobina é mediada pela reductase da metemoglobina. Nesta reacção é utilizado o NADpH (gerado pela desidrogenase da fosfato da glicose 6 na via das pentoses) como fonte de electrões. No entanto não existem aceitadores fisiológicos para estes electrões, sendo que esta depende de aceitadores exógenos, como é exemplo o azul-demetileno5,6,7.Denotar que nos indivíduos com défice da desidrogenase da glicose 6 fosfato o azul-de-metileno pode ser ineficaz (ou mesmo deletério como se discutirá adiante). A metemoglobina pode ainda ser reduzida por mecanismos não enzimáticos (por acção directa de compostos como o ácido ascórbico ou glutationa) mas são reacções lentas e pouco significativas.
Significado fisiológico
Em condições normais os mecanismos de formação e de redução descritos mantêm a fracção de metemoglobina estável, correspondendo a cerca de 1% da hemoglobina total.
A metemoglobinemia (concentração de metemoglobina superior a 1%) surge quando ocorre um desequilíbrio na produção ou na redução da metemoglobina, induzindo um estado de anemia funcional. Não só o heme férrico é incapaz de se ligar ao oxigénio como também induz alterações conformacionais que aumentam a afinidade dos outros heme ferrosos do tetrâmero pelo oxigénio, desviando a curva de dissociação para a esquerda. Assim, com fracções aumentadas de metemoglobina assistimos a um efeito combinado de menos oxigénio sendo transportado e menos oxigénio sendo libertado aos tecidos6.
Causas de metemoglobinemia
Na maioria das vezes a metemoglobinemia é adquirida, pela acção de vários agentes oxidantes. Embora raras, as formas hereditárias merecem pelo seu interesse histórico e características singulares, uma breve referência. são três as formas de metemoglobinemia hereditária. Duas obedecem a um padrão de transmissão autossómico recessivo: a deficiência do citocromo b5 reductase (cb5R) e a deficiência do citocromo b5 (note-se que o citocromo b5 reductase é um duplo sistema enzimático composto pelo citocromo b5 reductase e pelo citocromo b5). O terceiro tipo, designado de Doença da Hemoglobina m é transmitido de forma autossómica dominante e é caracterizado por uma mutação na cadeia globina.
1) Deficiência do citocromo b5 reductase (cb5R) - são descritas duas formas de deficiência do citocromo b5 reductase (cb5R): tipo I e tipo II. No tipo I há um défice funcional da Cb5R. Ocorrem mutações que conduzem a produção de uma enzima instável, facilmente degradada. Apesar de todas as células possuírem a cb5R anormal só os eritrócitos maduros, anucleados, são incapazes de a sintetizar e substituir. Esta forma de metemoglobinemia tem uma distribuição global mas é endémica na população dos índios Navajo e nos nativos Yakutsk da sibéria8,9. Os indivíduos homozigóticos ou heterozigotos compostos têm concentrações de metemoglobinemianaordemdos10-35%eapesarde cianóticos são assintomáticos. De facto a sua esperança de vida não é diferente da população geral e a cianose tem apenas significado cosmético3,6. Pelo contrário, os heterozigóticos correm o risco de desenvolver um quadro de metemoglobinemia aguda sintomática, após exposição a agentes oxidantes. A descrição clássica de metemoglobinemia aguda associada a profilaxia da malária em militares Norte-Americanos a prestar serviço no Vietname demonstrou pela primeira vez que os heterozigóticos para uma doença autossómica recessiva podem, em determinadas circunstâncias, desenvolver doença clinicamente mais exuberante que os seus pares homozigóticos10. Na deficiência do citocromo b5 reductase (cb5R) do tipo II ocorrem mutações que resultam numa diminuição da actividade catalítica da enzima ou num défice de produção. Para além da metemoglobinemia os doentes apresentam atraso de desenvolvimento psicomotor. A esperança de vida é significativamente diminuída e é comum a morte na infância. Os sintomas neurológicos parecem dever-se a alteração do metabolismo lipídico no sistema nervoso central, onde a cb5R parece desempenhar um papel importante11,12. Estas formas de deficiência de cb5R distinguem-se pelos eufenótipo clínico e são confirmadas pela análise da actividade enzimática em diferentes células. O azul-de-metileno ou o ácido ascórbico melhoram a cianose mas não têm qualquer efeito sobre as manifestações neurológicas.
2) A deficiência do citocromo b5 é uma causa extremamente rara de metemoglobinemia congénita, descrita apenas em um doente Israelita13 .
3) A Doença da Hemoglobina m engloba um grupo variado de mutações nas cadeias de globina. Na prática todas elas provocam uma alteração na conformação espacial do local de ligação ao grupo heme, conduzindo à oxidação espontânea do ferro. As diferentes variantes podem distinguir-se por eletroforese, espectrometria de massa, espectro de absorção ultravioleta e sequenciação molecular. Actualmente não existe tratamento eficaz para estes distúrbios1.
A exposição a agentes oxidantes pode aumentar subitamente os níveis de metemoglobina acelerando a taxa de formação até 1000 vezes, sobrecarregando os sistemas enzimáticos de protecção. Os doentes com deficiência da desidrogenase de fosfato glicose 6 têm risco aumentado de desenvolver metemoglobinemia uma vez que a glutationa actua como anti-oxidante fisiológico14,15. As crianças são um grupo particularmente susceptível uma vez que a actividade eritrocitária da cb5R é de apenas 50 a 60% do adulto. Nas áreas rurais a preparação de leite de fórmula com água do poço contaminada com nitratos corresponde a uma das formas mais frequentes de metemoglobinemia adquirida na infância16. De entre os agentes oxidantes mais frequentemente implicados como causa de metemoglobinemia (Tabela 1), contam-se alguns fármacos de uso ubiquitário no contexto hospitalar e ambulatório, como os nitratos, a dapsona, a benzocaína (utilizada como spray anestésico em técnicas como broncoscopia, ecocardiograma transesofágico) e os corantes de anilina14. A dapsona é um antibiótico que inibe a síntese do ácido fólico. Uma vez ingerida é rapidamente absorvida e atinge níveis plasmáticos máximos em cerca de 2-6h. É metabolizada no fígado por reacções de acetilação e hidroxilação, formando-se hidroxilaminas, responsáveis pela produção da metemoglobina. A semi-vida destas moléculas excede as 30h15,17,18. Vários casos de metemoglobinemia secundária a dapsona estão descritos na literatura, e embora alguns deles sejam resultado de ingestão excessiva acidental, a ocorrência de metemoglobinemia associada a dapsona em doses terapêuticas parece ser mais frequente. Num estudo retrospectivo de 138 casos de metemoglobinemia secundária, a dapsona foi o agente responsável em cerca de 42% dos casos, e em quase todos estava prescrita para profilaxia de pneumocistose em doentes imunocomprometidos14.
Diagnóstico
Como já referimos, quando a concentração de metemoglobinemia aumenta sobrevém um estado de anemia funcional e os doentes podem apresentar sintomas atribuídos a uma entrega inadequada de oxigénio aos tecidos.
Doentes jovens e sem anemia são geralmente assintomáticos com níveis de metemoglobinemia inferiores a15%.Níveis de 20-30% causam frequentemente sintomas como alteração do estado de consciência, cefaleias, fadiga, tonturas e síncope. Níveis superiores a 50% podem resultar em arritmias, convulsões, coma e mesmo morte19,20. Obviamente doentes com comorbilidades como anemia, doença cardiovascular, patologia pulmonar ou com presença de espécies anormais de hemoglobina podem apresentar sintomas com níveis de metemoglobina inferiores aos acima descritos. A suspeita de metemoglobinemia deve ser colocada na presença de cianose com pressão parcial de oxigénio (paO2) normal na gasometria.
A cianose é aparente quando o nível de metemoglobinemia excede 1,5g/dl3. por outro lado, a causa mais comum de cianose que se deve à presença de hemoglobina na forma desoxigenada (desoxihemoglobina) observa-se quando os níveis absolutos de desoxihemoglobina excedem 4 g/dl. Uma forma simples de distinguir a metemoglobina da desoxihemoglobina consiste em colocar uma ou duas gotas de sangue do doente num papel de filtro: o aspecto cor de chocolate da metemoglobina não se altera com o tempo, ao contrário da desoxihemoglobina que adquire um aspecto mais claro no contacto com o ar19,20. Uma outra pista que pode alertar para a presença de metemoglobinemia é o saturation gap, que corresponde à disparidade entre diferentes técnicas frequentemente usadas para medir a saturação arterial de oxigénio, nomeadamente a oximetria de pulso e a gasometria arterial21. A saturação de oxigénio pode ser medida de três formas diferentes: oximetria de pulso, gasometria arterial e co-oximetria. Em indivíduos sem dishemoglobinas os valores são virtualmente sobreponíveis. No entanto, na presença de fracções anormalmente elevadas de determinados tipos de hemoglobinas os diferentes métodos têm limitações que importa conhecer.
As moléculas de hemoglobina possuem um espectro de absorção de luz característico que possibilita a determinação da concentração dos diferentes derivados de hemoglobina. Os métodos de análise por espectrofotometria baseiam-se no princípio que a absorção de luz é proporcional à concentração de soluto21 .
1) A oximetria de pulso é um método espectrofotométrico não invasivo que utiliza apenas luz com dois comprimentos de onda e mede a contribuição de apenas duas espécies de hemoglobina: oxihemoglobina e desoxihemoglobina. Os oxímetros de pulso são concebidos de forma a conterem fonte de luz numa das extremidades e um fotodetector na outra. São capazes de emitir luz vermelha, com um comprimento de onda de 660nm e infra-vermelha a um comprimento de onda de 940nm. A desoxihemoglobina absorve mais energia a 660nm enquanto a oxihemoglobina absorve mais energia a 940nm. A razão entre a absorção dos diferentes comprimentos de onda durante a fase pulsátil e estática é convertida em saturação de oxigénio a partir de uma curva de calibração programada no aparelho. Na ausência de outras formas de hemoglobina (que não a oxi ou a desoxihemoglobina) uma razão de absorção de 1 corresponde a uma saturação de 85%. Os oxímetros de pulso são muito susceptíveis a interferências externas (pex arrepios que simulam pulsações) ou internas (diferentes formas de hemoglobina com espectros de absorção sobreponíveis). A metemoglobina tem dois picos de absorção, aproximadamente a 630nm e a 960nm. Desta forma a sua presença é interpretada pelo oxímetro como uma fracção quer de desoxihemoglobina quer de oxihemoglobina, fazendo aumentar o numerador e o denominador da razão de absorção 660/940nm, aproximando-o da unidade (um) e dessa forma obtendo um valor de saturação de oxigénio próximo de 85%. De facto, a partir de um determinado valor, concentrações crescentes de metemoglobina não fazem variar a saturação de oxigénio obtida por oximetria, que atinge um plateau mínimo de 84-86%21,22.
2) Os aparelhos de gasometria estimam a saturação de oxigénio a partir de equações empíricas que usam os valores de pH e de paO2. Eléctrodos de alta impedância medem alterações na voltagem e determinam pH e paCO2, enquanto a paO2 é determinada a partir de alterações de corrente num eléctrodo de Clark. mais uma vez a presença de formas diferentes de hemoglobina interferem no cálculo da saturação de oxigénio21 .
3) A co-oximetria é um método mais complexo e também mais fiável de determinação de saturação de oxigénio uma vez que mede absorção de luz a quatro ou mais comprimentos de onda, correspondentes aos diferentes padrões de absorção dos derivados de hemoglobina. Assim é determinada a percentagem das diferentes formas de hemoglobina: oxihemoglobina (cO2Hb), desoxihemoglobina (cHHb), metemoglobina (metHb), carboxihemoglobina (COHb) e sulfahemoglobina (sHb). Na presença de dishemoglobinas a co-oximetria é a forma mais fiável de avaliar a oxigenação sanguínea, calculando a fracção de oxihemoglobina (FO2Hb) em relação ao total de hemoglobina presente, que inclui todas as hemoglobinas non-oxygen binding22 . FO2Hb=cO2Hb+cHHb+cmetHb+cCOHb+csHb
Ainda assim existem algumas potenciais fontes de erro que devemos conhecer. Alguns co-oxímetros não são capazes de medir a sulfahemoglobina directamente, de modo que a sua presença pode traduzir-se numa falsa elevação do valor de metemoglobina e redução do valor de carboxihemoglobina, que pode até vir indicado como negativo! Neste contexto todos os esforços em reduzir os níveis de metemoglobina revelar-se-ão infrutíferos. A presença de azul-de-metileno pode também ser causa de falsa metemoglobinemia, o que coloca um desafio adicional na monitorização dos níveis de metemoglobinemia após tratamento com azul-de-metileno. Neste contexto a metemoglobina detectada por co-oximetria deve ser confirmada pelo método de Evelyn –malloy. Neste procedimento a adição de cianeto elimina o pico de absorção da metemoglobina, ao ligar-se a ela. A adição subsequente de ferricianeto converte toda a amostra em cianometemoglobina, permitindo a determinação da concentração total de hemoglobina. A metemoglobina é depois expressa em percentagem da concentração total de hemoglobina23,24. Uma outra interferência pode dever-se à presença de Hemoglobina m. Nesta forma de metemoglobinemia a co-oximetria pode revelar valores normais de metemoglobinemia e valores de carboxihemoglobina ou sulfahemoglobina aumentados! Isto porque nesta forma de metemoglobinemia a hemoglobina encontrase estruturalmente modificada e com um espectro de absorção que difere significativamente da metemoglobina típica.
Tratamento
O tratamento da metemoglobinemia depende do contexto clínico. Nas formas hereditárias to-dos os doentes devem ser aconselhados a evitar a exposição a agentes capazes de induzir a formação de metemoglobina. Como já referido não existe tratamento eficaz para a Hemoglobina m e o tratamento da cianose nos indivíduos com deficiência da cb5R prende-se apenas com razões cosméticas. Relativamente às formas adquiridas e nos casos ligeiros, os doentes são tratados apenas com a suspensão do agente oxidante e com oxigénio suplementar para maximizar a capacidade transportadora de oxigénio da hemoglobina normal. Assumindo que a produção de metemoglobinemia é interrompida, a redução pela via da citocromo b5 reductase é capaz de fazer diminuir o nível de metemoglobinemia em cerca de 15% por hora25 . Perante a presença de sintomas moderados/graves deve considerar-se a utilização adicional de azul-demetileno. Este antídoto é geralmente utilizado nas formas sintomáticas e com metemoglobina superior a 20%. No caso de indivíduos com condições pré-existentes que comprometam adicionalmente a correcta oxigenação dos tecidos, o limiar para utilização de azul-de-metileno é mais baixo, sendo frequentemente administrado se metemoglobinemia for superior a 10%26. A dose recomendada é de 1mg/kg, em administração por via endovenosa e em perfusão de cinco a dez minutos. A via intra-óssea também pode ser utilizada. Pode ser necessário repetir administração ao fim de uma hora se os níveis de metemoglobina forem superiores a 60% ou na ausência de melhoria. A dose total não deve exceder os 7mg/kg devido ao aumento da incidência de efeitos adversos como náusea, vómitos, diarreia ou hipersudorese. Deve ser utilizado de forma cautelosa em doentes com insuficiência renal grave ou em doentes com défice da desidrogenase de fosfato glicose -6. Nestes doentes o azul-de-metileno é ineficaz, uma vez que não existe NADpH necessário para reduzir o azul-de-metileno à sua forma activa. Aliás, neste contexto ou mesmo em indivíduos sem défice enzimático mas em que doses superiores a 15mg/kg são administradas, o azul-de-metileno pode funcionar como um agente oxidante, capaz de precipitar uma anemia hemolítica ou induzir, paradoxalmente, a formação de metemoglobina! Nestes doentes o tratamento mais eficaz passa pelo suporte transfusional. O ácido ascórbico (100 a 300mg/dia) pode também ser considerado no tratamento da metemoglobinemia, embora a resposta seja lenta e pouco ampla. De notar que tal como acontece com o azul-de-metileno, nos doentes com défice desidrogenase de fosfato glicose-6 pode funcionar como oxidante. Em casos extremamente graves a exsanguinotransfusão e a administração de oxigénio hiperbárico podem ser opções terapêuticas, embora sem clara demonstração da sua eficácia. No contexto particular de metemoglobinemia secundária à dapsona, a cimetidina pode contribuir para a redução da metemoglobina, inibindo a hidroxilação da dapsona e a sua transformação no metabolito oxidante. No entanto, apesar de prevenir o agravamento da metemoglobinemia nos doentes submetidos a terapêutica crónica com dapsona, o seu modo lento de actuação torna o uso da cimetidina ineficaz no contexto de metemoglobinemia aguda sintomática27,28.
Discussão
A metemoglobinemia adquirida é descrita como uma patologia comum14. No entanto desconhece-se a sua prevalência, nomeadamente em clínicas de ambulatório de doentes com Infecção VIH, local onde face à prescrição frequente de fármacos considerados agentes comuns de metemoglobinemia se esperaria uma prevalência elevada. Este foi o primeiro caso de metemoglobinemia descrito no serviço de Doenças Infecciosas do Hospital são João, onde cerca de 1800 doentes com infecção VIH se encontram em consultas de seguimento. O facto de muitos dos casos de metemoglobinemia poderem corresponder a formas ligeiras e cursarem clinicamente de forma silenciosa pode parcialmente justificar este facto.
O diagnóstico é dependente de um nível elevado de suspeição, sobretudo em doentes onde a cianose não é evidente. No nosso caso a presença do saturation gap foi a pista mais relevante. De facto a discrepância entre a saturação de oxigénio obtida por oximetria (89%) e por gasometria arterial (97%) foi o dado que alertou para a presença de metemoglobina, confirmada por cooximetria. Face à percentagem de metemoglobina (11%), à sintomatologia dominada pela dispneia e à presença concomitante de anemia (Hb 9,5g/dl) optou-se por aumentar a capacidade de transporte de oxigénio recorrendo a oxigénio suplementar e ao suporte transfusional. A contribuição da pneumocistose para o quadro de dispneia, provavelmente até o principal determinante foi também um factor tido em conta na opção de não utilizar azul-de-metileno.
Conclusão
A metemoglobinemia é uma causa de anemia funcional cuja prevalência exacta se desconhece mas se admite ser elevada e que se atribui na maioria dos casos à utilização de fármacos de prescrição frequente, quer em ambiente hospitalar quer em regime de ambulatório. O diagnóstico é simples mas dependente de um elevado índice de suspeição. É fundamental o reconhecimento precoce de uma patologia associada a importante morbilidade e potencialmente fatal, para a qual existe tratamento eficaz.
Referências
1. Percy MJ, McFerran NV, Lappin TR. Disorders of oxidised haemoglobin. Blood Rev 2005;19(2):61-8. [ Links ]
2. Misra HP, Fridovich I. The generation of superoxide radical during the autoxidation of hemoglobin. J Biol Chem 1972;247(21):6960-2. [ Links ]
3. Gregg XT, Prchal JT. Red Blood Cell Enzymopathies. In: Hoffman R, Benz E. Hematology: Basic Principles and Practice, 4Th ed. Philadelphia. Churchill Livingstone 2005; pp. 611-23. [ Links ]
4. Passon PG , Hultquist DE. Soluble cytochrome b 5 reductase from human erythrocytes. Biochim Biophys Acta 1972;275(1):62-73. [ Links ]
5. Rosen PJ, Johnson C, McGehee WG, Beutler E. Failure of methylene blue treatment in toxic methemoglobinemia. Association with glucose-6-phosphate dehydrogenase deficiency. Ann Intern Med 1971;75(1):83-6. [ Links ]
6. Mansouri A, Lurie AA. Concise review: methemoglobinemia. Am J Hematol 1993;42(1):7-12. [ Links ] 6. Gibson Q. Introduction: congenital methemoglobinemia revisited. Blood 2002;100(10):3445-6. [ Links ]
7. Janssen WJ, Dhaliwal G, Collard HR, Saint S. Clinical problem-solving. Why why matters. N Engl J Med 2004;351(23):2429-34. [ Links ]
8. Scott EM, Hoskins DD. Hereditary methemoglobinemia in Alaskan Eskimos and Indians. Blood 1958;13(8):795-802. [ Links ]
9. Balsamo P, Hardy WR, Scott EM. Hereditary methemoglobinemia due to diaphorase deficiency in Navajo Indians. J Pediatr 1964;65:928-31. [ Links ]
10. Cohen RJ, Sachs JR, Wicker DJ, Conrad ME. Methemoglobinemia provoked by malarial chemoprophylaxis in Vietnam. N Engl J Med 1968;279(21):1127-31. [ Links ]
11. Takeshita M, Tamura M, Kugi M, Matsuki T, Yoneyama Y, Igarashi T. Decrease of palmitoyl-CoA elongation in platelets and leukocytes in the patient of hereditary methemoglobinemia associated with mental retardation. Biochem Biophys Res Commun 1987;148(1):384-91. [ Links ]
12. Leroux A, Junien C, Kaplan J, Bamberger J. Generalised deficiency of cytochrome b5 reductase in congenital methaemoglobinaemia with mental retardation. Nature 1975;258(5536):619-20. [ Links ]
13. Hegesh E, Hegesh J, Kaftory A. Congenital methemoglobinemia with a deficiency of cytochrome b5. N Engl J Med 1986;314(12):757-61. [ Links ]
14. Ash-Bernal R, Wise R, Wright SM . Acquired methemoglobinemia: a retrospective series of 138 cases at 2 teaching hospitals. Medicine 2004;83(5):265-73. [ Links ]
15. Sin DD, Shafran SD. Dapsone- and primaquine-induced methemoglobinemia in HIV-infected individuals. J Acquir Immune Defic Syndr Hum Retrovirol 1996;12(5):477-81. [ Links ]
16. Comly HH. Cyanosis in infants caused by nitrates in well-water. JAMA 1945;129:112-6. [ Links ]
17. Zosel A, Rychter K, Leikin JB. Dapsone-induced methemoglobinemia: case report and literature review. Am J Ther 2007;14(6):585-7. [ Links ]
18. Ward KE, McCarthy MW. Dapsone-induced methemoglobinemia. Ann Pharmacother 1998;32(5):549-53. [ Links ]
19. Jaffé ER. Methemoglobin pathophysiology. Prog Clin Biol Res 1981;51:133-51. [ Links ]
20. Wright RO, Lewander WJ, Woolf AD. Methemoglobinemia: etiology, pharmacology, and clinical management. Ann Emerg Med 1999;34(5):646-56. [ Links ]
21. Haymond S, Cariappa R, Eby CS, Scott MG . Laboratory assessment of oxygenation in methemoglobinemia. Clin Chem 2005;51(2):434-44. [ Links ]
22. Rausch-Madison S, Mohsenifar Z. Methodologic problems encountered with cooximetry in methemoglobinemia. Am J Med Sci 1997;314(3):203-6. [ Links ]
23. Fairbanks VF, Klee GG . Biochemical aspects of hematology. In: Burtis CA, Ashwood ER, eds. Tietz textbook of clinical chemistry, 3rd ed. Philadelphia. WB Saunders 1999; pp. 1642-710. [ Links ]
24. Evelyn KA, Malloy HT. Microdetermination of oxyhemoglobin, methemoglobin and sulfhemoglobin in a single sample of blood. J Biol Chem 1938;126:655-57. [ Links ]
25. Finch CA. Treatment of intracellular methemoglobinemia. Bull New Engl Med Cent 1947;9(6):241-5. [ Links ]
26. Clifton J 2nd, Leikin JB. Methylene blue. Am J Ther 2003;10(4):289-91. [ Links ]
27. Coleman MD, Rhodes LE, Scott AK, Verbov JL, Friedmann PS , Breckenridge AM, Park BK. The use of cimetidine to reduce dapsone-dependent methaemoglobinaemia in dermatitis herpetiformis patients. Br J Clin Pharmacol 1992;34(3):244-9. [ Links ]
28. Turner MD, Karlis V, Glickman RS. The recognition, physiology, and treatment of medication-induced methemoglobinemia: a case report. Anesth Prog 2007;54(3):115-7. [ Links ]
Ana Cláudia Carvalho
Serviço de Doenças Infecciosas -Hospital São João, Porto Alameda Professor Hernâni Monteiro 4200-319 Porto, Portugal. Email: claudiac@med.up.pt; anaclaudiacarvalho@gmail.com














