Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Arquivos de Medicina
versão On-line ISSN 2183-2447
Arq Med v.23 n.2 Porto mar. 2009
Regulação da Absorção Intestinal de Glicose
Uma Breve Revisão
João R. Araújo, Fátima Martel
Departamento de Bioquímica (U38-FCT), Faculdade de Medicina da Universidade do Porto
A absorção intestinal de glicose engloba duas componentes. Uma consiste na absorção mediada por um transportador activo de glicose dependente do sódio (SGLT1); a outra é constituída por um transporte facilitado de glicose independente do sódio (GLUT2). O SGLT1 presente na membrana apical do enterócito comporta-se como um sensor de glicose, regulando a inserção membranar do GLUT2 apical. Em conjunto, o GLUT2 e o SGLT1 são responsáveis pela absorção intestinal de glicose. A absorção intestinal de glicose proveniente da dieta desempenha um papel importante na regulação dos níveis de glicose no plasma. Por sua vez, os níveis de glicose plasmática controlam a ingestão alimentar e regulam a secreção de insulina pelo pâncreas. A hiperinsulinémia e consequente insulino-resistência periférica (associadas a intolerância à glicose) estão relacionadas com o desenvolvimento de síndrome metabólica, uma patologia multifactorial que pode conduzir ao desenvolvimento de aterosclerose, patologias cardiovasculares, diabetes e elevada taxa de mortalidade. Como tal, o objectivo deste artigo é fazer uma breve descrição dos mecanismos subjacentes à absorção intestinal de glicose e sua modulação, e destacar a sua importância na prevenção e terapêutica de patologias como a diabetes, obesidade e síndrome metabólica.
Palavras-chave: intestino; glicose; absorção; SGLT1; GLUT2; diabetes.
Regulation of Intestinal Sugar Transport
Intestinal glucose absorption involves two components. One is mediated by an active sodium-dependent glucose transporter (SGLT1) and the other one is mediated by a facilitated sodium-independent glucose transporter (GLUT2).
SGLT1 is present in the apical membrane of the enterocyte where it acts as a glucose sensor, regulating membrane insertion of apical GLUT2. Together, these two transporters are responsible for intestinal glucose absorption. Intestinal absorption of glucose derived from the diet plays an important role in blood glucose homeostasis. Blood glucose levels, in turn, play a role in the control of food intake and in the regulation of insulin secretion by the pancreas. Hyperinsulinemia and its consequent peripheral insulin resistance (with its associated glucose intolerance) are closely linked to the development of metabolic syndrome, a multifactorial condition leading to accelerated atherosclerosis and increased risk for diabetes, major cardiovascular events and a high mortality rate. So, the main aim of this article is to briefly describe the mechanisms involved in intestinal glucose absorption and its modulation, emphasizing its importance in the prevention and therapeutics of diseases such as diabetes, obesity and metabolic syndrome.
Key-words: intestine; glucose; absorption; SGLT1; GLUT2; diabetes.
INTRODUÇÃO
O conhecimento dos mecanismos homeostáticos que controlam os níveis de glicose plasmática é fundamental no controlo e tratamento de patologias como a obesidade, a diabetes e a síndrome metabólica. A absorção intestinal de glicose proveniente da dieta desempenha um papel fundamental na regulação dos níveis de glicose plasmática (1). O conhecimento relativo à modulação do transporte intestinal de glicose, com vista a compreender e discutir os mecanismos envolvidos na alteração da sua absorção intestinal, reveste-se pois de grande importância (2). Por isso, o objectivo principal desta revisão consiste em elencar os principais mecanismos envolvidos na absorção intestinal de glicose, realçando a sua preponderância na prevenção e terapêutica de doenças cuja fisiopatologia envolve uma alteração do transporte intestinal de glicose.
GLICOSE: IMPORTÂNCIA E TRANSPORTE MEMBRANAR
O epitélio intestinal, desde o duodeno ao cólon, é constituído por enterócitos ligados entre si por junções apertadas. Este epitélio é responsável por inúmeras funções, entre as quais o transporte e metabolismo de nutrientes: monossacarídeos, aminoácidos, ácidos gordos, minerais como o sódio, o potássio, o bicarbonato e o cloreto, protões e água (3).
A glicose é o principal substrato metabólico para a actividade normal do ser humano ao longo do seu ciclo de vida. A sua principal fonte no organismo corresponde aos glícidos provenientes da dieta (uma dieta ocidental normal pode fornecer cerca de 180 g de glicose por dia) (4). Os glícidos da dieta, essencialmente polissacarídeos, são digeridos enzimaticamente a unidades mais simples, os monossacarídeos (maioritariamente glicose, galactose e frutose), antes da sua absorção no intestino delgado ao nível dos enterócitos das vilosidades intestinais (5, 6). O transporte intestinal de monossacarídeos é influenciado pela sua qualidade e quantidade presente no lúmen intestinal, sendo os mais bem documentados os que dizem respeito à glicose, frutose, galactose, manose, xilose e 3-O-metilglicose (7-9). O corpo humano tem uma necessidade obrigatória de glicose de aproximadamente 200 g por dia, sobretudo para satisfazer as necessidades metabólicas do cérebro (10). Se a concentração de glicose no sangue se situar abaixo de 40 mg/dL (2.2 mol/L) pode ocorrer coma, convulsões ou até mesmo morte (11). Por outro lado, níveis que excedam os 180 mg/dL (10 mmol/L) (correspondendo a hiperglicemia) podem estar associados a complicações a curto e a longo glicose, ou de outros monossacarídeos, para realizar a prazo (10). Como tal, a regulação da concentração de sua função de transporte (12, 14).As 5 primeirasisoformas glicose plasmática está fortemente dependente de vários (GLUT1-GLUT5) parecem ser as principais, tendo sido mecanismos homeostáticos (11).
Nos mamíferos, o transporte transmembranar de glicose e outros açúcares é levado a cabo por duas famílias de proteínas transportadoras: uma, formada por transportadores activos, que requerem o consumo deATP e dependentes do ião sódio (SGLT), e outra, formada por transportadores de glicose por difusão facilitada (GLUT), que não requerem energia transportando a glicose a favor do seu gradiente de concentração (12, 13).Ambos exibem diferentes especificidades para os substratos e diferentes propriedades cinéticas e padrões de expressão tecidular, o que garante que a captação celular de glicose está assegurada perante uma grande variedade de condições metabólicas (13). Pelo menos 3, e até 6, transportadores de glicose dependentes do sódio (SGLT1-SGLT6, genes da família SLC5A) já foram identificados no intestino, rim, músculo, neurónios e tiróide. Através destes transportadores, o gradiente electroquímico do ião sódio gerado pela bomba de sódio e potássio (ATPase-Na+/K+) é utilizado para transportar a glicose contra o seu gradiente de concentração (transporte activo secundário) (5, 12). Destes transportadores transmembranares, o SGLT1 é proeminentemente expresso no epitélio do intestino delgado (duodeno, jejuno e íleo) (5). Quanto ao outro mecanismo de transporte, engloba uma família de catorze membros de transportadores facilitados de glicose (GLUT1-GLUT14, genes da família SLC2)independentes do sódio, que utilizam o gradiente de concentração da as mais estudadas no que respeita à sua caracterização em situações fisiológicas e fisiopatológicas (15).
ABSORÇÃO INTESTINAL DE GLICOSE: MODELO CLÁSSICO E MODELO DO GLUT2 APICAL
De acordo com o modelo clássico de absorção intestinal de glicose, esta é captada activamente do lúmen intestinal para o interior do enterócito pelo SGLT1, localizado na membrana apical (5) (Figura 1). O SGLT1 possui um local de ligação ao sódio, e é essa ligação que induz uma alteração conformacional no transportador, tornando-o acessível à glicose (8, 9). Desse modo, por cada molécula de glicose transportada, dois iões sódio, cujo gradiente transmembranar é gerado pela ATPase-Na+/K+localizada na membrana basolateral, são transportados na mesma direcção (5). Depois, a glicose acumulada é libertada passivamente do enterócito para a circulação sanguínea através de duas vias distintas: a) uma, maioritária, que envolve o GLUT2 (Figura 1) e outra b) por transporte envolvendo vesículas intracelulares, que requer fosforilação da glicose a glicose-6-fosfato, transferência da glicose-6-fosfato para o retículo endoplasmático e posterior libertação da glicose livre (desfosforilada) para a corrente sanguínea. De realçar que uma pequena fracção intracelular da glicose pode ser usada como substrato metabólico no enterócito (5, 6).
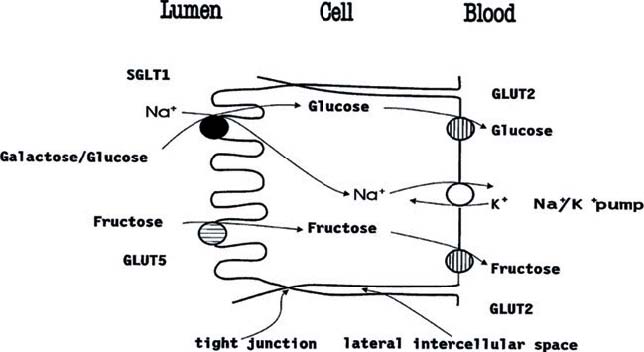
Fig. 1. Modelo clássico de absorção intestinal de glicose no enterócito. Na membrana apical a glicose é transportada activamente para o espaço intracelular principalmente pelo transportador activo de glicose dependente do sódio (SGLT1). Na membrana basolateral a glicose é transportada, a favor do gradiente de concentração, do enterócito
Simultaneamente, durante o transporte intestinal de glicose via SGLT1, outras moléculas são também transportadas com vista a manter a osmolaridade do conteúdo absorvido: a) dois aniões, o cloreto e o bicarbonato, acompanham, por uma via distinta do SGLT1, o transporte de sódio com vista a manter a electroneutralidade, e b) água (funcionando o SGLT1 como um canal específico de transporte de água - aquaporina). O co-transporte de glicose, sódio e água (estequiometria de 1:2:249 moles respectivamente) pelo SGLT1 e o transporte associado de cloreto e bicarbonato estão na base do desenvolvimento da terapia de re-hidratação oral, um dos avanços médicos mais importantes do século XX (5, 16). O transporte realizado pelo SGLT1 é reversível, ou seja, a taxa e a direcção do co-transporte de sódio e glicose dependem do gradiente electroquímico do sódio e da glicose (5). O SGLT1 (clonado pela primeira vez por Hediger e colaboradores em 1987) (6) transporta glicose e galactose com afinidades semelhantes e elevadas (constante de afinidade ou Km =0.1-0.6 mM para a glicose) mas com capacidade de transporte (actividade para elevadas concentrações de substrato ou Vmax) baixa, sendo a sua actividade inibida pela floridzina (um inibidor competitivo com uma constante de inibição ou Ki=0.1 mM) (5, 17).
Relativamente ao GLUT2, trata-se de um transportador de glicose por difusão facilitada, independente do sódio, com baixa afinidade (Km para a glicose >50 mM) e alta capacidade de transporte de glicose, e que para além da glicose transporta também a frutose, a galactose e a manose (1, 6). Este transportador é inibido pela citocalasina B e floretina, sendo este último, um inibidor específico (6).
Na sua essência, o modelo clássico de absorção intestinal de glicose é simples, explicando a sua absorção numa grande variedade de condições, principalmente perante baixas concentrações luminais de glicose (da ordem dos 5 mM), ou seja, quando a concentração de glicose no lúmen intestinal é inferior à plasmática e, portanto, característica do período anterior à refeição. Qualquer molécula de glicose é rapidamente captada pelo SGLT1, ideal para esta situação, pois trata-se de um transportador de alta afinidade e baixa capacidade e o único capaz de transportar a glicose contra o seu gradiente de concentração. Contudo, este modelo não explica a absorçãointestinalperante altas concentrações luminais de glicose (≥50 mM), que ocorrem apósingestão de uma refeição, quando o SGLT1 já está saturado (o que acontece por volta dos 30-50 mM). In vivo, o que se verifica é que a absorção intestinal de glicose aumenta linearmente, parecendo não ser saturável, com o aumento da concentração de glicose luminal (14). Por isso, o modelo clássico de absorção intestinal de glicose tem sido recentemente posto em causa por muitos investigadores (1,4-6,17,18).
Ao nível da membrana apical, várias evidências demonstraram a existência de um segundo mecanismo de transporte de glicose, para além daquele via SGLT1, que poderá corresponder a: a) transportador de por difusão facilitada com baixa afinidade e alta capacidade, não dependente do sódio e insensível à floridzina (1,4-6); b) um transportador activo, com alta afinidade e baixa capacidade e sensível à floridzina, ou seja, um segundo SGLT (SGLT2, SGLT3, SGLT4, SGLT5 ou SGLT6, ou até um novo SGLT1, nSGLT1). Este mecanismo encontra-se ainda vagamente descrito, e parece, de momento, não explicar o que se passa in vivo. Por último, esse segundo mecanismo pode ainda corresponder a: c) um transporte envolvendo vesículas intracelulares e endocitose, mas que actualmente ainda está vagamente caracterizado (1).
A primeira hipótese (a) tem sido a mais descrita e a que reúne mais consenso, e sugere a presença do transportador GLUT2 (clonado pela primeira vez por Thorens e colaboradores em 1990 (19)) ao nívelapical, designandose de modelo do GLUT2 apical (4, 6, 18) (Figura 2). Esta hipótese foi recentemente reforçada com a identificação do GLUT2 ao nível da membrana apical intestinal, por imunocitoquímica (20) e por biotinilização da membrana, por imunofluorescência e por imunogold (21). Para além disso, o facto da desoxiglicose, um análogo da D-glico-se transportado eficientemente pelos GLUT (GLUT1 e GLUT2) mas com pouca afinidade para o SGLT1 (6), ser transportada na membrana apicalde células Caco-2 (linha celular que mimetiza o epitélio intestinal humano) (22) e na membrana apical de enterócitos embrionários de galinha (23) também está de acordo com esta hipótese. Adicionalmente, foi referido que a captação apical, em células Caco-2, de alfa-metil-D-glicose (24), um análogo não metabolizável da D-glicose substrato do SGLT1 e GLUT2 (6), envolve dois mecanismos: 1) um sistema dependente do sódio, mais sensível à floridzina do que à floretina (Km =2 mM), eventualmente o SGLT1; e 2) um sistema dependente do sódio, mais sensívelà floretina do que à floridzina (Km =8 mM), que provavelmente reflecte a actividade conjunta do SGLT1 e do GLUT2 (24).
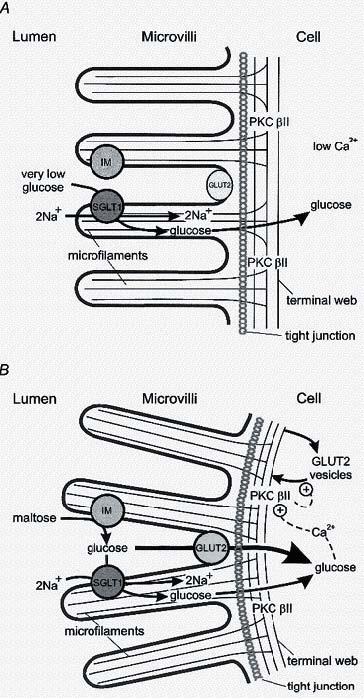
Fig. 2 - Modelo do GLUT2 apical. (A) Antes da refeição, a concentração de glicose no lúmen intestinal é baixa, sendo inferior à concentração plasmática. A actividade intrínseca e a expressão do transportador facilitado de glicose GLUT2 são baixas, e ocorre absorção de glicose contra o seu gradiente de concentração através do transportador activo de glicose dependente do sódio SGLT1. (B) Depois da refeição, concentrações elevadas de glicose estão em contacto com as microvilosidades, decorrente da actividade hidrolítica das dissacaridases (nomeadamente pela acção da isomaltase (IM) sobre a maltose). O transporte de glicose via SGLT1 resulta na activação da cínase de proteínas C isoforma βII (PKC βII) e, consequentemente, na activação e recrutamento do GLUT2 para a membrana apical do enterócito. O transporte de glicose via SGLT1 resulta na contracção do anel peri-juncional de actimiosina (abaixo da junção apertada), causando uma rotação subtil da superfície absortiva da célula. Ambos os processos poderão ser mediados pelo aumento da concentração do Ca2+ intracelular (Retirado de (25)).
Após a refeição, os produtos decorrentes da digestão de glícidos, sobretudo dissacarídeos, atingem a membrana apical do jejuno, 30 min após sua ingestão. Nessa altura, atingem-se concentrações fisiológicas à superfície da membrana apical entre os 50-300 mM de glicose. De acordo com a hipótese do GLUT2 apical, alguns minutos após a glicose ser transportada pelo SGLT1, ocorre um rápido (t1/25 min) recrutamento e inserção de transportadores GLUT2, provenientes de vesículas intracelulares localizadas nas imediações da membrana, na membrana apical, e um aumento da actividade intrínseca (quantidade de substrato transportado por unidade de proteínas transportadoras) dos GLUT2 já existentes na membrana (1, 7) (Figura 2). Isto acontece devido à activação de vias de transdução de sinal que envolvem proteínas reguladoras intracelulares dependentes do SGLT1: cínase de proteínas C (PKC), mais especificamente a isoforma βII (PKCβII) e cínase de proteínas activadas por mitogénios (cínase MAP), entre outras (1). O cálcio é essencial para a activação deste mecanismo de sinalização intracelular pois, para além de activar a PKC, promove no enterócito um rearranjo no citoesqueleto que está associado à contracção perijuncional do anel de actimiosina, levando à fosforilação da miosina II (21) (Figura 2).
Este mecanismo de transporte cooperativo entre o SGLT1 e o GLUT2 opera somente quando estão presentes altas concentrações de glicose no lúmen intestinal, ou seja, durante a digestão de uma refeição rica em glícidos, promovendo desse modo uma absorção facilitada de glicose várias vezes (3 a 5 vezes) superior àquela proporcionada só pelo SGLT1 (5,6,14,17). Nesta situação, o GLUT2 constitui a principal via de absorção intestinal de glicose (75% do total) (21). Pelo contrário, antes de uma refeição, quando os níveis de glicose luminais são baixos, a presença de GLUT2 na membrana apical é reduzida (bem como a sua actividade intrínseca) e o GLUT2 basolateral opera na direcção oposta, fornecendo glicose da corrente sanguínea para o enterócito, o que contribui para o equilíbrio energético do mesmo. In vivo, mesmo perante baixas concentrações luminais de glicose, pode existir algum GLUT2 na membrana apical. Nessa condição, a sua presença apical poderia ter consequências graves tais como a secreção de glicose do enterócito para o lúmen intestinal. No entanto, esta situação é minimizada por vários factores: 1) a presença de GLUT2 apical é reduzida quando estão presentes baixas concentrações luminais de glicose, e desaparece completamente após o período nocturno de jejum; 2) a actividade intrínseca do GLUT2 residual é baixa; e 3) qualquer secreção intestinal de glicose é rapidamente transportada pelo SGLT1 (actuando como um scavenger) contra gradiente concentração novamente para o interior do enterócito, impedindo que altas concentrações de glicose atinjam o cólon.
Em suma, podemos verificar que o SGLT1, além da função de transportador de glicose, funciona igualmente como um sensor de glicose, controlando ainserção membranar do GLUT2 apósingestão de uma refeição. Depois, à medida que a glicose é absorvida e a sua concentração no lúmen intestinal diminui, todo o sistema de sinalização é revertido, permitindo que o GLUT2 seja maioritariamente inactivado e removido da membrana apical, regressandose à situação pré-prandial inicial (14).
REGULAÇÃO DA ABSORÇÃO INTESTINAL DE GLICOSE
Como referido anteriormente, a absorção intestinal de glicose é dependente de dois transportadores distintos, o SGLT1 e o GLUT2, que são também regulados de um modo distinto. Sabe-se por exemplo que no período pósprandial não existe uma relação linear entre os níveis proteicos de SGLT1 membranar e a concentração de glicose luminal, ao passo que a actividade do GLUT2 e os seus níveis na membrana apical aumentam proporcionalmente a essa concentração (14). Por isso, interessa referir a regulação de cada um destes transportadores separadamente.
Em relação ao GLUT2 apical, sabe-se que é regulado por uma grande variedade de estímulos fisiológicos, a curto e a longo prazo: 1) pela ingestão de glícidos, sendo activado por dietas ricas em glícidos simples e dietas com elevado índice glicémico, contrariamente ao que se passa com as dietas de baixo índice glicémico, que diminuem a absorção proporcionada por esse transportador (1,2, 26,27); 2) por hormonas endócrinas (sendo aumentado pela insulina) e parácrinas (sendo aumentado pela incretina peptídeo semelhante à glicagina tipo-2 (GLP-2) (28) e diminuído pela incretina polipetídeo insulinotrópico semelhante à insulina (GIP) (14,21,28); 3) pelo jejum, diminuindo nesta situação (2,18); 4) pela absorção intestinal de cálcio, sendo aumentado por esta; 5) por receptores intestinais sensíveis ao doce, activados por monossacarídeos e edulcorantes, sendo aumentado por estes compostos (21); 6) pelo stresse, diminuindo em resposta ao stresse ambiental (30) e aumentando em resposta ao stresse psicológico, traumatismo crânioencefálico (31,32), stresse metabólico (20) e stresse induzido pela ausência de ingestão de água (21); 7) pela depleção energética, aumentando nesta situação (20,33); 8) por compostos polifenólicos, sendo inibido por alguns destes componentes presentes na dieta (34-37); e 9) em patologias como a diabetes, aumentando nesta situação (18,21). Por isso, o GLUT2 deve ser encarado como um transportador com umaimportantíssima função fisiológica (18). Um dos motivos pelo qual o papel do GLUT2 só agora começou a ser revelado reside no facto de nas preparações in vitro o GLUT2, ou o transporte mediado pelo GLUT2, e as vias intracelulares que conduzem à sua activação (nomeadamente a via da PKC βII), serem difíceis de detectar. Isto acontece, sobretudo, porque o SGLT1 é o transportador dominante em experiências de captação in vitro, onde frequentemente se usam concentrações baixas de substrato (25).
Aregulação a curto e a longo prazo do SGLT1 também tem sido documentada. O SGLT1 parece ser modulado: 1) pela ingestão de glícidos, sendo activado por dietas ricas em glícidos simples e dietas com elevado índice glicémico, contrariamente ao que se passa com as dietas de baixo índice glicémico, que diminuem a absorção proporcionada por este transportador; 2) pelo jejum, sendo o SGLT1 activado nessa situação (2,18); 3) pelos sinais de saciedade leptina e colecistocinina-8 (CCK-8), que inactivam o SGLT1 (38,39); 4) pelo stresse, diminuindo em resposta ao stresse psicológico e traumatismo crânioencefálico (30,31); 5) por compostos polifenólicos, sendo inibido por alguns destes componentes presentes na dieta (34,40-42), e 6) pelo sódio, que activa este transportador (2,25,43-48).O transporte mediado pelo GLUT2 é essencialmente dependente do SGLT1 na medida em que: 1) a activação do SGLT1 activa a via da PKC βII; 2) a activação da PKC βII mostrou ser saturável sendo o seu valor de Ka para a glicose semelhante ao Km do SGLT1; 3) a inibição do SGLT1 inactiva a PKC βII, conduzindo à redução do GLUT2 apical e a uma inibição do transporte facilitado (14,25); e 4) pacientes com síndrome de Fanconi-Bickel (caracterizado pela inactivação dos 2 alelos do gene do GLUT2) não apresentam ingestão deficitária de glícidos (49). Em suma, o GLUT2 e o SGLT1 actuam em conjunto no processo de absorção intestinal de glicose, regulando os níveis de glicose no enterócito e possivelmente no plasma (14).
MECANISMOS DE REGULAÇÃO A CURTO E LONGO PRAZO DA ABSORÇÃO INTESTINAL DE GLICOSE
A regulação da absorção intestinal de glicose, em resposta a alterações na dieta, envolve vários mecanismos (8,9). Agudamente ou a curto prazo, existem mecanismos que podem alterar: 1) os níveis de transportadores na membrana, 1a) promovendo a inserção de transportadores provenientes de vesículasintracelulares, os endossomas (envolve transportadores que não se encontram en route para a membrana plasmática após biossíntese, pois são insensíveis aos inibidores do citoesqueleto), ou 1b) promovendo o desaparecimento dos já existentes na membrana (reciclagem ou turnover) (1). Esta modulação a curto prazo do transporte intestinal de glicose (via SGLT1 e GLUT2 apical) foi descrita para hormonas endócrinas e parácrinas (14,28,50), segundos mensageiros (51), activadores e/ou inibidores de cínases de proteínas (52,53), jejum, receptores intestinais sensíveis ao doce (18, 21) e principalmente para níveis extracelulares de glicose (1,2,22,25-27,54). Quando o transporte de glicose via SGLT1 ou GLUT2 é inibido, os transportadores, após certo tempo, são endocitados, mas quando o SGLT1 ou GLUT2 endossomais são activados, retornam à membrana apical (8, 9). Esta população intracelular de transportadores de glicose está presente em células de jejuno humano absortivas e nas células Caco-2, evidenciando a validade desta linha celular no estudo da regulação da absorção intestinal de glicose em enterócitos humanos (55).
Cronicamente ou a longo prazo, os níveis de transportadores de glicose membranares podem ser modulados por: 2) alteração da expressão do seu RNAm (transcrição) ou da sua taxa de síntese (8,9). Esta modulação a longo prazo foi descrita para o transporte apical via GLUT2 por monossacarídeos da dieta (1,2,25-27), por hormonas (14,28), pelo jejum (18,21), pelo stresse (31), e em algumas patologias (18,21).
Por fim, o outro factor envolvido, a curto e/ou longo prazo, na regulação do transporte intestinal de glicose relaciona-se com: 3) a actividade intrínseca dos transportadores. Esta pode estar alterada sem que haja modificação dos níveis de transportadores na membrana (8,9). Este mecanismo pode envolver a presença de proteínas reguladoras do SGLT1 intracelulares (como a sub-unidade reguladora do SGLT1 (RS1), a cínase A de proteínas (PKA), a PKC e a cínase MAP), que conduzem a processos de fosforilação ou desfosforilação, e consequentemente à activação ouinibição dos transportadores. A RS1 altera a actividade do SGLT1, reduzindo a sua Vmax. A deficiência de RS1 em ratinhos knockout (RS1-/-) está associada a um aumento da ingestão alimentar, do transporte de glicose, dos níveis de ARNn do SGLT1 e consequentemente ao desenvolvimento de obesidade (56). Estes investigadores sugerem que estratégias terapêuticas que reduzam o transporte de glicose através do aumento dos níveis de RS1 podem eventualmente ser usadas no tratamento da obesidade (1). Relativamente a outras proteínas reguladoras como a PKA e PKC, responsáveis pela fosforilação do SGLT1, os efeitos decorrentes da sua activação no transporte intestinal de glicose podem ser diferentes, e até mesmo antagónicos, dependendo da espécie considerada (o aumento dos níveis de PKC parece aumentar o transporte via SGLT1 no Homem, mas diminuir o transporte via SGLT1 no Rato e Coelho) (57).
ABSORÇÃO INTESTINAL DE GLICOSE E PATOLOGIA DIABÉTICA
A diabetes mellitus é um grupo de doenças caracterizadas por hiperglicemia crónica e outras alterações metabólicas, que ocorrem devido a deficiência da acção da insulina (58). Na maioria dos países desenvolvidos, a diabetes é uma das principais causas de morte e existe uma evidência substancial de que está a alcançar proporções epidémicas em muitos países em desenvolvimento e países recém-industrializados. Estima-se que 246 milhões de pessoas no mundo inteiro sejam diabéticas. Segundo estimativas da Organização Mundial de Saúde, prevê-se que em 2025 haja 300 milhões de doentes diabéticos em todo o Mundo (59). Embora não existam estudos epidemiológicos dirigidos, a prevalência da diabetes em Portugal, estimada pela International Diabetes Federation no seu Atlas de 2006, é de cerca de 9,8%, na população acima dos 20 anos de idade (59, 60). Esta epidemia de diabetes implicará inevitavelmente uma epidemia paralela de doença cardiovascular (DCV), já que a principal causa de morbilidade e mortalidade nesta população são as complicações macrovasculares (61). A hiperglicemia pós-prandial, associada ao aparecimento de hiperinsulinismo e insulino-resistência, tem sido recentemente reconhecida como um factor de risco importante para a DCV também na população em geral, e não apenas nos diabéticos (11,62,63). A obesidade visceral, insulino-resistência, dislipidemia e hipertensão formam uma constelação de patologias (interligadas entre si) que constituem a síndrome metabólica (64). Além da DCV, a intolerância à glicose está também associada a um risco aumentado de desenvolvimento de síndrome metabólica.
Assim, o conhecimento dos mecanismos que controlam os níveis de glicose plasmática, e mais especificamente a glicemia pós-prandial, é fundamental do ponto de vista clínico para o controlo e tratamento de patologias como a obesidade e a diabetes, reduzindo as suas complicações (1). De entre esses mecanismos destacam-se a absorçãointestinalde glicose, a acção das glicosidades intestinais e a captação de glicose pelos tecidos (esta última dependente da síntese de insulina e da sensibilidade tecidular periférica à sua acção) (15). Até 30 min após a ingestão alimentar, o aumento da concentração de glicose plasmática é atribuído somente à passagem de glicose, proveniente da absorção intestinal, para a corrente sanguínea. Uma vez atingido este momento, o metabolismo periférico da glicose (essencialmente a captação pelo músculo e adipócitos e o metabolismo hepático) tem um impacto significativo na glicemia, não podendo as diferenças ser unicamente explicadas pelos efeitos da absorção intestinal (65).
Na população em geral, e particularmente nos diabéticos e nos obesos, o bom controlo glicémico e insulinémico através da ingestão de uma dieta adequada e de terapia farmacológica que tenha como alvo a redução do transporte intestinal de glicose via SGLT1 e GLUT2 apical, permitem reduzir de forma significativa o risco de complicações macro- e microvasculares decorrentes da hiperglicemia (14,60).Aredução da absorçãointestinalde glicose nos diabéticos assume uma grande importância, pois estudos experimentais concluíram que nos diabéticos existe um aumento da capacidade de absorção intestinal de monossacarídeos (glicose e frutose) e que tal facto é, em parte, devido à sobre-expressão (ARNn e proteína) do GLUT2, do SGLT1 e do GLUT5 apicais (5, 14) e à sobre-regulação da ATPase-Na+/K+ (1, 66). A sobre-expressão destes transportadores, particularmente do SGLT1 apical, também poderá estar associada ao fenótipo de obesidade em humanos (5, 14).
A indústria farmacêutica tem vindo a desenvolver inibidores do SGLT1 semelhantes à floridzina (três patentes já foram registadas, ver em www.lamerie.com Janeiro 2006) e inibidores do GLUT2, com vista a atenuar o aumento da glicemia pós-prandial (5). Alguns trabalhos apontam para que alguns polifénois (catequinas, quercetina, miricetina, ácido clorogénico, ácido cafeico, neospiridina entre outros), devido ao potente efeito inibitório na captaçãointestinalde glicose possam, eventualmente, constituir algumas dessas alternativas (36,65,67,68).Adicionalmente, novas terapias que actuem de outra forma, quer modulando os factores de transcrição intestinais do SGLT1 e GLUT2, para em última instância aumentar ou diminuir a sua expressão, quer modulando as vias de sinalização intracelular responsáveis pelo recrutamento do GLUT2, poderão futuramente ser importantes.
CONCLUSÃO
Apesar de não ser um nutriente essencial, a glicose proveniente da dieta desempenha um papel importante na regulação dos níveis de glicose plasmática, após a sua absorçãointestinal. Sabe-se actualmente que a absorção intestinalde glicose é dependente de dois transportadores distintos, o SGLT1 e o GLUT2. O SGLT1, além da função de transportador de glicose, funciona também como um sensor de glicose, controlando a inserção apical do GLUT2 após a ingestão de uma refeição.
Aregulação da absorçãointestinalde glicose, com vista a manter a homeostasia da glicose plasmática, constitui um importante factor de protecção em patologias como a diabetes tipo 2, obesidade e síndrome metabólica. Por esse motivo, a elucidação dos mecanismos que modulam, aguda e cronicamente, o transporte intestinal de glicose, possibilitará desenvolver o campo da prevenção e das estratégias terapêuticas no combate a essas patologias. Neste contexto, o conhecimento de que a actividade e expressão quer do SGLT1 quer do GLUT2 apical ao nível intestinal são reguladas por uma série de factores abre uma nova possibilidade no tratamento dessas patologias, nomeadamente com o desenvolvimento de inibidores do SGLT1 ou do GLUT2, de moduladores dos factores de transcrição intestinais do SGLT1 e GLUT2 ou de moduladores das vias de sinalização intracelular responsáveis pelo recrutamento apical do GLUT2.
REFERÊNCIAS
1 -Drozdowski LA, Thomson AB. Intestinal sugar transport. World J Gastroenterol 2006;12:1657-70.
2 -Ferraris RP. Dietary and developmental regulation of intestinal sugar transport. J Biochem 2001;360:265-76.
3 -Field M. Intestinal ion transport and the pathophysiology of diarrhea. J Clin Invest 2003;111:931-43.
4 -Wright EM, Hirayama BA, Loo DF. Active sugar transport in health and disease. J Intern Med 2007;261:32-43.
5 -Wright EM, Martín MG, Turk E. Intestinalabsorptionin health and disease—sugar. Best Pract Res Clin Gastroenterol 2003;17:943-56.
6 -Hediger MA, Coady MJ, Ikeda TS, Wright EM. Expression cloning and cDNA sequencing of the Na+/glucose co-transporter. Nature 1987;330:379-81.
7 -Miyamoto K, Hase K, Takagi T, et al. Differential responses of intestinal glucose transporter mRNA transcripts to levels of dietary sugars. Biochem J 1993;295:211-5.
8 -Thomson AB, Wild G. Adaptation of Intestinal Nutrient Transport in Health and Disease. Part I. Dig Dis Sci 1997;42:453-69.
9 -Thomson AB, Wild G. Adaptation of Intestinal Nutrient Transport in Health and Disease. Part II. Dig Dis Sci 1997;42:470-88.
10 -Wilson JD, Foster DW, Kronenberg HM, Larsen PR. Williams Textbook of Endocrinology. 9th ed. Philadelphia: WB Saunders; 1998.
11 -Ludwig DS. The glycemic index physiological mechanisms relating to obesity, diabetes, and cardiovascular disease. JAMA 2002;287:2414-23.
12 -Wood IS, Trayhurn P. Glucose transporters (GLUT and SGLT): expanded families of sugar transport proteins. Br J Nutr 2003;89:3-9.
13 -Burant C. Facilitative glucose transport. In: Bittar E, editor. Principles of MedicalBiology.Amsterdam: Elsevier BV;1996. p. 67-86.
14 -Santer R, Hillebrand G, Steinmann B, Schaub J. Intestinal glucose transport: Evidence for a membrane traffic–based pathway in humans. Gastroenterol 2003;124:34-9.
15 -Sartorelli DS, Cardoso MA. Association between dietary carbohydrates and type 2 diabetes mellitus: epidemiological evidence. Arq Bras Endocrinol Metabol 2006;50:415-26.
16 -Wright EM, Loo DD. Coupling between Na+, sugar, and water transport across the intestine. Ann N Y Acad Sci 2000;915:54-66.
17 -Turk E, Martín MG, Wright EM. Structure of the human Na+/glucose cotransporter gene SGLT1. J Biol Chem 1994;269:15204-9.
18 -Kellett GL, Brot-Laroche E.Apical GLUT2 AMajor Pathway of Intestinal Sugar Absorption. Diabetes 2005;54:3056-62.
19 -Thorens B, Cheng ZQ, Brown D, Lodish HF. Liver glucose transporter: a basolateral protein in hepatocytes and intestine and kidney cells. Am J Physiol 1990;259: C279-C285.
20 -Walker J, Jijon HB, Diaz H, Salehi P, Churchill T, Madsen KL. 5-aminoimidazole-4-carboxamide riboside (AICAR) enhances GLUT2-dependent jejunal glucose transport: a possible role for AMPK. Biochem J 2005;385:485-91.
21 -Kellett GL, Brot-Laroche E, Mace OJ, Leturque A. Sugar absorption in the intestine: the role of GLUT2. Annu Rev Nutr 2008;28:35-54.
22 -Gonçalves P, Araújo JR, Azevedo I, Martel F. Lack of significant effect of cannabinoids upon the uptake of 2-deoxy-D-glucose by Caco-2 cells. Pharmacology 2008;82:30-7.
23 -Prager C, Cross HS, Peterlik M. Triiodothyronine stimulates 2-deoxy-D-glucose uptake by organ cultured embryonic chick small intestine. Acta Endocrinol (Copenh) 1990;122:585-91.
24 -Bissonnette P, Gagne H, Coady MJ, Benabdallah K, Lapointe JY, Berteloot A. Kinetic separation and characterization of three sugar transport modes in Caco-2 cells. Am J Physiol 1996;270:G833-43.
25 -Kellett GL. The facilitated component of intestinal glucose absorption. J Physiol 2001;531:585-95.
26 -Dyer J, Scott D, Beechey RB, Care AD, Abbas SK, Shi-razi-Beechey SP. Dietary regulation of intestinal glucose transport. In: Lentze MJ, Grand RJ, Naim HY, editors. Mammalian brushborder membrane proteins. Stuttgart: Thieme-Verlag;1994. p. 65-72.
27 -Monteiro IM, Jiang L, Ferraris RP. Dietary modulation of intestinal fructose transport and GLUT5 mRNA expression in hypothyroid rat pups. J Pediatr 1999;29:563-70.
28 -Drozdowski LA, Iordache C, Clandinin MT, Todd Z, Gonnet M, Wild G, Uwiera RR, Thomson AB. Maternal dexamethasone and GLP-2 have early effects on intestinal sugar transport in their suckling rat offspring. J Nutr Biochem 2008. doi:10.1016/j.jnutbio.2008.07.006
29 -Au A, Gupta A, Schembri P, Cheeseman CI. Rapid insertion of GLUT2 into the rat jejunal brush-border membrane promoted by glucagon-like peptide 2. Biochem J 2002;367:247-54.
30 -Shepherd EJ, Helliwell PA, Lister N, Mace OJ, Morgan EL, Patel N, Kellett GL. Stress and glucocorticoid inhibit apical GLUT2-trafficking and intestinal glucose absorption in rat small intestine. J Physiol 2004;560:281-90.
31 -Santos A, Gonçalves P, Araújo JR, Martel F. Intestinal permeability to glucose after traumatic brain injury: effect of gadopentetate dimeglumine administration. Basic Clin Pharmacol Toxicol 2008;103:247-54.
32 - Boudry G, Cheeseman CI, Perdue MH. Psychological stress impairs Na+-dependent glucose absorption and increases GLUT2 expression in the rat jejunal brush-bor-der membrane. Am J Physiol Regul Integr Comp Physiol 2007;292:R862-7.
33 -Zou MH, Kirkpatrick SS, Davis BJ, et al. Activation of the AMP-activated protein kinase by the anti-diabetic drug metformin in vivo: role of mitochondrial reactive nitrogen species. J Biol Chem 2004;279:43940-51.
34 -Cermak R, Landgraf S, Wolffram S. Quercetin glucosides inhibit glucose uptakeinto brush-border-membrane vesicles of porcine jejunum. Br J Nutr 2004;91:849-55.
35 -Chen CH, Hsu HJ, Huang YJ, Lin CJ. Interaction of flavonoids and intestinal facilitated glucose transporters. Planta Med 2007;73:348-54. [ Links ]
36 -Kwon O, Eck P, Chen S, et al. Inhibition of the intestinal glucose transporter GLUT2 by flavonoids. FASEB J 2007;21:366-77.
37 -Song J, Kwon O, Chen S, et al. Flavonoid inhibition of sodium-dependent vitamin C transporter 1 (SVCT1) and glucose transporter isoform 2 (GLUT2), intestinal transporters for vitamin C and Glucose. J Biol Chem 2002;277:15252-60.
38 -Lostao MP, Urdaneta E, Martinez-Anso E, Barber A, Martinez JA. Presence of leptin receptors in rat small intestine and leptin effect on sugar absorption. FEBS Lett 1998;423:302-6.
39 -Hirsh AJ, Cheeseman CI. Cholecystokinin decreases intestinal hexose absorption by a parallel reduction in SGLT1 abundance in the brush-border membrane. J Biol Chem 1998;273:14545-9.
40 -Matsui T, Tanaka T, Tamura S, et al. alpha-Glucosidase inhibitory profile of catechins and theaflavins. J Agric Food Chem 2007;55:99-105.
41 -Bryans J, Judd PA, Ellis PR. The effect of consuming instant black tea on postprandial plasma glucose and insulin concentrations in healthy humans. J Am Coll Nutr 2007;26:471-7.
42 -Ader P, Block M, Pietzsch S, Wolffram S. Interaction of quercetin glucosides with the intestinal sodium/glucose co-transporter (SGLT-1). Cancer Lett 2001;162:175-80.
43 -Ferraris RP, Diamond JM. Specific regulation of intestinal nutrient transporters by their dietary substrates. Annu Rev Physiol 1989;51:125-41.
44 -Ferraris RP, Diamond JM. Regulation of intestinal sugar transport. Physiol Rev 1997;77:257-302.
45 -Shirazi-Beechey SP, Hirayama BA, Wang Y, Scott D, Smith MW, Wright EM. Ontogenic development of lamb intestinal sodium-glucose co-transporter is regulated by diet. J Physiol 1991;437:699-708.
46 -Ortiz M, Lluch M, Ponz F. Influence of luminal Na+ on the intestinal absorption of sugars in vivo. Rev Esp Fisiol 1979;35:367-73.
47 -Bindslev N, Hirayama BA, Wright EM. Na+/D-glucose cotransport and SGLT1 expression in hen colon correlates with dietary Na+. Comp Biochem Physiol A Physiol 1997;118:219-27.
48 -Garriga C, Moreto M, Planas JM. Effects of resalination on intestinal glucose transport in chickens adapted to low Na+ intakes. Exp. Physiol 2000;85:371-8.
49 -Stümpel F, Burcelin R, Jungermann K, Thorens B. Normal kinetics of intestinal glucose absorption in the absence of GLUT2: evidence for a transport pathway requiring glucose phosphorylation and transfer into the endoplasmic reticulum. Proc Natl Acad Sci USA 2001;98:11330-5.
50 -Fedorak RN, Thomson ABR, Porter VM. Adaptation of intestinal glucose transport in rats with diabetes mellitus occurs independent of hyperphagia. Can J Physiol Pharmacol. 1991;69:1143-8.
51 -Garg ML, Keelan M, Thomson ABR, Clandinin MT. Intes--tinal microsomes: polyunsaturated fatty acid metabolism and regulation of enterocyte transport properties. Can J Physiol Pharmacol 1990;68:636-41.
52 -ThomsonABR, Keelan M, Clandinin MT. Feeding rats a diet enriched with saturated fatty acids prevents the inhibitory effects of acute and chronic ethanol exposure on the in vitro uptake of hexoses and lipids. Biochim Biophys Acta 1991;1084:122-8.
53 -Garg ML, Keelan M, Thomson ABR, Clandinin MT. Desaturation of linoleic acid in the small bowel is increased by short-term fasting and by dietary content of linoleic acid. Biochim Biophys Acta 1992;1126:17-25.
54 -Keelan M, Thomson ABR, Clandinin MT, Singh B, Rajotte R, Garg M. Improved intestinal form and function in diabetic rats fed long-term with a polyunsaturated fatty acid diet. Diabetes Res 1989;10:43-7. [ Links ]
55 -Riley SA, Warhurst G, Crowe PT, Turnberg LA. Active hexose transport across cultured human Caco-2 cells: characterisation andinfluence of culture conditions. Biochim Biophys Acta 1991;1066:175-82.
56 -Osswald C, Baumgarten K, Stumpel F, et al. Mice without the regulator gene Rsc1A1 exhibit increased Na+-D-glu-cose cotransport in small intestine and develop obesity. Mol Cell Biol 2005;25:78-87.
57 -Veyhl M, Spangenberg J, Püschel B, et al. Cloning of a membrane-associated protein which modifies activity and properties of the Na(+)-D-glucose cotransporter. J Biol Chem 1993;268:25041-53.
58 -Committee of the Japan Diabetes Society on the diagnostic criteria of diabetes mellitus. Report of the Committee on the classification and diagnostic criteria of diabetes mellitus. Diabetes Res Clin Pract 2002;55:65-85. [ Links ]
59 -Diabetes Atlas, 3rd edition. International Diabetes Federation, 2006.
60 -Duarte R, Rodrigues E, Duarte J, Duarte A, Ruas M. Recomendações da Sociedade Portuguesa de Diabetologia para o tratamento da hiperglicemia e factores de risco na diabetes tipo 2. Revista Portuguesa de Diabetes 2007;2 (Suppl 4):5-18. [ Links ]
61 -Diabetes Controland ComplicationsTrial(DCCT) Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med 1993;329:977-86.
62 -de Vegt F, Dekker JM, Ruhé HG, et al. Hyperglycaemia is associated with all-cause and cardiovascular mortality in the Hoorn population: the Hoorn Study. Diabetologia 1999;42:926-31. [ Links ]
63 -Dyer J, Wood IS, Palejwala A, Ellis A, Shirazi-Beechey SP. Expression of monosaccharide transporters in intestine of diabetic humans. Am J Physiol Gastrointest Liver Physiol 2002;282:G241-8.
64 -Rayssiguier Y, Gueux E, Nowacki W, Rock E, Mazur A. High fructose consumption combined with low dietary magnesium intake may increase the incidence of the metabolic syndrome by inducing inflammation. Magnes Res 2006;19:237-43.
65 -Johnston K, Sharp P, Clifford M, Morgan L. Dietary polyphenols decrease glucose uptake by human intestinal Caco-2 cells. FEBS Lett 2005;579:1653-7.
66 -Wild GE, Thompson JA, Searles L, Turner R, Hasan J, Thomson AB. Small intestinal Na+,K+-adenosine triphosphatase activity and gene expression in experimental diabetes mellitus. Dig Dis Sci 1999;44:407-14.
67 -Shimizu M, Kobayashi Y, Suzuki M, Satsu H, Miyamoto Y. Regulation of intestinal glucose transport by tea catechins. Biofactors 2000;13:61-5.
68 -Kobayashi Y, Suzuki M, Satsu H, et al. Green Tea Polyphenols Inhibit the Sodium-Dependent Glucose Transporter of Intestinal Epithelial Cells by a Competitive Mechanism. J Agric Food Chem 2000;48:5618-23.
Financiamento
Fundação para a Ciência e a Tecnologia e Programa Ciência, Tecnologia e Inovação do Quadro Comunitário de Apoio (PTDC/SAU-FCF/67805/2006).
Correspondência:
Dr.ª Fátima Martel
Departamento de Bioquímica
Faculdade de Medicina da Universidade do Porto
Alameda Prof. Hernâni Monteiro
4200-319 Porto
e-mail: fmartel@med.up.pt














