Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de Ciências Agrárias
versão impressa ISSN 0871-018X
Rev. de Ciências Agrárias vol.42 no.1 Lisboa mar. 2019
https://doi.org/10.19084/RCA18065
ARTIGO
Compostos voláteis da acerola (Malpighia emarginata) obtidos por HS-SPME em dois estágios de maturação
Volatile compounds of acerola (Malpighia emarginata) obtained by HS-SPME at two ripening stages
Gerby Giovanna Rondan-Sanabria1,2,*, Ausberta Jesus Cabezas Garcia2, Holger Saul Perez Montaño3, Erika Catherine Salas Arias1 e Narendra Narain2
1Dirección de Investigación, Universidad Tecnológica del Perú (UTP), Arequipa – Perú
2Laboratório de Análise de Flavor e Análises Cromatográficas, Universidade Federal de Sergipe 49100-000 São Cristóvão-SE, Brasil
3Departamento de Ciencias Naturales. Universidad Católica San Pablo, Arequipa – Perú
(*E-mail: C16238@utp.edu.pe)
RESUMO
O aroma é uma das principais características dos alimentos e é determinado por uma combinação de moléculas voláteis presentes na matriz, sendo um dos seus atributos mais atraentes para o consumidor. Neste trabalho foram identificados compostos voláteis presentes em dois estágios de maturação da acerola. Para a análise, utilizou-se a técnica da microextração em fase sólida por headspace (HS-SPME – HeadSpace Solid Phase MicroExtraction) associada com a cromatografia gasosa de alta resolução acoplada a espectrômetro de massa (GC-MS – Gas Chromatography - Mass Spectrometry). A influência das fibras na extração dos voláteis via SPME (CAR/PDMS e DVB/CAR/PDMS) foi avaliada. Os efeitos da temperatura de extração, concentração do meio de extração (cloreto de sódio - NaCl) e quantidade de amostra foram estudados usando-se o Delineamento Central Composto (DCC) para avaliar a maior eficiência de extração. Observou-se que, na acerola madura (vermelha) e semimadura (amarela) os compostos predominantes foram os ésteres, dentre eles o etil hexanoato o 4-pentenil-butanoato foram os que apresentaram maior concentração relativa. Esta identificação é uma informação importante para a indústria de aromas, que utilizam diferentes compostos aromáticos para a formulação de fragrâncias e aromas para serem usados em alimentos, cosméticos e perfumes.
Palavras-chave: Malpighia emarginata, compostos voláteis, HS-SPME, GC-MS.
ABSTRACT
Flavor is one of the main characteristics of food identified as a combination of volatile molecules present in the matrix and is one of its most attractive attributes to the consumer. In this research have been identified volatile compounds present in two stages of acerola maturation. For the analysis, have been used the following techniques and equipment: Headspace (HS-SPME) Solid Phase Microextraction Technique associated with High-Resolution Gas Chromatography coupled to mass spectrometer (GC-MS). The influence of SPME fibers (CAR / PDMS and DVB / CAR / PDMS) was evaluated on the volatiles extraction. The effects of extraction temperature, extraction medium concentration (NaCl) and amount of sample were studied using the Composite Central Delineation (CCD) to achieve the highest extraction efficiency. In mature (red) and semi-yellow (yellow) acerola the dominant compounds were esters; among them, ethylhexanoate and 4-pentenyl butanoate were the ones with the highest relative concentration. This identification is essential information for the flavors industry which use different aromatic compounds for the formulation of fragrances and aromas to be used in food, cosmetics, and perfumes.
Keywords: Malpighia emarginata, volatile compounds, HS-SPME, GC-MS.
INTRODUÇÃO
A diversidade de climas e microclimas fizeram do Brasil um país perfeito para a produção de frutas. Atualmente, é um dos três maiores produtores mundiais com uma produção que supera os 41 milhões de toneladas ao ano. Entre os muitos atributos atraentes que criam demanda por frutas de regiões tropicais e subtropicais é devido ao aroma perceptível característico. Alem disso, estas frutas são muitas vezes de baixo custo e extremamente ricas em vitaminas, podendo ser utilizadas em uma ampla gama de produtos alimentícios. A popularidade dessas frutas tem aumentado, especialmente na Europa e Estados Unidos. No Brasil, as frutas tropicais são consumidas frescas no local durante todo o ano e são exportadas para outros países, normalmente sob a forma de polpa congelada. Grande atenção tem sido dada para os compostos voláteis de uma grande variedade de frutas ao longo das últimas décadas (Carasek e Pawliszyn, 2006).
Em algumas frutas, os compostos de impacto individuais foram identificados como sendo responsáveis por um aroma característico, mas a maioria de aromas parece ser a contribuição de um grande número de compostos voláteis (Marostica e Pastore, 2007). Segundo a literatura, a identificação dos compostos voláteis de frutas tropicais exóticas estão ainda sendo estudados. Além disso, observa-se que os ésteres e os terpenos são os voláteis mais prolíficos nas frutas os quais predominariam no aroma. Além do mais segundo a literatura uma das técnicas mais empregadas para extrair os voláteis é HS-SPME (Souza-Silva et al., 2015). Portanto, existe um crescente interesse neste campo para elucidar se os perfis de aroma de frutas e vegetais frescos são afetados pelo sistema de cultivo o armazenamento (Vallverdú-Queralt e Lamuela-Raventós, 2016).
Pode-se citar, por exemplo, a polpa da acerola que é muito suculenta e possui um aroma frutado e doce, mas a fruta é principalmente conhecida por ser rica em vitamina C, sendo uma das principais fontes naturais dessa vitamina. A cor vermelha atrativa da fruta é devido às antocianinas presentes na casca. Também é fonte de carotenóides e compostos fenólicos (Vendramini e Trugo, 2004) que participam como antioxidantes no sistema biológico. Schippa et al. (1993) relataram o primeiro trabalho sobre a composição de compostos voláteis da acerola, utilizando extração com o solvente diclorometano, e os compostos mais dominantes foram o 3-metil-3-buteno-1-ol, seguido por ésteres (acetato, propionato, butanoato, hexanoato e octanoato). Segundo os autores, estes compostos eram em sua maioria responsáveis pelo aroma da fruta.
Neste trabalho, foi realizada a otimização de extração de compostos voláteis da acerola por HS-SPME – técnica caracterizada por sua rapidez, variabilidade, linearidade, boa cinética de saturação e minimização dos efeitos de matriz – em combinação com GC-MS, em que foram utilizadas colunas capilares com altas taxas de fluxo linear, com o objetivo de isolar e identificar os compostos orgânicos voláteis da acerola em dois estágios de maturidade.
MATERIAIS E MÉTODOS
Materiais
Acerolas nos estágios maduro (vermelha) e semimaduro (amarelo) foram compradas em um supermercado de Aracaju, Brasil, e transportadas ao laboratório. As frutas frescas, com ausência de lesões ou deterioração microbiana aparente nas cascas, foram selecionadas de acordo ao estado de maturidade e lavadas com solução de hipoclorito de sódio a 1%.
Um amostrador de SPME e fibras revestidas com carboxen/polidimetilsiloxano (CAR/PDMS) 85 μm e divinilbenzeno/carboxen/polidimetilsiloxano (DVB/CAR-PDMS) 50/30 μm foram adquiridas da Supelco (Bellefonte, PA, USA). O cloreto de sódio foi adquirido da Sigma Chemical Co. (Aldrich Chemical Co.) e a água destilada empregada foi do sistema de purificação Milli-Q da Millipore.
Seleção da fibra de SPME na extração dos compostos voláteis
O despolpamento da acerola foi realizado manualmente. Após a extração da semente, a polpa e a casca foram homogeneizadas em liquidificador comum sem adição de água e peneiradas. O homogenato resultante foi acondicionado em sacos de polietileno de baixa densidade e armazenado em freezer a -20 °C até a realização das análises.
Para a seleção da fibra, foram realizados testes com fibras CAR/PDMS e DVB/CAR-PDMS com o intuito de verificar a capacidade de coletar e concentrar os voláteis da polpa no HS (headspace). Essas fibras foram dispostas no HS em frascos de 40 mL hermeticamente fechados com uma rolha de polipropileno, contendo uma mistura com 3,5 g de amostra e 10 mL de água deionizada, durante 30 min a 25 °C, sob agitação magnética constante. Após extração, as fibras de SPME foram retiradas dos frascos e inseridas no sistema de injeção do GC-MS para a separação e identificação de voláteis. O tempo de dessorção térmica foi de 8 min a 250 °C no modo split. O número de picos detectados foi uma variável de resposta tanto para a seleção da fibra e como para a otimização das condições de extração.
Planejamento experimental
A otimização do procedimento experimental foi realizada através do delineamento central composto (DCC), com três variáveis e cinco níveis (-1,68, -1, 0, +1, 1,68) e 3 triplicatas no ponto central, totalizando 17 experimentos. As condições experimentais no ponto central foram: força iônica de 15% de NaCl, temperatura de 40 ºC e o peso da amostra de 2,5g. Os valores experimentais foram: concentração de NaCl - x1 = 0, 6, 15, 24 e 30%; temperatura - x2 = 30, 34, 40, 46 e 50 ºC e amostra - x3 = 0,8, 1,5, 2,5, 4, 2,5 (Quadro 1).
O número de picos detectados, em cada corrida, foi usado como uma variável de resposta do DCC e um modelo quadrático foi construído para descrever os dados observados. As condições de cada extração foram realizadas seguindo o planejamento experimental (Quadro 1) e foi empregada a fibra que apresentou o melhor resultado em relação ao número de picos absorvidos. O tempo de equilíbrio e o tempo da extração para cada análise foram de 15 e 30 min., respectivamente. Todas as análises foram realizadas em duplicata.
Análise cromatográfica
Nas análises cromatográficas usou-se um sistema de GC (Agillent CG-7820A) - MS (Agilent MS-5975) equipado com uma coluna capilar DB-5 (30 m x 0,25 mm de diâmetro interno, 0,25 µm de espessura do filme). Após injeção, a programação de temperatura para a coluna foi: início a 40 °C durante 4 min, aumentando-se 7 °C/min até atingir 160 °C onde permaneceu por 8 min, seguido por um aumento de 15 °C/min até 250 °C onde foi mantido por 3 minutos, totalizando 38 min de corrida cromatográfica. O hélio foi usado como gás de arraste em uma proporção constante de 1,0 mL/min. O detector de massa foi operado por impacto de elétrons (EI)-mode de 70 eV em uma faixa de 29 – 550 m/z. A identificação dos componentes voláteis foi realizada por meio do cálculo do índice de retenção linear (RI) de cada composto, usando uma série de padrões de n-alcanos (C8-C24) (Sigma Chemical Co., St. Louis) nas mesmas condições das amostras e por comparação do espectro de massa de um composto desconhecido com a biblioteca espectral de massa NIST/EPA/NIH, versão 2.0. Os valores dos índices de retenção (RI) de cada composto também foram comparados com os descritos na literatura referentes a outras frutas e vegetais os quais foram determinados nos mesmos equipamentos e condições anteriores. As concentrações relativas dos componentes individuais foram expressas como porcentagem das áreas de pico relativas à área total do pico.
Análise estatística
A significância estatística do modelo foi avaliada por análise de variância (ANOVA), a um nível de significância de 5% (p < 0,05). A ANOVA e a superfície de resposta foram geradas pelo programa STATISTICA v. 7 Statsoft Inc., Tulsa, OK, USA.
RESULTADOS E DISCUSSÃO
Seleção do revestimento da fibra
Neste estudo foram avaliadas duas fibras semipolares CAR/PDMS e a DVB/CAR-PDMS, e comparadas individualmente. Os resultados mostraram que, ambas as fibras conseguiram extrair compostos similares, dos quais os mais representativos foram o etil hexanoato, e o 3-metil-3-buten-1-ol, 4-pentenil butanoato e etil octanoato (Figura 1). No entanto, a fibra CAR/PDMS, foi a que apresentou uma elevada eficiência de extração dos compostos voláteis. Comparando os cromatogramas das duas fibras testadas, foram detectados 50 picos quando empregada a fibra DVD/CAR/PDMS e 65 picos com a PDMS/CAR. Baseado no perfil apresentado por este revestimento, a fibra CAR/PDMS foi selecionada para a caracterização dos compostos voláteis da polpa da acerola.
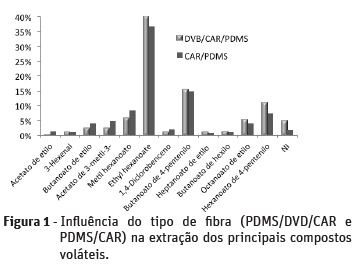
Bicchi et al. (2000) observaram que a fibra mais eficaz para o HS‑SPME de compostos voláteis é aquela composta por um líquido (PDMS) para os componentes menos polares e um revestimento sólido (DVD, CAR ou ambos) para os componentes mais polares. Similarmente, Augusto et al. (2000) concluíram que os dois revestimentos DVD/CAR seriam um meio de filtrar compostos voláteis de algumas polpas de frutas e sugeriram que a combinação destas duas fibras seria o revestimento mais eficiente para a extração de compostos mais leves. Contudo, o revestimento desta fibra (CAR/PDMS) foi a mais apropriada para a extração de moléculas pequenas. A sensibilidade desta fibra em moléculas menores, tais como ésteres, ácidos e compostos não polares, permitiria a extração de uma ampla faixa de compostos aromáticos.
Delineamento central composto e identificação de compostos voláteis da acerola
Os resultados dos 17 experimentos são mostrados no Quadro 1 e na Figura 2. As respostas baseadas no número de picos é um dos parâmetros mais empregados na otimização das condições de extração por SPME e, portanto empregado como ponto final nestes estudos para avaliar a significância de cada uma das variáveis estudadas. Uma análise de variância (ANOVA) foi realizada para determinar se os fatores experimentais estudados foram significativos (p<0,05) sobre o desempenho do sistema HS-SPME. Os principais efeitos e suas interações são apresentados no diagrama de Pareto, mostrado na Figura 2.
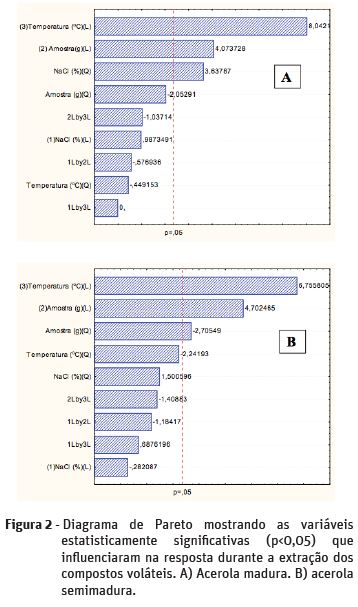
A Figura 2A mostra os resultados obtidos para a acerola madura, e pode-se observar que a quantidade de amostra (x2), a temperatura de extração (x3) e o termo quadrático da força iônica (x1x1) foram altamente significativos (p<0,05) e influenciaram positivamente na extração dos compostos voláteis. Estas variáveis influenciaram grandemente na pressão de vapor e do equilíbrio dos compostos voláteis no espaço livre da amostra, o que indicaria que aumentando estes valores, também incrementaria o sinal do composto. Assim, é possível atribuir a alta eficiência da fibra de SPME ao aumento da concentração dos compostos menos voláteis no espaço superior (devido à temperatura de extração superior) do que a extração dos compostos altamente voláteis à fibra.
A Figura 2B representa os resultados da acerola semimadura e, observa-se que a temperatura de extração (x3), a quantidade de amostra (x2) e o termo quadrático da concentração do sal foram significativos (p<0,05). Dessas variáveis, influenciaram positivamente a temperatura e a quantidade de amostra. No entanto, o valor negativo indicaria um efeito oposto sobre a resposta analítica.
O número de picos obtidos em cada experimento foi usado para obter a superfície de resposta que estão apresentados na Figura 3A e 3B. Estes resultados representam os valores máximos alcançados tanto para a temperatura de extração, para a quantidade de amostra e para a concentração de NaCl. Os gráficos mostram que a melhor resposta (número de picos) foi atingida quando a temperatura de extração estava na faixa de 46 oC, a quantidade de amostra era de 4 gramas a 24% de NaCl. O delineamento experimental apresentou um valor R de 0,947 para a acerola madura e 0,93 para a acerola semimadura, ambos considerados valores adequados para o planejamento. Neste ponto, foram separados 81 compostos voláteis da polpa da acerola madura e 64 da acerola semimadura, os quais estão mostrados na Figura 4 e Quadro 2.
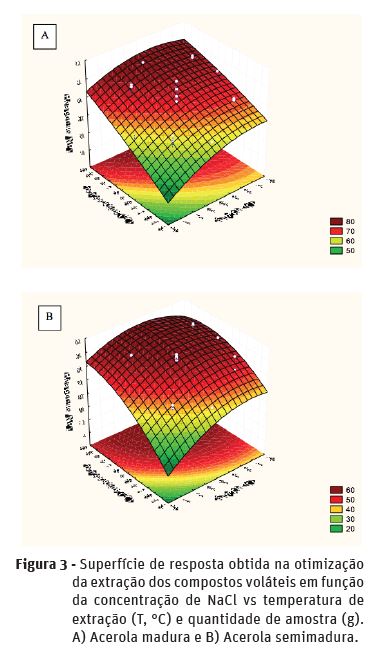
Segundo nossos resultados podemos dizer que a adição de um sal inerte à amostra produz um aumento da força iónica o que acarreta a diminuição da solubilidade de inúmeros compostos em água, favorecendo a extração dos analitos (efeito salting-out). Igualmente o tempo de extração afeta diretamente a extensão da extração de compostos voláteis e semi-voláteis sendo que, teoricamente, para tempos de extração maiores uma maior parcela de compostos será extraída. Do mesmo modo a temperatura é um dos parâmetros mais importantes na extração dos compostos por difusão gasosa visto que o transporte de massa é baseado na volatilização dos compostos.
Identificação dos compostos voláteis da polpa da acerola
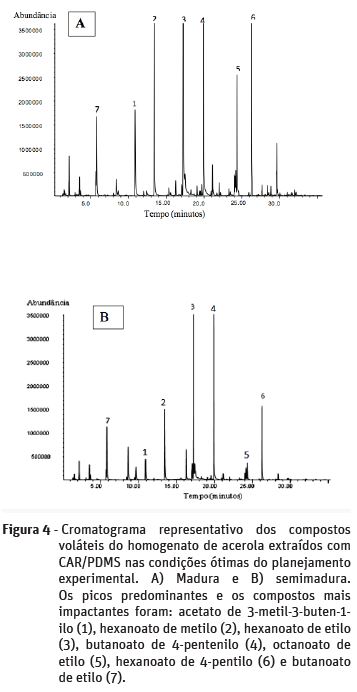
A Figura 4 representa os cromatogramas da melhor condição de extração. Os números mostram os compostos que apresentaram maior intensidade e possíveis responsáveis pelo aroma da fruta. No Quadro 2 estão listados todos os compostos que foram detectados e identificados. Foram identificados 55 compostos na acerola madura e 51 na semimadura, de acordo com a semelhança dos seus espectros de massa e por comparação com os valores padrão descritos na literatura, dentre os compostos identificados, os ésteres foram os mais predominantes nos dois estágios de maturidade. O etil hexanoato foi o pico mais impactante em ambos os estágios representando 36,7% de concentração relativa na fruta madura e 27,6% na semimadura, seguido do 4-pentenil butanoato com 14,8% na madura e 20,81% na semimadura. Apesar de apresentarem muitos compostos em comum, foram identificados alguns compostos presentes somente na acerola madura tais como furfural, 3-metil octanoto, etil-4-octanoato e metil-4-decanoato. Na acerola semimadura foi identificado o (E)-hexenil acetato, (E)-2-hexen-1-ol, 3-octanol e β-ionone.
Na literatura, poucos artigos referentes à composição do aroma da acerola são encontrados (Schippa et al., 1993; Boulanger e Crouzet, 2001; Carasek e Pawliszyn, 2006), dentre os quais Boulanger e Crouzet (2001) identificaram 46 compostos voláteis livres, onde os álcoois (3-metil-3-buten-1-ol, 3-metil-butan-1-ol e 2-metil-butan-1-ol) eram predominantes na fração volátil. Outros estudos (Schippa et al., 1993; Carasek e Pawliszyn, 2006) também identificaram estes alcoóis na polpa da acerola.
Pino e Marbot (2001) detectaram a presença de diferentes compostos incluindo monoterpenóides os quais não foram encontrados em outros estudos. Os autores investigaram os compostos voláteis de acerola cultivada em Cuba e identificaram furfural, ácido hexadecanóico, 3-metil-3-buten-1-ol e limoneno como os compostos de maior intensidade. Outro grupo estudou os efeitos na composição química dos compostos voláteis da acerola em três estágios de maturidade, onde foi observado que o perfil do aroma vai incrementando com o estágio de maturidade. Foram identificados 14 compostos no fruto imaturo, 23 no intermediário tais como metil hexanoato e 3-octen-1-ol e nos frutos maduros identificaram 31 compostos, entre eles acetil- metil-carbinol e etil hexanoato. Os autores também observaram que, quando imaturo, o odor prevaleceu durante a primeira fase de maturação, as concentrações de ésteres eram baixas e incrementaram durante a maturação (Vendramini e Trugo, 2004).
A abundância de ésteres em frutas é bastante comum e relatada por vários autores em estudos dos perfis voláteis de diversas frutas, como em germoplasma de manga chinesa, Borojoa Sorbiles fruta da Amazônia, groselha preta, cajá, graviola, cupuaçu, goiaba, banana e uva, normalmente, esta classe está envolvida com as notas de aromas frutais da fruta (Augusto et al., 2000; Porat et al., 2011; Ma et al., 2018; Rabelo et al., 2018; Marsol-Vall et al., 2018). Estes autores detectaram a presença de aldeídos tais como furfural, nonanal e hexenal, ésteres como o butanoato de etilo, butanoato de metilo, hexanoato de metilo entre outros os quais foram também identificados na acerola.
CONCLUSÕES
Neste estudo a combinação da técnica de HS-SPME na captura de compostos voláteis empregando um sistema de CG-MS resultou em um método eficiente com o qual foi possível identificar uma grande quantidade de compostos voláteis, dos quais os ésteres foram os compostos predominantes nos dois estágios de maturidade. Entre as fibras testadas (CAR/PDMS e DVB/CAR/PDMS), a CAR/PDMS foi a mais eficiente na extração de maior número de compostos. Os compostos mais impactantes foram o 3- acetato de 3-metil-3-buten-1-ilo, hexanoato de metilo, hexanoato de etilo, butanoato de 4-pentenilo, octanoato de etilo, hexanoato de 4-pentilo e butanoato de etilo, dentre eles este último poderia ser o principal responsável pelo aroma da fruta.
REFERENCIAS BIBLIOGRAFICAS
Acree, T. & Arn, H. (2004) – Flavornet. <http://www.flavornet.org> [ Links ]
Augusto, F.; Valente, A.L.P.; Tada, E.S. & Rivellino, S.R. (2000) - Screening of Brazilian fruit aromas using solid-phase microextraction-gas chromatography-mass spectrometry. Journal of Chromatography, vol. 873, n. 1, p. 117-127. https://doi.org/10.1016/S0021-9673(99)01282-0 [ Links ]
Beaulieu J.C. & Lea, J.M. (2006) - Characterization and semiquantitative analysis of volatiles in seedless watermelon varieties using solid-phase microextraction. Journal of Agricultural and Food Chemistry, vol. 54, n. 20, p. 7789-7793. https://doi.org/10.1021/jf060663. [ Links ]
Bicchi, C.; Drigo, S. & Rubiolo, P. (2000) - Influence of fiber coating in headspace solid-phase microextraction-gas chromatographic analysis of aromatic and medicinal plants. Journal of Chromatography A, vol. 892, n. 1-2, p. 469-485. https://doi.org/10.1016/S0021-9673(00)00231-4 [ Links ]
Boulanger, R. & Crouzet, J. (2001) - Identification of the aroma components of acerola (Malphigia glabra L.): free and bound flavor compounds. Food Chemistry, vol. 74, n. 2, p. 209-216. https://doi.org/10.1016/S0308-8146(01)00128-5 [ Links ]
Carasek, E. & Pawliszyn, A. (2006) - Screening of tropical fruit volatile compounds using Solid-Phase Microextraction (SPME) fibers and internally cooled SPME fiber. Journal Agricultural and Food Chemistry, vol. 54, n. 23, p. 8688−8696. https://doi.org/10.1021/jf061394. [ Links ]
Érica, A.; Souza, S.; Saboia, G.; Nina, C.J.; Hoffmann, C.; Dos Santos, R.S.I.; Geraldo, L.G.; Soares, G.L. & Zini, C.A. (2017) - Development of a HS-SPME-GC/MS protocol assisted by chemometric tools to study herbivore-induced volatiles in Myrcia splendens. Talanta, vol. 175, p. 9-20. https://doi.org/10.1016/j.talanta.2017.06.063 [ Links ]
Lasekan, O.; Khatib, A.; Juhari, H.; Patiram, P. & Lasekan, S. (2013) - Headspace solid-phase microextraction gas chromatography–mass spectrometry determination of volatile compounds in different varieties of African star apple fruit (Chrysophillum albidum). Food Chemistry, vol. 141, n. 3, p. 2089–2097. https://doi.org/10.1016/j.foodchem.2013.05.08. [ Links ]
Liu, F.-X.; Fu, S.-F.; Bi, X.-F. & Chen, F. (2013) - Physico-chemical and antioxidant propiertes of four mango (Mangifera indica L.) cultivars in China. Food Chemistry, vol. 138, n. 1, p. 396-405. https://doi.org/10.1016/j.foodchem.2012.09.11. [ Links ]
Ma, X.W.; Su, M.Q.; Wu, H.X.; Zhou, Y.G. & Wang, S.B. (2018) - Analysis of the Volatile Profile of Core Chinese Mango Germplasm by Headspace Solid-Phase Microextraction Coupled with Gas Chromatography-Mass Spectrometry. Molecules, vol. 23, n. 6, art. 1480. https://doi.org/10.3390/molecules2306148. [ Links ]
Marsol-Vall, A.; Kortesniemi, M.; Karhu, S.T.; Kallio, H. & Yang, B. (2018) – Profiles of volatilecompounds in Blackcurrant (Ribes nigrum) cultivars with a special focus on the influence of growth latitude and weather conditions. Journal of Agriculture and Food Chemistry, vol. 66, n. 28, p. 7485-7495. https://doi.org/10.1021/acs.jafc.8b0207. [ Links ]
Marostica, M.R. & Pastore, G.M. (2007) - Tropical fruit flavor. In: Flavor and Fragrance, p. 189–201. Berge, R.G., Ed., Springer, Berlin. [ Links ]
Pino, J.A. (2012) - Odour-active compounds in mango (Mangifera indica L. cv. Corazón). International Journal of Food Science and Technology, vol. 47, n. 9, p. 1944–1950. https://doi.org/10.1111/j.1365-2621.2012.03054 [ Links ]
Pino, J.A. & Marbot, R. (2001) - Volatile flavor constituents of acerola (Malpighia emarginata DC.) fruit. Journal of Agricultural and Food Chemistry, vol. 49, n. 12, p. 5880−5882. https://doi.org/10.1021/jf010270g [ Links ]
Porat, R.; Tietel, Z.; Zippori, I. & Dag, A. (2011) - Aroma volatile compositions of high-and low-aromatic guava varieties. Journal of Agricultural and Food Chemistry, vol. 91, n. 15, p. 2794–2798. https://doi.org/10.1002/jsfa.452. [ Links ]
Rabelo, R.F.; de Souza, R.A.; Fernandes, A.A.C.; Pinto, F.J.L.; da Silva, C.C. & Rocha, A.S.J. (2018) - Evaluation of Amazon fruits: chemical and nutritional studies on Borojoa sorbilis. Journal of the Science of Food and Agriculture, vol. 98, n. 10, p. 3943-3952. https://doi.org/10.1002/jsfa.891. [ Links ]
Sampaio, T.S. & Nogueira, P.C.L. (2006) - Volatile components of mangaba fruit (Hancornia speciose Gomes) at three stages of maturity. Food Chemistry, vol. 95, n. 4, p. 606–610. https://doi.org/10.1016/j.foodchem.2005.01.038 [ Links ]
Schippa, C.; George, G. & Fellous, R. (1993) - Constituants volatils de l'acérola. Parfums, Cosmétiques, Arômes, vol. 113, p. 81−84. [ Links ]
Souza-Silva, É.A.; Gionfriddo, E. & Pawliszyn, J. (2015) - A critical review of the state of the art of solid-phase microextraction of complex matrices II. Food analysis. TrAC Trends in Analytical Chemistry, vol. 71, p. 236-248. https://doi.org/10.1016/j.trac.2015.04.01. [ Links ]
Vallverdú, Q.A. & Lamuela-Raventós, R.M. (2016) - Foodomics: A new tool to differentiate between organic and conventional foods. Electrophoresis, vol. 37, n. 13, p. 1784-1794. https://doi.org/10.1002/elps.20150034. [ Links ]
Vendramini, A.L. & Trugo, L.C. (2004) - Chemical composition of acerola fruit (Malpighia punicifolia L.) at three stages of maturity. Food Chemistry, vol. 71, n. 2, p. 195−198. https://doi.org/10.1016/S0308-8146(00)00152-7 [ Links ]
AGRADECIMENTOS
Os autores agradecem ao Instituto Nacional de Ciência e Tecnologia (INCT) de Frutas Tropicais, ao CNPq e a CAPES pelo fornecimento do apoio financeiro para o desenvolvimento do projeto.
Recebido/received: 2018.03.10
Recebido em versão revista/received in revised form: 2018.08.15
Aceite/accepted: 2018.08.30














