Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de Ciências Agrárias
versão impressa ISSN 0871-018X
Rev. de Ciências Agrárias vol.42 no.1 Lisboa mar. 2019
https://doi.org/10.19084/RCA18160
ARTIGO
Distinção de espécies e estádios de maturação de sementes de Comanthera spp. por análise de imagem e citometria de fluxo
Distinction of species and maturation stages of Comanthera spp. by image analysis and flow cytometry
Elizabeth R. Marques1,*, Janaína G. R. de Assis1, Fernanda O. Bustamante2, Dayliane B. de Andrade1, Maria L. M. de Carvalho1 e Camila Aparecida Lopes1
1Departamento de Agricultura, produção e tecnologia de sementes, Universidade Federal de Lavras, Lavras MG, Brasil
2 Departamento de Genética, Centro de Ciências Biológicas, Universidade Federal de Pernambuco, Recife PE, Brasil
(*E-mail: bethagro@yahoo.com.br)
RESUMO
Comanthera spp. são perenes e comumente utilizadas para ornamentação, de alto valor económico e social, esse fato tem comprometido a conservação de populações pelo fato de serem colhidas antes da maturação das sementes. O primeiro ensaio foi realizado para verificar a eficiência do sistema de análise de imagens na distinção de espécies de Comanthera em diferentes estádios de desenvolvimento das inflorescências, bem como o potencial germinativo das sementes. O segundo ensaio foi realizado com o objetivo de estimar o conteúdo de DNA nuclear na distinção de espécies, estabelecer o tampão adequado para isolamento de núcleos interfásicos e investigar a viabilidade de utilização de diferentes partes da planta para análises em citometria de fluxo. Constatou-se que o sistema de análise de imagens tem potencial para diferenciar espécies e estádios de desenvolvimento de inflorescências de sempre-viva. A espécie C. elegans possui valores de germinação superiores nos estádios 4 e 5, que apresentam capítulo com mais de 60% de abertura. Folhas, raízes e sementes de C. bisulcata, C. elegans e C. nitida podem ser utilizadas para quantificação de DNA nuclear em citometria. O tampão Marie é indicado para extração de DNA de tecidos foliares e radiculares e o tampão LB01 das sementes.
Palavras-chave: germinação; GroundEye®; Syngonanthus spp.
ABSTRACT
Comanthera spp. are perennial and commonly used for ornamentation, of high economic and social value, this fact has compromised the conservation of populations because they are harvested before the maturation of the seeds. The first experiment was carried to verify the efficiency of the image analysis system in the distinction of two Comanthera species at different development stages of inflorescence, as well as the germination potential of the seeds. The second assay was carried out to estimate the nuclear DNA content in the species distinction, establish the appropriate buffer for the isolation of interphase nuclei and investigate the feasibility of using different parts of the plant for analysis by flow cytometry. It was verified that the image analysis system has the potential to differentiate species and development stages of inflorescence of sempre-vivas. The C. elegans species has higher germination values in stages 4 and 5, presenting a head with opening higher than 60%. Leaves, roots and seeds of C. bisulcata, C. elegans and C. nitida can be used for quantification of nuclear DNA by cytometry. The Marie buffer is indicated for the extraction of DNA from leaf and root tissues and the LB01 buffer for seeds.
Keywords: germination; GroundEye®; Syngonanthus spp.
INTRODUÇÃO
Comanthera spp. são conhecidas como sempre-vivas por seus escapos e inflorescências conservarem um aspeto vivo mesmo depois de colhidas e secas. A coleta de sempre-vivas, principalmente as pertencentes ao género Comanthera é intensiva pelo alto valor de mercado, sendo de grande importância para a população da sua área (Giulietti et al., 2012).
Esse fato tem comprometido a conservação de populações naturais com a remoção de inflorescências que pode ocorrer antes mesmo da produção de sementes ou da maturação completa e consequentemente havendo uma redução no tamanho da população natural (Oliveira et al., 2015). Algumas espécies desse género estão incluídas na lista de espécies ameaçadas de extinção, tornando-se necessárias medidas que garantam a sua conservação.
O aspeto da inflorescência poderia ser um indicativo do ponto ideal de colheita, no entanto as diferenças morfológicas subtis entre as inflorescências nem sempre podem ser detectadas pela análise visual.
O uso de análises de imagens obtidas por câmeras de alta precisão tem-se tornado uma ferramenta promissora por ser um método rápido e não destrutivo e que possibilita a análise individual de sementes durante as fases de coleta, classificação, distribuição ou até reconhecimento inicial da espécie (Dias et al., 2010; Andrade et al., 2016).
A criação de parâmetros visuais fixos para classificação de flores através da análise de imagens pode ser uma maneira de minimizar a subjetividade, garantindo lotes mais uniformes (Dias et al., 2010). Além disso, a informação sobre o comportamento germinativo das sementes em diferentes estádios de desenvolvimento das inflorescências pode fornecer informações para práticas de exploração sustentável.
Estudos que caracterizem as espécies de Comanthera são escassos na literatura e dizem respeito apenas ao estabelecimento da espécie in vitro (Albuquerque et al., 2016; Lima-Brito et al., 2016), germinação de sementes (Oliveira et al., 2016), taxonomia, sistemática (Echternacht et al., 2015), aspetos da morfologia (Giulietti et al., 2012), anatomia (Oliveira et al., 2015) e marcadores microssatélites (Leal et al., 2014).
A citometria de fluxo é uma técnica que permite a estimativa da quantidade de DNA nuclear e tem sido reconhecida como um relevante parâmetro para caracterização genômica, com aplicabilidade em estudos evolutivos, biodiversidade (Knight e Beaulieu, 2008), biologia celular, ecologia, filogenia, melhoramento, sistemática e taxonomia vegetal (Kolar et al., 2009).
O uso de uma solução tampão adequada é importante para a estimativa correta da quantidade de DNA, no isolamento e manutenção da integridade dos núcleos da amostra a ser analisada em citometria. A utilização de folhas jovens é a mais comum em análises de citometria de fluxo, entretanto, em alguns casos pode ser mais conveniente utilizar sementes, pela facilidade de serem transportadas e sem precisar esperar o tempo da emergência de raízes ou mesmo o crescimento foliar.
A pesquisa foi realizada com objetivo de verificar a eficiência do sistema de análise de imagens na distinção de espécies de Comanthera em diferentes estádios de desenvolvimento das inflorescências, bem como o potencial germinativo das sementes. Além disso, objetivou-se o conteúdo de DNA nuclear na distinção de três espécies, estabelecer o tampão adequado para isolamento de núcleos interfásicos e investigar a viabilidade de utilização de diferentes partes da planta para análises em citometria de fluxo.
MATERIAIS E MÉTODOS
A coleta das inflorescências das sempre-vivas (Comanthera elegans, Comanthera nitida e Comanthera bisulcata) foi realizada na Cadeia do Espinhaço município de Diamantina-MG entre os meses de maio a agosto de 2015 em locais representativos da área de produção.
As inflorescências foram selecionadas de acordo com avanço da maturação em diferentes estádios de desenvolvimento. Foram utilizadas quatro repetições de 50 inflorescências em cada estádio de maturação pertencentes às espécies C. elegans e C. nitida popularmente conhecidas como pé-de-ouro e sapatinha. (Quadro 1).

Análise de imagens – As inflorescências nos diferentes estádios de desenvolvimento foram colocadas separadamente sobre a bandeja de acrílico transparente do Sistema de Análise de Imagens Groundeye® S800, versão 1.3.5. As imagens foram capturadas por câmeras de alta resolução contidas dentro da câmara de captação do equipamento. O modelo de cor utilizado para análise foi o HSV (Hue, Saturation and Value) com índice de Matiz de 191,90 a 261,20, Saturação de 0,00 a 1,00 e Brilho de 0,00 a 1,00.
Para extração das sementes, as inflorescências das sempre-vivas foram trituradas em liquidificador durante 30 segundos. Sementes e impurezas foram separadas com o auxílio de peneiras para obtenção das sementes puras as quais foram utilizadas para o teste de germinação.
Determinação do teor de água - A determinação do teor de água foi obtida pelo método de estufa a 130 ºC durante 1 hora, utilizando-se duas subamostras de 0,1g para cada espécie. Os resultados foram expressos em porcentagem média em base úmida (Brasil, 2009).
Germinação - O teste de germinação foi conduzido com quatro repetições de 50 sementes por tratamento, com a semeadura em papel de germinação tipo mata-borrão umedecido com água destilada na proporção de 2,5 vezes o peso do papel. As sementes permaneceram em BOD durante 35 dias em temperatura alternada de 25-15 °C e fotoperíodo de 12 horas (Pereira et al., 2014). Os resultados foram expressos em porcentagem média de plântulas normais.
Para as sementes remanescentes do teste de germinação, realizou-se o teste de tetrazólio para a determinação de sua viabilidade, e os dados foram somados aos do teste de germinação. As sementes foram colocadas em solução 0,5% de cloreto 2,3,5 trifenil tetrazólio por 3 horas, no escuro, na temperatura de 30 °C até coloração para análise.
Análise estatística – Para o primeiro ensaio adotou-se o delineamento inteiramente casualizado em esquema fatorial (6x2) sendo seis estádios de desenvolvimento da inflorescência e duas espécies de sempre-vivas. As médias obtidas nos dois ensaios foram comparadas pelo teste de Scott Knott a 5% de probabilidade com o auxílio do programa estatístico Sisvar (Ferreira, 2011).
Quantificação do DNA nuclear - A quantificação de DNA nuclear foi realizada para as espécies C. bisulcata, C. elegans e C. nitida. As estimativas de DNA foram obtidas a partir de três tecidos das espécies avaliadas: sementes, folhas e raízes. As folhas e radículas foram obtidas de plântulas contendo 2 a 3 folhas, com 1 cm de comprimento, oriundas de sementes germinadas in vitro em meio MS, acrescidas de 15 g L-1 de sacarose e solidificadas com 8 g L-1 de ágar (Pêgo et al., 2013). O pH do meio foi ajustado para 5,8 antes da autoclavagem à pressão de 1,5 atm e à temperatura de 120°C por 20 minutos. As plantas foram inoculadas em tubos de ensaio contendo 10 mL de meio de cultura e mantidas por 30 dias em sala de crescimento sob luz constante à temperatura de 25 ± 2°C. Para cada amostra foram utilizados, aproximadamente, 15 mg de cada parte específica das espécies avaliadas e três repetições por parte da planta. O tecido foliar da espécie Glycine max (quantidade de DNA de 2,5 pg/2C; Doleel et al., 1994) foi utilizado como padrão interno de referência nas análises foliares e como padrão externo de referência nas demais análises. As amostras foram trituradas em placa de Petri (mantidas em gelo) contendo 1 mL de tampão gelado. A suspensão nuclear foi então filtrada em um filtro de 30 nm (PARTEC, Muster-Alemanha). Com a finalidade de definir o melhor tampão a ser empregado para a espécie, foram utilizados os tampões LB01 (Doleel et al., 1989) e Marie (Marie e Brown, 1993). Foram adicionados a suspensão 2,5μL de RNase e a coloração foi efetuada com 25 µL de iodeto de propídeo (1 mg mL-1). Para cada amostra foram analisados no mínimo 10 mil núcleos e os histogramas foram obtidos no citómetro de fluxo FacsCalibur (Becton Dickinson) com o programa Cell Quest (Becton, Dickinson and Company, San Jose, CA, USA) e analisados pelos softwares WinMDI 2.8. O tamanho do genoma foi estimado pela seguinte equação: 2C amostra = (Média do pico G1 da amostra / Média do pico G1 do padrão interno de referência) × 2C padrão interno de referência, onde 2C é o conteúdo de DNA em um núcleo holoplóide não replicado e a média do pico G1 é o valor médio de fluorescência emitida pelos núcleos na fase G1 do ciclo celular (Doleel e Bartos, 2005). Os dados foram submetidos à análise de variância e ao teste de Scott-Knott (P<0,05) com o auxílio do programa Sisvar (Ferreira, 2011).
RESULTADOS E DISCUSSÃO
O software GroundEye® possui cerca de 300 características, entretanto foram selecionadas cor e geometria que diferiram das demais em análise comparativa por meio de gráficos que resultaram em faixas de variação calculadas em porcentagem para cada espécie estudada.
As características selecionadas: cor (dominância laranja, luminosidade e dominância preta) e geometria (diâmetro mínimo e diâmetro máximo) foram as que apresentaram maior contraste entre as cultivares nos diferentes estádios de maturação ao utilizar-se o sistema de gráficos do software GroundEye®.
Na avaliação da cor, em relação à dominância laranja (Quadro 2), observou-se que houve distinção entre espécies nos diferentes estádios de maturação da inflorescência, exceto nos estádios um (capítulo fechado) e seis (capítulo aberto e já escurecido). O capítulo fechado possui o mesmo padrão de cor dominância laranja que o capítulo totalmente aberto e já escurecido para as duas espécies. Assim, não é possível distinguir as espécies de sempre-vivas pela dominância laranja, nesses dois estádios. Para a espécie C. elegans o maior índice foi encontrado no estádio cinco, no qual as flores estão totalmente abertas. Esse maior índice ocorreu provavelmente devido a abertura total da inflorescência, sem ocasionar alteração da cor devido a senescência. Para a espécie C. nitida os maiores valores foram encontrados nos estádios quatro e cinco, não havendo diferença significativa entre eles.
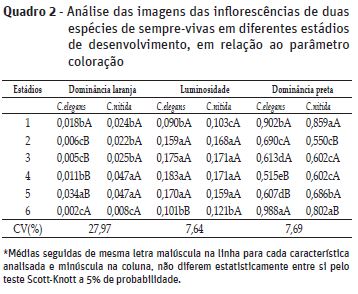
Com relação à característica luminosidade (Quadro 2), a espécie C. elegans não apresentou diferença significativa entre os estádios um e seis, os quais diferiram dos demais estádios. O estádio um não difere do estádio seis devido à coloração escura do último estádio. A espécie C. nitida apresentou diferença significativa entre o estádio um e seis, os quais diferiram dos demais estádios de maturação. No entanto, as médias obtidas foram muito próximas. Não houve diferença significativa nos demais estádios para ambas as espécies, o que evidencia a semelhança da inflorescência quando aberta e antes da alteração de cor. Entre as espécies houve diferença significativa para a característica luminosidade apenas no estádio seis.
Com relação a característica cor dominância preta (Quadro 2), a espécie C. nitida apresentou médias que foram diferenciadas em três grupos: estádios dois, três e quatro, com as menores médias; estádio cinco, com valor intermediário; e o estádio um e seis, com as maiores médias. As maiores médias foram observadas nos estádios um e seis, provavelmente porque no estádio um o capítulo estava fechado e apresentou brácteas com coloração escura, e no estádio seis as inflorescências estavam escuras devido à senescência. Por outro lado, para a espécie C. elegans as médias diferiram entre os estádios, com exceção dos estádios três e cinco, que apresentaram médias iguais. Assim, observou-se um comportamento diferente entre as espécies devido às particularidades no desenvolvimento da inflorescência. Devido a essa variação é possível inferir que a dominância da coloração preta não é um indicativo da variação da cor na distinção das espécies. No entanto, a variação da cor dominância laranja, observada nas duas espécies, demonstrou ser suficiente para a distinção das mesmas.
Dias et al. (2010) utilizaram a análise de imagens para o desenvolvimento de uma ferramenta para padronização de flores, e concluíram que o uso dessa técnica atendeu às necessidades para os padrões de classificação de comercialização de flores no Brasil. A análise computadorizada também se mostrou suficientemente rápida e eficaz reduzindo os custos, o tempo, os danos mecânicos aos materiais estudados, elevando assim, a eficiência do processo e a qualidade do produto oferecido ao consumidor.
Os maiores valores tanto para o diâmetro mínimo quanto para o diâmetro máximo foram observados no estádio cinco para espécie C. elegans (Quadro 3). Não houve diferença entre esse estádio e o estádio quatro para a espécie C. nitida. O diâmetro mínimo e máximo foi crescente à medida que o estádio aumentou e atingiu o valor máximo no estádio cinco. Ocorreu uma queda no estádio seis, conforme esperado, devido a senescência da inflorescência. Para o diâmetro mínimo não houve diferença entre as espécies nos estádios três e quatro e no diâmetro máximo não houve diferença no estádio um, uma vez que o capítulo estava totalmente fechado.
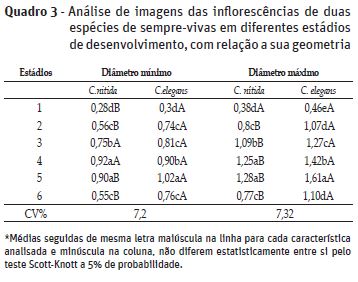
Diante do exposto, o equipamento GroundEye® pode ser utilizado na distinção de espécies de sempre-vivas dependendo dos estádios de desenvolvimento das inflorescências.
Após a análise das inflorescências foi feita a extração das sementes de C. elegans e C. nitida que apresentaram teor de água em torno de 7 e 8% respectivamente, independente do estádio de desenvolvimento da inflorescência, e os valores de germinação e viabilidade dessas sementes encontram-se no Quadro 4.
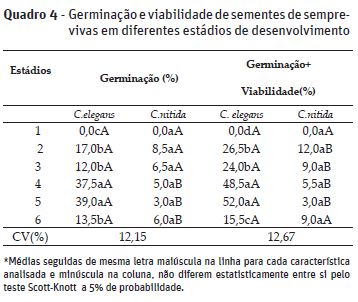
C. elegans apresentou maiores valores de germinação e viabilidade nos estádios quatro (60 a 90% de abertura das inflorescências) e cinco (inflorescências totalmente abertas) (Quadro 4). Para as sementes de C. nitida não houve diferença na germinação e viabilidade entre os estádios de desenvolvimento. A análise de viabilidade pelo teste de tetrazólio indicou dormência nas espécies C. elegans e C. nitida com até 13 e 4%. As demais sementes estavam mortas.
A identificação correta do estádio de desenvolvimento das espécies de C. elegans e C. nitida é fundamental para obtenção de uma maior porcentagem de germinação. Deste modo irá viabilizar tanto a sua regeneração quanto a produção de novas sementes medidas estas fundamentais para conservação da espécie. O equipamento GroundEye® auxilia nessa identificação, indicando o momento ideal para a colheita das inflorescências.
Oliveira et al. (2015) trabalhando com sementes de C. elegans observaram que a germinação variou de acordo com a época e o local de colheita. Esses autores analisaram a época da colheita precoce, antes da produção ou maturação completa das sementes, e verificaram que a colheita precoce pode interferir negativamente na germinação de sementes.
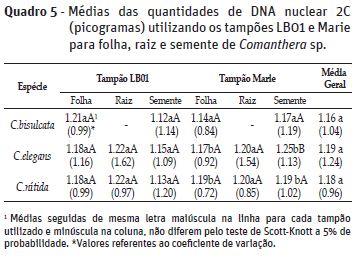
Com relação as análises de citometria de fluxo das espécies C. bisulcata, C. elegans e C. nitida, testou-se os tampões LB01 e Marie com o intuito de estabelecer o tampão adequado para isolamento de núcleos interfásicos. Não foi observada diferença significativa entre os tampões testados (p<0.05). Desta maneira ambos os tampões podem ser utilizados para análises de citometria de fluxo de Comanthera. No entanto, os coeficientes de variação do tampão Marie foram menores para todas as análises, exceto em sementes de C. bisulcata e C. elegans (Quadro 5). Assim, é aconselhável a utilização do tampão Marie para tecidos foliares e radiculares e do tampão LB01 para sementes de Comanthera sp.
A avaliação do uso adequado do tampão a ser utilizado em análises de citometria de fluxo é um fator importante, uma vez que em alguns casos não é possível obter a leitura de núcleos ao utilizar-se um tampão específico.
Visando investigar a viabilidade de utilização de diferentes partes da planta para análises em citometria de fluxo de Comanthera, o DNA nuclear em folhas, raízes e sementes das referidas espécies foi quantificado (Figura 1). A espécie C. bisulcata apresentou quantidade insuficiente de raízes, não sendo possível estimar a quantidade de DNA para este tecido. Não houve diferença significativa (p<0.05) entre os tecidos vegetais avaliados dentro de cada espécie. A única exceção foi a semente de C. elegans ao utilizar-se o tampão Marie (Quadro 5), provavelmente devido ao elevado background durante a leitura dos núcleos interfásicos. Dessa forma, folhas, raízes ou mesmo sementes podem ser utilizadas para análises em citometria de fluxo das espécies de Comanthera avaliadas.
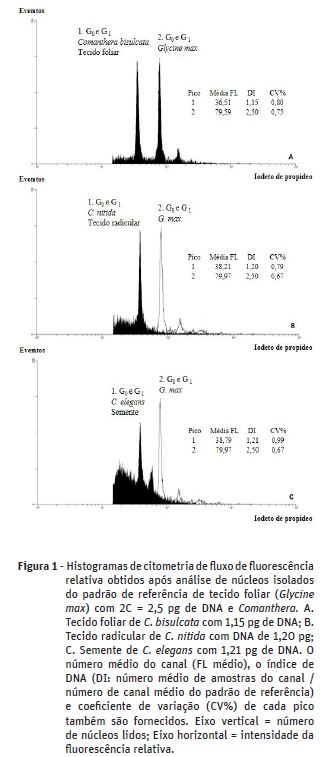
A possibilidade de estimativa do conteúdo de DNA nuclear a partir de diferentes partes da planta de Comanthera sp. no presente trabalho representa um resultado vantajoso, uma vez que nem sempre se tem disponível uma determinada parte da planta para análise, além de ser um indicativo de que as espécies estudadas não possuem metabólitos secundários, já que apresentam o mesmo tamanho do genoma em diferentes tecidos.
Todas as partes das plantas avaliadas em citometria de fluxo apresentaram médias de coeficientes de variação inferiores a 1.63%, o que evidencia a confiabilidade dos resultados. Em citometria de fluxo, a ocorrência de variação é normalmente expressa pelo coeficiente de variação (Doleel et al., 1989), sendo valores entre 1%-2% considerados de alta qualidade e, próximos a 3%, considerados como rotina (Marie e Brown, 1993). Entretanto, quando se trata de quantificações que incluem estimativas do tamanho do genoma ou mesmo para espécies ricas em metabólitos secundários, coeficientes de variação menores que 5% são aceitáveis (Doleel e Barto, 2005).
Não houve diferenças significativas entre as quantidades de DNA das três espécies avaliadas dentro de cada tecido, com exceção do tecido foliar e de semente, ao se utilizar o tampão Marie. Os valores médios resultantes das análises de folha, raiz e semente de C. bisulcata, C. elegans e C. nitida, corresponderam a 1.16, 1.19 e 1.18 pg respetivamente (Quadro 5). A estimativa do conteúdo de DNA nuclear para espécies do género Comanthera é de grande importância de modo a obter a caracterização genômica, ainda inexistente, para tais espécies constituindo informação básica para estudos posteriores.
CONCLUSÕES
O sistema de análise de imagens (GroundEye®) tem potencial para diferenciar espécies e estádios de desenvolvimento de inflorescências de sempre-viva.
A espécie Comanthera elegans apresentou maiores valores de germinação e viabilidade nos estádios quatro (60 a 90% de abertura das inflorescências) e cinco (inflorescências totalmente abertas).
Folhas, raízes e sementes podem ser utilizadas para quantificação de DNA nuclear em citometria de fluxo para as espécies de Comanthera sp.
Foi possível estimar o conteúdo de DNA nuclear com grande precisão para C. bisulcata, C. elegans e C. nitida, no entanto as espécies apresentam tamanhos de genoma muito similares não sendo possível a distinção entre essas espécies por citometria de fluxo.
Recomenda-se a utilização do tampão Marie para tecidos foliares e radiculares, e do tampão LB01 para sementes de Comanthera sp.
Referências bibliográficas
Albuquerque, S.M.M.; Brito, A.L.; Lima, A.P.P.S.; Alvim, B.M.F. & Santana, J.R.F. (2016) - In vitro establishment of Comanthera curralensis, sempre viva native of Chapada da Diamantina-Bahia. Ciência Rural, vol. 46, n. 6, p. 991-995. http://dx.doi.org/10.1590/0103-8478cr20131091 [ Links ]
Andrade, D.B.; Oliveira, A.S.; Pinto, C.A.G.; Pires, R.M.O.; Oliveira, A.S.O.; Silva, M.A. & Carvalho, M.L.M. (2016) - Detection of green seeds in soybean lots by the seed analysis system (SAS). International Journal of Current Research, vol. 8, p. 26462-26465. [ Links ]
Brasil (2009) - Regras para Análises de Sementes. Ministério da Agricultura, Pecuária e Abastecimento. Secretaria de Defesa Agropecuária. Brasília, DF: MAPA/ACS, p.395.
Dias, G.; Lino, A.C.L.; Sanches, J.; Lima, F.A.B. & Nascimento, T.S. (2010) - O uso de imagens digitais na classificação de flores de corte. Revista Brasileira de Horticultura Ornamental, vol. 16, n. 2, p. 123-126. [ Links ]
Doleel, J. & Barto, J. (2005) - Plant DNA flow cytometry and estimation of nuclear genome size. Annals of Botany, vol. 95, n. 1, p. 99-110. https://doi.org/10.1093/aob/mci005 [ Links ]
Doleel, J.; Doleelova, M. & Novák, F. J. (1994) - Flow cytometric estimation of nuclear DNA amount in diploid bananas (Musa acuminata and M. balbisiana). Biologia Plantarum vol. 36, p. 351-357. https://doi.org/10.1007/BF02920930 [ Links ]
Doleel, J.; Binarová, P. & Lucretti, S. (1989) - Analysis of nuclear DNA content in plants cells by flow cytometry. Biologia Plantarum, vol. 31, n. 2, p.113-120. https://doi.org/10.1007/BF02907241 [ Links ]
Echternacht, L.; Santo, P.T. & Dubuisson, J.Y. (2015) - Taxonomic study of Comanthera subg. Thysanocephalus (Eriocaulaceae). Systematic Botany, vol. 40, n. 1, p. 136-150. https://doi.org/10.1600/036364415X686431 [ Links ]
Ferreira, D.F. (2011) - Sisvar: A computer statistical analysis system. Ciência e Agrotecnologia, vol. 35, n. 6, p. 1039-1042. http://dx.doi.org/10.1590/S1413-70542011000600001 [ Links ]
Giulietti, A.M.; Hensold, N.; Parra, L.R.; Andrade, M.J.G.; Van Den Berg, C.&e Harley, R. M. (2012) - The synonymization of Philodice with Syngonanthus (Eriocaulaceae). Phytotaxa, vol. 60, p. 50-56. http://dx.doi.org/10.11646/phytotaxa.60.1.7
Knight, C.A. & Beaulieu, J.M. (2008) - Genome size scaling through phenotype space. Annals of Botany. vol. 101, n. 6, p. 759-766. https://doi.org/10.1093/aob/mcm321 [ Links ]
Kolar, F.; Stech, M.; Travnicek, P.; Rauchova, J.; Urfus, T.; Vit, P.; Kubeesova, M. & Suda, J. (2009) - Towards resolving the Knautia arvensis agg. (Dipsacaceae) puzzle: primary and secondary contact zones and ploidy segregation at landscape and microgeographic scales. Annals of Botany, vol. 103, n. 6, p. 963-974. https://doi.org/10.1093/aob/mcp016 [ Links ]
Leal, B.B.S.; Tannure, M.P.; Santos, F.R.; Lovato, M.B. & Ribeiro, R.A. (2014) - Isolation and characterization of microsatellite markers for the endangered Comanthera elegans (Eriocaulaceae) and cross-species amplification within the family. Biochemical Systematics and Ecology, vol. 55, p. 305-309. [ Links ]
Lima-Brito, A.; Albuquerque, M.M.S.; Resende, S.V.; Carneiro, C.E. & Santana, J.R. (2016) - In vitro hardening in different environment and acclimatization of microplants of Comanthera mucugensis Giul. Subsp. mucugensis. Revista Ciência Agronômica, vol. 47, n. 1, p. 152-161. http://dx.doi.org/10.5935/1806-6690.20160018 [ Links ]
Marie, D. & Brown, S.C. (1993) - A cytometric exercise in plant DNA histograms, with 2C values for 70 species. Biology of the Cell, vol.79, n. 1-2, p. 41-51. https://doi.org/10.1016/0248-4900(93)90113-S [ Links ]
Oliveira, A.S.; Carvalho, M.L.M.; Bárbara, C.N.V.; Almeida, T.T. & Nery, M.C. (2016) - Maturação, temperatura e quebra de dormência na germinação de sementes de sempre-vivas. Ornamental Horticulture, vol. 22, p. 186-195. [ Links ]
Oliveira, M.N.S.; Dias, B.A.S.; Andrade, G.C.; Tanaka, M.K.; Ávila, R.G. & Silva, L.C. (2015) - Harvest times of Comanthera elegans, a worldwide traded Brazilian species of everlasting flower implications on seed production, germination, and on species management. Brazilian Journal of Botany, vol. 38, n. 4, p. 795-808. https://doi.org/10.1007/s40415-015-0179. [ Links ]
Pêgo, R.G.; Paiva, O.P.D. & Paiva, R. (2013) - Micropropagação de Syngonanthus elegantulus. Ciência e agrotecnologia, vol. 37, n. 1, p. 32-39. http://dx.doi.org/10.1590/S1413-70542013000100004 [ Links ]
Pereira, L.A.; Carvalho, M.L.M.; Nery, M.C. & Toorop, P.E. (2014) - Embryo morphology indicates physiological maturity better than seed mass in Syngonanthus elegans (Eriocaulaceae). Seed Science and Technology, vol. 42, n. 2, p. 161-170. https://doi.org/10.15258/sst.2014.42.2.05 [ Links ]
Agradecimentos
À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES), pelo apoio financeiro e pela concessão de bolsa. Aos revisores que com as suas revisões contribuíram para a qualidade do manuscrito apresentado.
Recebido/received: 2018/05.30
Recebido em versão revista/received in revised form: 2018.08.16
Aceite/accepted: 2018.08.19














