Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Corrosão e Protecção de Materiais
versão impressa ISSN 0870-1164versão On-line ISSN 2182-6587
Corros. Prot. Mater. vol.35 no.2 Lisboa dez. 2016
https://doi.org/10.19228/j.cpm.2016.35.06
ARTIGOS
Resistência à corrosão em meio de diesel e biodiesel do aço carbono revestido com cobre
Corrosion resistance in diesel and biodiesel for carbon steel copper coated
Julian Johann1 , Danielle Silva1 , Maico Cunha1 , Mayara Soares1 , Paulo Rodrigues1 e Everson Banczek1,*
1Universidade Estadual do Centro-Oeste - UNICENTRO, Departamento de Química / Centro de Ciências Exatas e de Tecnologia,Campus do CEDETEG, 85040-080, Guarapuava - PR, Brazil.E-mail: jullyjohann@hotmail.com, danielle.dcs@hotmail.com, maico_tc@yahoo.com.br, mayarasoares_842@hotmail.com, prprodrigues@gmail.com . * A quem a correspondência deve ser dirigida. E-mail: edopradobanczek@yahoo.com.br
RESUMO
A corrosão metálica é dependente do meio ao qual o material está em contato. Em eletrólitos com condutividade elevada a corrosão é facilmente quantificada. Entretanto, em combustíveis, a determinação da corrosão é dificultada, pois a condutividade é baixa. Normas como a ABNT 14359 e ASTM D130 estabelecem métodos de determinação da corrosão em combustíveis, porém, a avaliação é qualitativa. Neste contexto, a determinação da corrosão em combustíveis é um desafio. Neste estudo, determinou-se a corrosão do aço carbono (SAE 1045) revestido com cobre pelo método indireto. Os metais foram imersos em biodiesel B100 ou diesel S10 e posteriormente, em NaCl 0,5 mol L-1 . Ensaios de potencial de circuito aberto, impedância eletroquímica e polarização anódica, indicaram que a metodologia empregada foi eficiente para a avaliação da corrosão.
Palavras-chave: Biocombusvel, Ensaios Eletroquímicos, Aço Carbono (SAE 1045)
ABSTRACT
Metal corrosion is dependent upon the environment to which the material is in contact. In electrolytes with high conductivity corrosion is easily quantified. However, in fuel, corrosion determination is complicated, because the conductivity is low. Standards like ABNT 14359 and ASTM D130 establish fuel corrosion determining methods, however, the evaluation is qualitative. In this context, the fuel corrosion determination is a challenge. In this study, carbon steel (SAE 1045) copper coated corrosion was determined using the indirect method. The metals were immersed in B100 biodiesel or diesel S10 and thereafter, NaCl 0.5 mol L-1 . Open circuit otential, electrochemical impedance and anodic polarization, indicated that the method was effective for corrosion evaluation.
Key-words: Biofuel, Electrochemical Measures, Carbon Steel (SAE 1045)
INTRODUÇÃO
O biodiesel é um biocombustível que possui algumas vantagens sobre o diesel convencional, entretanto, é mais corrosivo [1] . A presença de água e de ácidos graxos no combustível pode culminar no processo de hidrólise, acarretando no aumento dos íons hidrogênio em solução que provocam a diminuição do pH do meio, aumentando a corrosividade [2-5].
No biodiesel é possível encontrar impurezas no meio como resíduo de catalisador e excesso de álcool que não reagiram durante a reação de obtenção do biocombustível, glicerina residual livre, sais de ácidos graxos, mono, di e triglicerídeos. Tais resíduos são responsáveis por acentuar os processos corrosivos [6,7]. Comparado com o diesel, biodiesel tem uma maior tendência para absorver água porque os ésteres têm propriedades higroscópicas [5].
O cobre e suas ligas são os metais mais afetados por biodiesel, especialmente quando expostos à luz [8]. No entanto, dependendo das condições de armazenamento, outros metais podem corroer quando são colocados em contato prolongado com o combustível [9].
A determinação da corrosão em meio de combustíveis pode ser realizada por meio de técnicas eletroquímicas, porém, para que este método seja aplicado são necessárias condutividades significativas [1, 10,].
Os testes de corrosividade exigidos pela ASTM D130 [11] e pela ISO 2160 [12] tem seu foco em combustíveis derivados de petróleo, não sendo adequados para se avaliar a corrosão de biocombustíveis, como é o caso do biodiesel.
Quando um ensaio eletroquímico deve ser aplicado é necessário o uso de eletrólitos suporte, os quais devem ser adicionados a fim de aumentar a condutividade do combustível [1].
Alguns estudos apresentam ensaios de corrosão realizados com aço carbono em bioetanol [13] e ferro em solução metanólica [14] . Os autores observaram que o potencial de circuito aberto em aço carbono respondeu de forma diferente à remoção de oxigênio dependendo do eletrólito adicionado [15].
Um procedimento alternativo de avaliar a corrosão de metais em combustíveis é a utilização de microeléctrodos [16, 17]. Esta técnica tem sido proposta para executar a polarização de microeletrodos de aço de carbono em etanol, sem a adição de qualquer eletrólito de suporte. Espectroscopia de impedância eletroquímica (EIE) tem sido proposta para avaliar a corrosividade do sistema de água-biodiesel [5, 18], mas a eficácia está em discussão.
A determinação da corrosão em combustíveis pode ser determinada de maneira indireta por imersão da amostra metálica no combustível e, posterior imersão em um eletrólito forte e aplicações de ensaios eletroquímicos de espectroscopia de impedância eletroquímica e polarização potenciodinâmica [19] . O presente trabalho propõe a aplicação de um método para avaliação da corrosão do aço carbono SAE 1045 em diesel comercial S10 B5 e biodiesel de soja B100 revestido com cobre eletrodepositado.
METODOLOGIAS EXPERIMENTAIS
2.1. Amostras de biodiesel e diesel
O diesel empregado foi o S10 B5, comprado em um posto de combustíveis local. O biodiesel utilizado foi o B100 fornecido pela companhia Ipiranga®.
2.2. Material metálico
O substrato metálico empregado foi o aço carbono (SAE 1045), previamente lixado com lixas de SiC com #220, #400, #600, #1200 e polido com pasta de diamante de 9µm, 6µm, 3µm, 1µm e ¼ µm. Tal substrato, depois do lixamento, foi utilizado como eletrodo para a eletrodeposição de cobre.
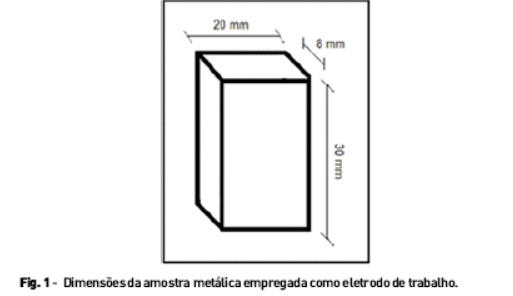
Na Figura 1 está a representação do formato das amostras utilizadas.
2.3. Eletrodeposição do revestimento de cobre
As medidas eletroquímicas foram realizadas em uma célula eletroquímica de três eletrodos (trabalho, referência e contra eletrodo) conectados a um potenciostato/galvanostato modelo VersaStat4 da Princeton Applied Research com agitação realizada por um agitador magnético. O eletrodo de trabalho foi colocado em contato com a solução por um orifício lateral vedado com um anel O'ring, sendo que a área do eletrodo que ficou em contato com a solução foi de 113,1 mm².
Para se obter as soluções com íons Cu2+ , estáveis em meio alcalino, utilizou-se um composto orgânico complexante para o íon Cu2+ (ou cúprico), o etilenodiamina.
Para o preparo das soluções de trabalho, empregou-se uma solução estoque de Na2SO 1 mol L-1 e sob agitação, adicionou-se a massa de CuSO4 .5H2O necessária para que a concentração final de Cu2+ fosse igual a 1x10 mol L-1 . A partir de uma alíquota de 100 mL da solução de Na2SO4 /CuSO4 adicionou-se o volume adequado do composto orgânico empregado como agente complexante (etilenodiamina), de modo que relação molar Cu2+ : complexante fosse da ordem de 1:5. Em sequência o pH da solução foi ajustado para 10 com o auxílio de uma solução de NaOH 2 mol L-1 . O eletrodo de sulfato mercuroso foi utilizado como referencial de potencial para as eletrodeposições.
2.4. Microscopia eletrônica de varredura e espectroscopia de energia dispersiva
A caracterização morfológica da superfície foi feita por microscopia eletrônica de varredura (MEV) em um equipamento Tescan® Vega 3, com aumento de 1000 vezes. No mesmo equipamento foram realizadas análises da composição da superfície por espectroscopia de energia dispersiva (EDS). As medidas de espessura foram realizadas da seção transversal de amostras de aço carbono revestido com cobre.
2.5. Caracterização eletroquímica
A caracterização eletroquímica foi realizada pelas técnicas de potencial de circuito aberto (ECA), espectroscopia de impedância eletroquímica (EIE) e polarização potenciodinâmica anódica (PA). A velocidade de varredura da polarização potenciodinâmica foi de 1 mV/s. O aparelho utilizado foi um potenciostato Gamry® PC4-300, associado a um analisador de frequência EIS 300.
A célula eletroquímica utilizada continha três eletrodos, sendo o contra eletrodo uma placa de platina de grande área, o eletrodo de referência de prata cloreto de prata (Ag/AgCl) com KCl saturado e o eletrodo de trabalho a amostra de aço carbono com área de 0,68 cm2 .
O meio eletrolítico foi NaCl 0,5 mol L-1 . Antes dos ensaios eletroquímicos em meio de NaCl, as amostras foram imersas ao diesel B5 S10 e ao biodiesel B100 durante dois meses à temperatura ambiente.
RESULTADOS E DISCUSSÕES
3.1. Microscopia eletrônica de varredura
As amostras de aço carbono SAE 1045 não revestidas e revestidas com cobre foram analisadas por MEV e as micrografias estão apresentadas na Figura 2.

A partir da análise observa-se que a morfologia da superfície do aço carbono foi alterada pela deposição do revestimento de cobre. A superfície ficou mais irregular e podem ser observados alguns defeitos escuros no revestimento de cobre devido a formação de óxido cúprico como consequência da alteração do pH na interface metal/solução.
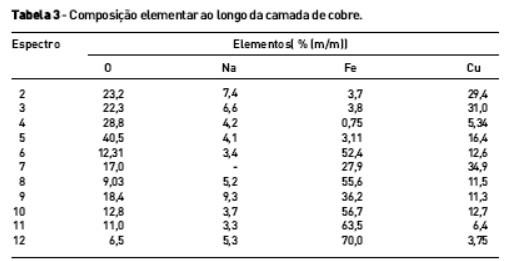
Na Tabela 1 está a composição elementar da superfície das amostras analisadas. Os resultados evidenciam a presença dos principais elementos constituintes do aço carbono com o maior percentual para o elemento ferro.
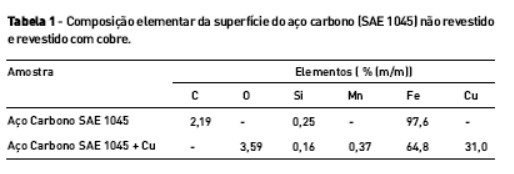
O revestimento de cobre altera a composição da superfície do aço carbono e promove a diminuição da quantidade de ferro determinado, pois a presença da camada eletrodepositada bloqueia a detecção do ferro que está na superfície do metal base. Adicionalmente, foi possível observar a presença de 31,0 % de cobre na superfície da amostra revestida. Este resultado comprova que o processo de eletrodeposição foi efetivo. A presença do elemento oxigênio pode estar relacionada com a formação do óxido de cobre na superfície da camada eletrodepositada.
Na literatura [20] a eletrodeposição do cobre foi investigada sobre uma liga de alumínio, empregando um banho de deposição na ausência de cianeto. Neste estudo observou-se que com a elevação da densidade de corrente de electrodeposição, o desprendimento de hidrogênio torna-se mais significativo e, desta forma, acarreta na diminuição da eficiência de electrodeposição do cobre. Com a ocorrência da reação de desprendimento de hidrogênio acontece a formação de óxido cúprico como consequência da alteração do pH na interface metal/solução. Tal óxido escurece o depósito, sendo essa alteração da coloração possível de ser observada visualmente.
A dissolução do revestimento de cobre em meio dos combustíveis foi avaliada após a imersão por 2 meses e os resultados são apresentados nas micrografias da Figura 3 e pela quantificação elementar da superfície que está apresentada na Tabela 2.

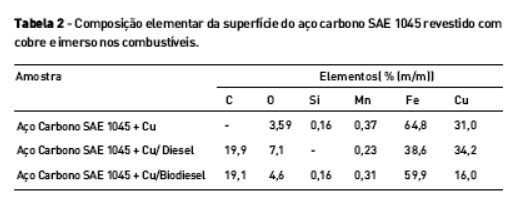
Os resultados indicam que houve um aumento na quantidade de oxigênio quando a amostra foi imersa nos combustíveis e, pode ser atribuída a formação de óxido de cobre e ferro na superfície do revestimento devido as características corrosivas do meio. A presença de carbono na superfície da amostra está relacionada à adsorção de moléculas dos combustíveis na superfície da camada de cobre.
Uma dissolução preferencial pode ser determinada a partir dos resultados da Tabela 2 quando se compara a variação na composição de ferro e cobre. Uma diminuição na quantidade de ferro foi observada quando as amostras foram imersas em diesel indicando que neste meio o processo corrosivo é determinado pela dissolução de ferro. Comportamento diferente foi observado para as amostras imersas em biodiesel para as quais foi determinada uma dissolução maior de cobre, sugerindo que o processo corrosivo é determinado pela dissolução de cobre.
As micrografias confirmam os resultados da quantificação por EDS, pois a amostra imersa em diesel (Figura 3A) apresenta uma superfície mais irregular característica da remoção seletiva de ferro da matriz de aço.
3.2. Determinação da espessura do revestimento de cobre
A espessura da camada de cobre foi determinada por microscopia eletrônica de varredura e a micrografia da Figura 4 apresenta os resultados. Um valor de espessura de 7,37 µm foi medido, valor este muito próximo ao encontrado na literatura [21]. A composição elementar ao longo do revestimento foi determinada e os resultados são apresentados na micrografia da Figura 5 e Tabela 3, com os valores médios obtidos.

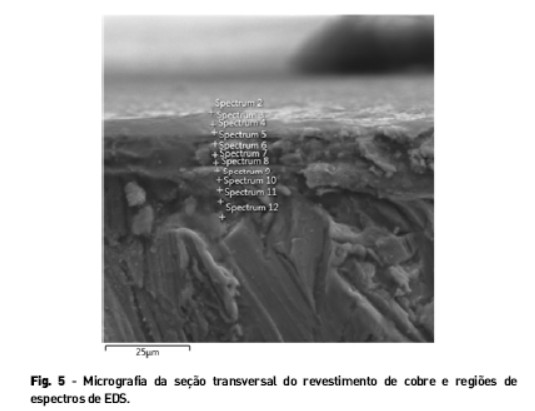
A determinação da composição do revestimento do cobre ao longo de sua espessura indica que na superfície do revestimento há uma maior quantidade de cobre quando comparada à quantidade de ferro. Este resultado está de acordo com o esperado, pois o efeito de difusão de ferro pelo revestimento, durante a eletrodeposição, faz com que a quantidade de ferro na superfície seja menor (Figura 6). Uma diminuição da quantidade de cobre pode ser observada ao longo do revestimento no sentido da sua superfície para o substrato de aço e pode ser explicada pelo processo difusivo do cobre e do ferro (Figura 6).
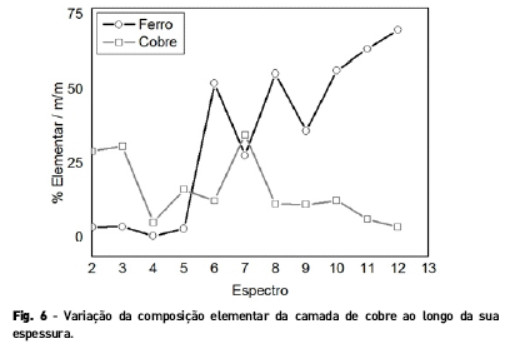
A difusão do cobre e do ferro se caracteriza pelo gradiente de concentração desses metais ao longo do depósito eletroquímico. Sendo que, mais próximo ao substrato metálico do aço carbono a concentração do ferro é muito maior ao passo que, com o distanciamento desta região para a superfície do depósito a concentração do ferro vai diminuindo e aumentando a concentração do cobre que foi eletrodepositado [21].
3.3. Ensaios de corrosão
3.3.1. Potencial de circuito aberto
Na Figura 7 são apresentados os resultados de potencial de circuito para as amostras imersas em diesel e biodiesel.
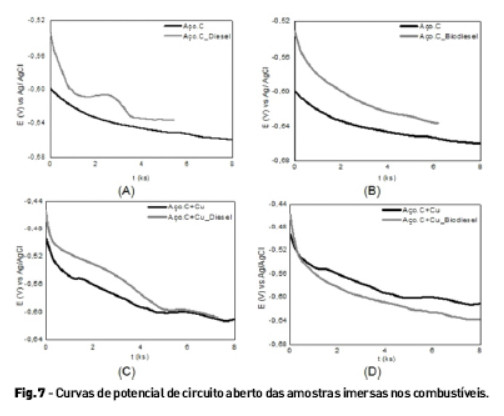
A partir destas medidas foi possível observar que, independente do meio, o potencial apresentou uma faixa de variação muito semelhante para todas as amostras.
Adicionalmente, observou-se que o comportamento das amostras revestidas e não revestidas com cobre, quando imersas nos combustíveis não foram semelhantes, pois o revestimento de cobre altera o potencial de circuito aberto do metal base revestido quando imerso em biodiesel, deslocando-o para valores mais negativos. Tal resultado pode estar relacionado à maior solubilidade do cobre em meio de biodiesel e com a corrosividade deste biocombustível que é maior que do diesel [2, 22-23]. O deslocamento para valores mais negativos indica uma menor resistência à corrosão.
Os resultados de potencial de circuito aberto estão de acordo com a literatura [24], a partir dos quais, amostras de microemulsão de B100 apresentaram resultados semelhantes aos deste trabalho a partir de medidas de potencial de circuito aberto.
Silva [25] realizou as medidas de potencial de circuito aberto para o biodiesel B100 de soja e o óleo diesel, bem como para biodiesel com diesel (B5 e B20). A autora observou que os valores dos perfis de variação do potencial de circuito aberto foram similares para todas as condições estudadas. Com o aço carbono imerso tanto no biodiesel como no diesel, os valores de potencial de circuito aberto se tornaram cada vez menos positivos com o passar do tempo de imersão. Resultados estes condizentes com os obtidos neste estudo.
3.3.2. Espectroscopia de impedância eletroquímica
Na Figura 8 estão os diagramas de espectroscopia de impedância eletroquímica. Os diagramas de Nyquist apresentam apenas um arco capacitivo para todos os sistemas estudados. Maiores valores de impedância foram determinados para as amostras não imersas nos combustíveis sugerindo uma menor resistência à corrosão. As amostras imersas em diesel apresentaram maiores valores de impedância, quando comparados aos valores de impedância determinados para as amostras imersas em biodiesel, sugerindo que este último é mais corrosivo.
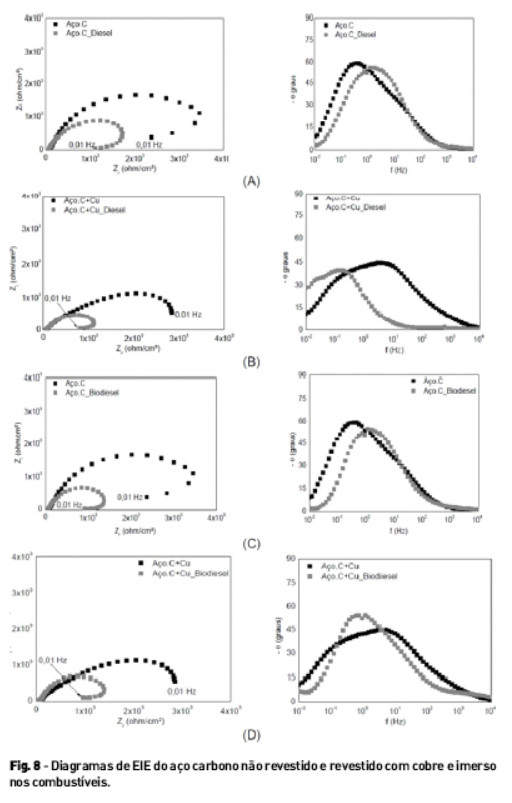
Silveira [26] obteve resultados semelhantes a estes, realizando espectroscopias de impedância de diesel, biodiesel e suas blendas. O autor observou que o módulo de impedância tende a aumentar com a diminuição da concentração de biodiesel na amostra, confirmando que o biodiesel se mostrou mais corrosivo do que o diesel também neste estudo.
Os diagramas de ângulo de fase de Bode indicam a presença de apenas uma constante de tempo para as amostras não revestidas com cobre, sugerindo que apenas um processo está acontecendo na superfície e pode ser atribuída aos processos de transferência de carga. Um deslocamento desta constante de tempo para maiores frequências foi observado para as amostras não revestidas com cobre, indicando uma aceleração do processo corrosivo. Os menores ângulos de fase medidos também indicam que houve uma menor resistência à corrosão.
Para as amostras revestidas com cobre e não imersas nos combustíveis indicam a presença de duas constantes de tempo associadas a dois processos. A primeira constante em 10 Hz pode ser atribuída à presença do cobre na superfície. A segunda constante em 0,1 Hz pode ser atribuída aos processos de transferência de carga.
A imersão em diesel promove uma diminuição dos valores de ângulo de fase da constante de tempo de transferência de carga da amostra revestida, indicando uma diminuição da resistência à corrosão promovida pelo diesel.
A imersão nos combustíveis modifica a resposta de impedância, pois o diagrama de Bode apresentou apenas uma constante de tempo sugerindo apenas um processo, que pode estar relacionado com a dissolução do revestimento de cobre.
Queiroz e Costa [27], que estudaram o comportamento corrosivo de um aço galvanizado por espectroscopia de impedância eletroquímica, verificaram comportamento semelhante a este em seu estudo. A partir dos diagramas de Bode, os autores observaram um grande aumento no módulo de impedância em quase toda a faixa de frequências, sendo difícil identificar uma segunda constante de tempo no diagrama. Segundo os autores, tais resultados indicam a remoção de uma fase mais externa do revestimento da amostra metálica. Já a fase mais interna, do aço, apresentou maiores valores de impedância, sugerindo uma maior resistência ao ataque pela solução.
3.3.3. Polarização potenciodinâmica anódica
As curvas de polarização potenciodinâmicas anódicas estão apresentadas nas Figuras 9 e 10.
Os resultados de polarização potenciodinâmica anódica indicaram um comportamento corrosivo distinto das amostras em função do combustível utilizado para a imersão.
É possível observar que o aço carbono imerso em biodiesel ou diesel apresentou maior resistência à corrosão quando comparado ao material não imerso, pois menores densidades de corrente foram medidas. Este comportamento pode ser associado à formação de um produto de corrosão que protegeu o metal base.
A resposta de polarização, para as amostras revestidas com cobre, indicaram uma menor resistência à corrosão deste material, pois maiores densidades de corrente foram medidas, quando comparadas com aquelas do material não imerso nos combustíveis.
Matos [19] observou um comportamento semelhante para o aço carbono SAE 1010 imerso em biodiesel B100, diesel S10 e biodiesel mixer. Nestes casos o comportamento corrosivo dos combustíveis foi alterado devido a formação de um biofilme na superfície do substrato metálico. A autora também observou que a polarização da amostra de aço carbono imersa em diesel S10 teve comportamento semelhante a mesma amostra sem imersão, sugerindo que o diesel S10 não alterou significativamente a resposta à polarização. A amostra imersa em biodiesel apresentou um pequeno deslocamento para potenciais mais positivos, além de uma densidade de corrente maior. A amostra imersa no biodiesel teve sua superfície alterada, resultando em uma pequena variação nos valores de densidade de corrente, confirmando que a geração do filme que bloqueia parcialmente a superfície do substrato metálico, não sendo possível obter resultados de polarização com diferenças significativas entre os substratos imersos e não imersos no combustível.
CONCLUSÕES
Os resultados demonstraram que a aplicação de técnica de medida da corrosão de forma indireta se mostrou eficiente para a caracterização dos diferentes substratos metálicos imersos nos combustíveis, pois diferenças significativas nos valores de impedância e densidades de corrente foram medidos. De uma maneira geral, as amostras não imersas nos combustíveis apresentaram maiores valores de impedância e menores densidades de corrente e estes resultados indicam que, nestas condições há uma maior resistência à corrosão do metal base.
A comparação entre o comportamento corrosivo de diesel e biodiesel observou-se que as amostras imersas em diesel apresentaram maiores valores de impedância, quando comparados aos valores de impedância determinados para as amostras imersas em biodiesel, sugerindo que este último é mais corrosivo. Este resultado está de acordo com o que era esperado, pois o biodiesel possui características higroscópicas e instabilidade oxidativa que o tornam mais agressivo.
O revestimento das amostras com cobre é uma alternativa para proteção do aço carbono SAE 1045 imerso em combustíveis, pois as amostras eletrodepositadas apresentaram maiores densidades de corrente na polarização indicando uma menor resistência à corrosão. Este comportamento pode ser atribuído a um efeito de eletrodo de sacrifício promovido pelo cobre que se oxidou em detrimento da proteção do aço carbono. Estes resultados estão apoiados pelas medidas de PCA.
AGRADECIMENTOS
Os autores agradecem ao CNPq pela concessão da Bolsa de Produtividade em Desenvolvimento Tecnológico e Extensão Inovadora
REFERÊNCIAS
[1] J. A. Calderón, L. M. Baena and J. Lenis, Cien.Tecn. Fut., 5, 85-86 (2014). [ Links ]
[2] I. Aquino (Avaliação da corrosividade do biodiesel por técnicas gravimétricas e eletroquímicas), Tese de Doutoramento, Escola Politécnica da Universidade de São Paulo. Departamento de Engenharia Química, São Paulo, Brazil (2012). [ Links ]
[3] S. Jain and M. P. Sharma, Fuel, 90, 2045-2050, (2011). [ Links ]
[4] M. A. Fazal, A. S. M. A. Haseeb and H. H. Masjuki, Fuel Process.Technol., 9, 1308-1315 (2010). [ Links ]
[5] J. Kaminski and K. J. Kurzydtowski, J. Corros. Meas., 6, B35-B39 (2008). [ Links ]
[6] C. Faccio, Ciências e Tecnologia de Alimentos, 24, 178-182 (2005). [ Links ]
[7] A. S. M. A. Haseeb, H. H. Masjuki, L. J. Ann and M. A. Fazal, Fuel Process. Technol., 91, 329334 (2010). [ Links ]
[8] I. P. Aquino, R. P. B. Hernández, D. L. Chicoma, H. P. F. Pinto and I. V. Aoki, Fuel, 102, 795-807 (2012). [ Links ]
[9] S. Kaul, R. C. Saxena, A. Kumar, M. S. Negi, A. K. Bhatnagar, H. B. Goyal and A. K. Gupta, Fuel Process. Technol., 88, 303-307 (2007). [ Links ]
[10] A. L. Gallina (Uma alternativa sustentável para a produção de biodiesel: Cyperus esculentus), Dissertação de Mestrado em Bioenergia, Universidade Estadual do Centro-Oeste, Guarapuava, Brazil (2011). [ Links ]
[11] ASTM D 13: 2010. (Standard Test Method for Corrosiveness to Cooper from Petroleum Products by Copper Strip Test), ASTM (2010). [ Links ]
[12] ISO 2160: 1998. (Petroleum products, corrosiveness to copper, copper strip test), ISO (1998). [ Links ]
[13] X. Lou, D. Yang and P. M. Singha, J. Electrochem. Soc., 157, C86-C94 (2010). [ Links ]
[14] C. Brossia, E. Gileadi and R. Kelly, Corros. Sci., 37, 1455-1471 (1995). [ Links ]
[15] N. Sridhar, K. Price, J. Buckingham and J. Dante, Corrosion, 62, 687-702 (2006). [ Links ]
[16] F. Gui, and N. Sridhar, Corrosion, 66, 045005-1_045005-8 (2010). [ Links ]
[17] F. Gui, N. Sridhar and J. Beavers, Corrosion, 66, 125001-1_125001-12 (2010). [ Links ]
[18] L. Díaz-Ballote, J. López-Sansores, L. Maldonado-López and L. J Garfias-Mesias, Electrochem. Commun.,11, 41-44 (2009). [ Links ]
[19] L. A. C. Matos (Estudo da corrosão de ligas ferrosas em diesel e biodiesel), Dissertação de Mestrado em Bioenergia, Programa de Pós-Graduação em Bioenergia, Universidade Estadual do Centro-Oeste, Guarapuava, Brazil (2013). [ Links ]
[20] M. M. Oizume, C. A. C. Souza, J. L. P. Siqueira, A. K. Melle and I. A. Carlos (Estudo voltamétrico da eletrodeposição de um deposito de cobre sobre uma liga de alumínio a partir de um banho não cianetado) in Proceedings of 18º CBECiMat - Congresso Brasileiro de Engenharia e Ciência dos Materiais, Porto de Galinhas, Brazil (2008). [ Links ]
[21] M. M. P. Silva (Efeito de surfactantes aniônicos e catiônicos no comportamento eletroquímico de interfaces metal / soluções aquosas de cloreto de sódio), Tese de Doutoramento, Universidade de São Paulo, São Paulo, Brazil (2002). [ Links ]
[22] A. R. P. Ambrozin, S. E. Kuri and M. R. Monteiro, Química Nova, 32, 1910 - 1916 (2009). [ Links ]
[23] B. E. S Arenas (Avaliação da corrosividade do biodiesel para diferentes metais empregando microeletrodos clássicos e arranjos de microelétrodos), Dissertação de Mestrado, Escola Politécnica da Universidade de São Paulo, São Paulo, Brazil (2014). [ Links ]
[24] F. B. VIANA (Avaliação da corrosividade do biodiesel e misturas em aço por espectroscopia de impedância eletroquímica), Dissertação de Mestrado em Química, Universidade Federal do Maranhão, Maranhão, Brazil (2013). [ Links ]
[25] Y. P. Silva (Estudo da estabilidade oxidativa de biodiesel empregando técnicas eletroquímicas e efeito das condições e tempo de estocagem em aço carbono), Dissertação de Mestrado, Universidade Federal do Rio Grande do Sul, Porto Alegre, Brazil (2009). [ Links ]
[26] L. G. D. Silveira (Aplicação de espectroscopia de impedância no estudo de blendas de biodiesel/diesel), Dissertação de Mestrado, Universidade Estadual de Maringá, Maringá, Brazil (2010). [ Links ]
[27] F. M. Queiroz and I. Costa (Avaliação do comportamento de corrosão de um aço "Galvannealed" comercial por espectroscopia de impedância eletroquímica) in Proceedings of 22º CONBRASCORR - Congresso Brasileiro de Corrosão, Salvador, Brazil (2002). [ Links ]














