Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Corrosão e Protecção de Materiais
versão impressa ISSN 0870-1164
Corros. Prot. Mater. vol.32 no.4 Lisboa dez. 2013
ARTIGO
Efeito de biocidas na corrosão induzida microbiologicamente do aço duplex em água de produção de petróleo
Effect of biocides on the microbiologically induced corrosion of duplex stainless steel in oil produced water
L. Araújo(1) (*), L. Carvalho (1), L. Reznik (1), M. Lutterbach (2) e E. Sérvulo (*)
(1) Universidade Federal do Rio de Janeiro, Escola de Química, Av. Athos da Silveira Ramos, 149, Ilha do Fundão, 21941-909, Rio de Janeiro - RJ – Brasil.
(2) Instituto Nacional de Tecnologia, Laboratório de Biocorrosão e Biodegradação, Av. Venezuela, 82, 20081-312 – Rio de Janeiro – RJ – Brasil, e-mail: marcia.lutterbach@int.gov.br
(*) A quem a correspondência deve ser dirigida, e-mail: lindomarc@eq.ufrj.br
RESUMO
A utilização de biocidas tem sido uma das estratégias adotadas para o controle de microrganismos em sistemas aquosos, a fim de impedir a corrosão induzida microbiologicamente (MIC). Este trabalho teve como objetivo avaliar a ação de três biocidas comerciais - sulfato de tetrakis hidroximetil fosfônico (THPS), combinação de sais quaternários de amônio (QUATs) e THPS+QUATs – em água de produção para diferentes concentrações dos biocidas (50 e 100 ppm). A eficácia dos biocidas foi realizada contra populações planctônicas e sésseis de bactérias heterotróficas aeróbias (BHA), produtoras de ácido aeróbias e anaeróbias (BPAA, BPAAn) e redutora de sulfato (BRS). Com exceção das BRS, o THPS não apresentou toxicidade contra as BHA, BPAA e BPAAn em nenhuma das condições testadas. Os biocidas QUATs e THPS+QUATs causaram inibição do crescimento de todos os grupos bacterianos, nas duas concentrações ensaiadas. Na presença de microrganismos o potencial dos corposde- prova variaram para valores negativos e quando aplicado 100 ppm do biocida THPS+QUATs, os potenciais alcançaram um platô de estabilização.
Palavras-chave: Biocidas, Aço Duplex, Corrosão Induzida Microbiologicamente (MIC), Bactérias
ABSTRACT
The use of biocides has been a useful strategy for the control of microorganisms in aqueous systems to prevent microbiological induced corrosion (MIC). This study aimed the evaluation of the action of three commercial biocides - tetrakis hydroxymethyl phosphonic sulfate(THPS), combination of quaternary ammonium salts (QUATs) and THPS + QUATs - in oil produced water for different concentrations of biocides (50 and 100 ppm) against planktonic and sessile populations of aer obic heterotrophic bacteria (BHA), acid-producing aerobic and anaerobic (BPAA, BPAAn) and sulfate reduction bacteria (BRS). With the exception of BRS, the THPS showed no toxicity against BHA, BPAA and BPAAn in any of the conditions tested. QUATs and THPS+QUATs biocides inhibited the growth of all bacterial groups at both concentrations tested. In the presence of microrganisms, the open circuit potential of the steel coupons tended to negative values while when 100 ppm of the THPS+QUATs biocide was applied, it could be seen a potential stability plateau.
Keywords: Biocides, Duplex Steel, Microbiologically Induced Corrosion (MIC), Bacteria
1. INTRODUÇÃO
No processo de extração do petróleo são coproduzidos grandes volumes de água, um efluente complexo, de salinidade elevada, contendo minerais dissolvidos, hidrocarbonetos, ácidos orgânicos, sólidos e gases dissolvidos, como CO2 e H2S [1]. Portanto, apesar da elevada salinidade, a água de produção apresenta condições de cultivo que permitem o desenvolvimento de uma grande diversidade de espécies microbianas, particularmente as bactérias [2 - 6]. Estes microrganismos têm em comum a capacidade de se desenvolver em ambientes salinos, o que lhes confere a denominação de halofílicos.
No ambiente, os microrganismos tendem a aderir às superfícies, cuja colonização leva à formação de estruturas denominadas biofilmes. Em geral, a atividade microbiana nos biofilmes causa a degradação dos materiais, metálicos e não metálicos, acarretando diversos prejuízos de ordem econômica e ambiental. Especificamente no caso de estruturas metálicas, a interação de diferentes populações microbianas pode resultar na sua corrosão, quer direta quer indiretamente. Na indústria do petróleo, os problemas causados pela corrosão induzida microbiologicamente (MIC) são mais cruciais em virtude da elevada quantidade de material utilizado. A malha dutoviária brasileira tem extensão superior a 20 mil km [7]. Dentre os problemas causados pela MIC, destacam-se: entupimento de reservatórios causados pelo aumento da biomassa bacteriana e/ou formação de sulfeto de ferro; maior consumo de energia; e diminuição da vida útil dos equipamentos [8, 9].
Para combater os problemas causados pela MIC, a indústria petrolífera tem feito um grande investimento em biocidas. A principal atuação desses produtos está baseada na supressão do crescimento e/ou atividade metabólica microbiana, que pode ser função de: modificação da permeabilidade da parede celular; alteração dos processos vitais relacionados com a sua reprodução; ou, através da reação com enzimas microbianas, interferindo deste modo em todo o metabolismo, inclusive podendo levar à morte [10, 11].
De uma maneira geral, o modo como se aplica o biocida é tão importante quanto a sua seleção, posto que a simples aplicação do biocida pode não reduzir convenientemente a população microbiana, se não forem empregadas a dosagem e a frequência corretas [10, 11]. Ao contrário, nestes casos, os microrganismos podem criar mecanismos de resistência aos biocidas, dificultando o controle do seu crescimento, e, consequentemente dos danos por eles causados. Além disso, o desempenho do biocida pode ser comprometido por diferentes fatores, como, por exemplo, as propriedades físicas e químicas do ambiente. Logo, se a aplicação do biocida não for feita adequadamente, corre-se o risco de agravamento do problema [10, 12].
É, portanto, imperativo que o biocida seja compatível com o sistema operacional, devendo-se estabelecer a estratégia de tratamento, baseada principalmente na concentração do biocida e no tempo de contato [13, 14]. O tempo de contato deve ser bem definido, posto que muitos dos microrganismos não são eliminados por contato imediato com a maioria dos biocidas usados industrialmente [12, 15]. Em alguns casos pode-se, inclusive, induzir a resistência das bactérias potencialmente causadoras da MIC. Estes parâmetros, apesar de serem geralmente recomendados pelo produtor/fornecedor dos biocidas, devem ser sempre ajustados às características do sistema, primeiramente em condições de teste controladas e, posteriormente, a serem confirmadas em condições operacionais reais.
Face ao exposto, o presente trabalho teve como objetivo avaliar a ação de três biocidas comerciais - THPS (sulfato de tetrakis hidroximetil fosfônico) – Quaternário de amônio (combinação de QUATs) e a combinação de THPS e QUAT, em duas concentrações, 50 e 100 ppm, contra populações bacterianas consideradas principais responsáveis pela MIC em água de produção.
2. METODOLOGIA EXPERIMENTAL
Corpos de prova (CPs)
Foram utilizados corpos-de-prova (CPs) retangulares de aço duplex (UNS S 31803) de diferentes dimensões. Para o monitoramento microbiológico, foram usados CPs de (4,0 x 1,0 x 0,3) cm e furo de 0,2 cm de diâmetro, perfazendo uma área total de aproximadamente 8,0 cm2, considerando as duas faces do CP. Antes do uso, os CPs foram polidos com lixa 600, desengordurados por imersão em acetona, secos com jato de ar quente e mantidos em dessecador à temperatura ambiente até ao momento de uso. Para as medidas de potencial em circuito aberto, CPs de (2,0 x 1,0 x 0,3) cm, embutidos em uma resina epoxídica, deixando área exposta de aproximadamente 2 cm2, foram conectados a um fio de cobre, de modo a permitir as medições eletroquímicas. Imediatamente antes do uso, os CPs foram polidos (lixa 600), lavados com água destilada, seguida de álcool etílico, e secos com jato de ar quente.
Biocidas
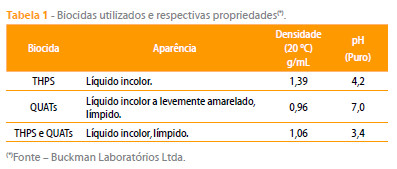
Foram utilizados três biocidas comerciais, gentilmente doados pela Buckman Laboratórios Ltda: THPS (sulfato de tetrakis hidroximetil fosfônico), um blend formado por uma combinação de sais quaternários de amônio (QUATs) e outro blend originário da mistura dos produtos THPS e QUATs. As propriedades típicas destes biocidas estão indicadas na Tabela 1.
Microrganismos
Os microrganismos halofílicos utilizados neste trabalho foram isolados de água coletada em oleoduto. Para a coleta foram utilizados dois frascos estéreis de 100 mL, sendo a água neles armazenada para transporte ao laboratório em condição refrigerada (cerca de 10 °C), por acondicionamento em sacolas térmicas com sacos de gel refrigerantes reutilizáveis. Num prazo inferior a 24 h, a água foi analisada microbiologicamente. Para tanto, duas amostras de 10 mL do material coletado foram distribuídos em frasco Erlenmeyer de 250 mL de capacidade contendo 90 mL de solução salina para seleção de bactérias aeróbias e em frasco tipo penicilina de 100 mL contendo 90 mL de solução redutora (contendo em g/L: tioglicolato de sódio 0,124, ácido ascórbico 0,1 + 4 mL de solução de rezasurina 0,025 %) para seleção de bactérias anaeróbias. Após devidamente homogeneizados, de cada um foram tomadas alíquotas de 1 % (v/v) que a seguir foram inoculadas em meios de cultura específicos com salinidade crescente para seleção de microrganismos consideradas principais promotoras da MIC, conforme descrito a seguir:
- Bactérias heterotróficas aeróbias (BHA) em caldo nutriente (g/L): Peptona de carne 5,0 ; Extrato de levedura 3,0 ; Dextrose 9,0 e pH ajustado para 7,0 ± 2;
- Bactérias produtoras de ácido aeróbias (BPAA) e bactérias produtoras de ácido anaeróbias (BPAAn) em caldo vermelho de fenol (g/L): Extrato de peptona 10; Extrato de carne 1,0; Vermelho de fenol 0,018; Glicose 10 e pH = 7,4 ± 2. Para BPAAn, a condição de anaerobiose foi garantida através de purga de nitrogênio no meio;
- Bactérias redutora de sulfato (BRS) em meio Postgate E (g/L): KH2PO4 0,5; NH4Cl 1,0 ; CaCl2.6H2O 1,0 ; MgCl2.7H2O 2,0 ; FeSO4.7H2O 1,0 ;Extrato de lêvedo 0,1; Ácido ascórbico 0,5; Agar-agar 5,0 + 7 mL de solução de lactato de sódio 50 %; 4 mL de solução de resazurina 0,025 % e pH ajustado para 7,6 ± 2.
Tão logo observado o crescimento das populações bacterianas, foram realizados sucessivos subcultivos de modo a obter culturas enriquecidas de bactérias halofílicas de cada grupo capazes de se desenvolver próximo de 160 g/L de NaCl.
Eletrólito
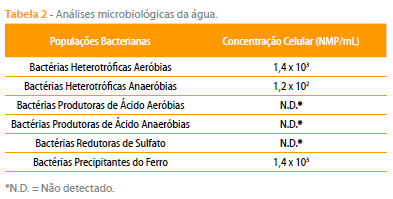
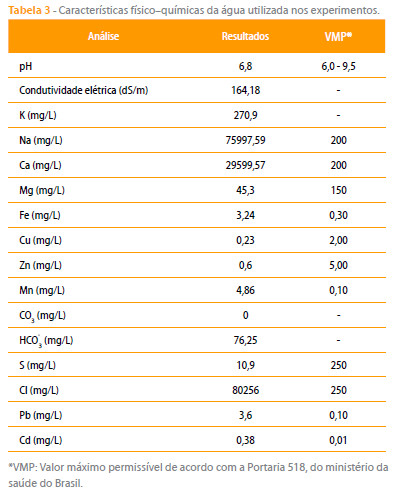
Os ensaios foram realizados com água de produção de uma plataforma offshore, contendo cerca de 160 g/L de NaCl. As concentrações de microrganismos encontrados neste eletrólito foram descritas na Tabela 2, enquanto as características físico-químicas são apresentadas na Tabela 3.
Para a realização dos ensaios, a água de produção foi suplementada com (g/L): KH2PO4 0,5; NH4Cl 1,0, extrato de levedura 0,2 e ácidos orgânicos de cadeia curta (ácido lático 60,8; ácido propiônico 50,0 e ácido butírico 44,6), conforme descrito por Sousa [2] e o pH ajustado para 6,0 afim de favorecer a atividade dos microrganismos e, consequentemente induzir a colonização do metal. E ainda, devido à baixa concentração de bactérias heterotróficas aeróbias e anaeróbias, e de bactérias precipitantes do ferro, a água foi enriquecida com as culturas halofílicas anteriormente selecionadas, de modo a estabelecer concentrações iniciais de 108 células/mL de cada um dos grupos bacterianos.
Célula experimental
Os experimentos foram conduzidos em cubas de vidro de 1 L de capacidade, contendo 800 mL do eletrólito, onde foram dispostos os CPs, fixados à tampa por fios de nylon. O eletrólito foi mantido em constante e suave agitação, por meio de bastão magnético e placa de agitação, o mínimo requerido para manter as células planctônicas em suspensão e, assim, favorecer a colonização das superfícies metálicas.
Antes e após cada experimento, a cuba foi desinfetada por imersão em solução de 5 g/L de metabissulfito de sódio por 24 horas, sendo a seguir lavada por cinco vezes com água destilada estéril, para a total remoção do desinfetante. O sistema foi mantido em sala climatizada, com temperatura variando de 25 a 27 ºC.
Etapas Experimentais
Avaliação da toxicidade dos biocidas contra as populações bacterianas
Os grupos de microrganismos principais responsáveis pela MIC (BHA, BPAA, BPAAn e BRS) foram expostos aos três biocidas comerciais - THPS, QUATs e THPS+QUATs - em duas concentrações (50 e 100 ppm). Para as populações anaeróbias (BPAAn, BRS), os ensaios foram realizados em frascos do tipo penicilina, de 50 mL de capacidade, contendo 45 mL de meio de cultura específico, purgado com nitrogênio. Neste caso, os frascos foram vedados com tampa de borracha e lacrados com selo de alumínio para garantir condição de anaerobiose. Já as populações aeróbias (BHA, BPAA) foram cultivadas em frascos do tipo penicilina, de 50 mL de capacidade, contendo 45 mL de meio, com vedação feita com rolha de algodão, de modo a permitir a difusão de oxigênio.
Aos meios foram adicionadas amostras dos biocidas, convenientemente diluídas de modo a estabelecer a concentração desejada no meio. Depois de homogeneizados, 0,1 mL de um dos cultivos bacterianos foram adicionados a cada frasco, conforme indicado por Gaylarde [14]. Os cultivos foram analisados diariamente por um período total de 28 dias.
Efeito dos biocidas nas populações planctônicas e na colonização do aço duplex em água de produção
Os ensaios foram realizados na célula experimental, anteriormente descrita, com água de produção na presença de biocida (50 e 100 ppm) e na sua ausência, para fins comparativos. As concentrações das populações bacterianas planctônicas e sésseis foram determinadas em 168 e 360 horas.
Análise comparativa do potencial em circuito aberto dos sistemas experimentais
As medições dos potenciais em circuito aberto dos CPs em relação ao Eletrodo de Calomelano Saturado foram realizadas periodicamente, com o auxílio de um multímetro portátil (Minipa Et 20 33) por um tempo total de 360 horas. Os valores plotados nos gráficos correspondem as médias de potenciais de 2 CPs.
Metodologias Analíticas
Quantificação celular
As populações de BHA, BPA e BRS, nas fases planctônica e séssil, foram quantificadas pela técnica do Número Mais Provável (NMP) [16] através do cultivo, nos respectivos meios apropriados: meio líquido nutriente (Merk No 5443, Germany), meio vermelho de fenol - BBL Phenol Red Broth Base - (BD - Becton Dickinson & Company) acrescido de 1 % (m/v) de glicose, e meio Postgate E modificado [17] sendo acrescido aos meios 160 g/L de NaCl. No caso das BPA, os cultivos foram incubados em condição de aerobiose e anaerobiose, para quantificação das BPAA e BPAAn, respectivamente.
3. RESULTADOS
Avaliação da toxicidade dos biocidas contra as populações bacterianas
Na Tabela 4 são apresentados os comportamentos das populações bacterianas quando expostas ao biocida THPS, em duas diferentes concentrações, por um período total de 28 dias. As populações aeróbicas (BHA e BPAA) apresentaram desempenho similar, tendo sido observado crescimento somente decorridas 72 h quando cultivadas na presença de 50 ou 100 ppm do biocida. Comparativamente, as bactérias produtoras de ácido, quando cultivadas em anaerobiose, foram mais resistentes, só tendo sido detectado crescimento com 96 h. Note-se que as BRS foram susceptíveis ao biocida nas diferentes concentrações e tempos de exposição ensaiados, demonstrando a sua eficácia contra este grupo bacteriano, mesmo em alta salinidade.
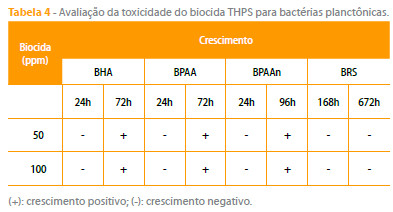
Os biocidas contendo QUATs e THPS+QUATs inibiram o crescimento de todos os grupos bacterianos, em todas as concentrações ensaiadas, por isso os dados não foram apresentados. O biocida composto de THPS+QUATs ocasionou maior impacto nas populações microbianas do que o THPS e QUATs separadamente, onde se pode inferir que quando estes dois compostos são utilizados combinados tornam-se mais tóxicos contras estas populações microbianas.
Efeito dos biocidas nas populações planctônicas e nos biofilmes formados sobre aço duplex em água de produção
Na Figura 1 são apresentadas as variações das concentrações celulares nas fases planctônica (A) e séssil (B) em água de produção, expressas em valores médios de NMP/mL e NMP/cm2, respectivamente. Com exceção das BRS, o número inicial das diferentes populações bacterianas monitoradas, da ordem de 108 células/mL cada, decorridas 168 h, manteve-se (Figura 1(A)). Para 360 h, foram detectados aumentos das populações microbianas em 1 a 3 ordens de grandeza, sendo a maior amplitude referente às BHA. No caso das BRS, houve uma redução do número na fase planctônica, que se manteve inalterado durante todo o período monitorado.
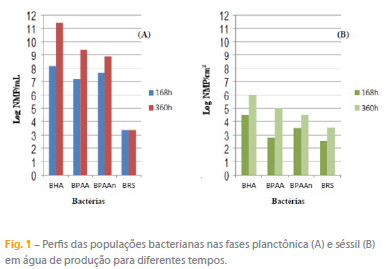
Na fase séssil (Figura 1(B)), foi determinada a viabilidade de todos os grupos bacterianos no período monitorado, com o predomínio das bactérias aeróbias, particularmente das BHA. Destaca-se que este grupo bacteriano compreende as espécies potencialmente produtoras de substancias poliméricas extracelulares (EPS, extracelullar polymeric substances), que favorecem a adesão destes e de outros microrganismos não produtores de EPS, resultando na rápida colonização das superfícies dos materiais. O EPS, em conjunto com o metabolismo das bactérias que o produzem, criam as condições nutricionais (produção de ácidos e H2) e físicas (redução do potencial redox) para o desenvolvimento dos microrganismos anaeróbios, particularmente as BRS [18]. Também ao EPS são atribuídos: propriedade protetora contra produtos químicos, como biocidas e inibidores de corrosão; servir de fonte nutricional, quando os microrganismos se encontram em fase de estarvação; estimular a degradação do material metálico, devido a presença de grupos funcionais negativos que reagem com íons metálicos intensificando o processo corrosivo [19, 20].
A Figura 2 apresenta os resultados de concentração celular nas fases planctônica (A, C, E) e séssil (B, D, F) para os ensaios realizados com água de produção com uma única aplicação dos biocidas, na concentração de 50 ppm para diferentes tempos.
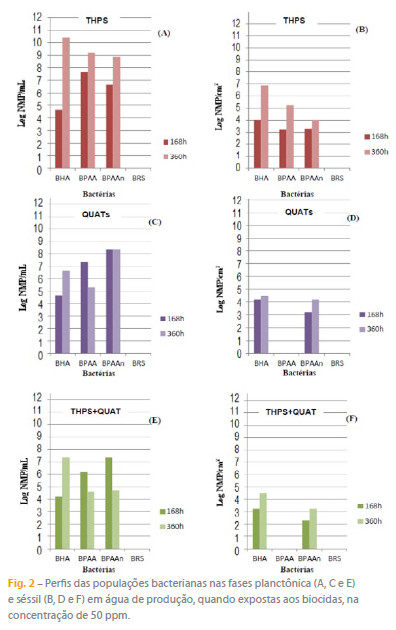
Analisando as Figuras 1 e 2 pode-se inferir que os três biocidas foram efetivos contra BRS na fase planctônica, refletindo em ausência de BRS nos biofilmes formados sobre as superfícies dos CPs durante todo o período. Comparativamente, o biocida THPS foi o que causou menor impacto nas demais populações microbianas (Figuras 2(A) e 2(B)).
Para este biocida, todos os grupos analisados apresentaram aumentos de pelo menos uma ordem de grandeza ao longo do tempo. Contudo, quando em mistura com QUATs, a ação foi mais efetiva no controle das bactérias tanto na fase planctônica quanto na séssil (Figuras 2 (A)-2(F)). Segundo Takahashi et. al [21] e Van der Kraan et. al [22], em geral, a associação de biocidas pode ser desenvolvida de modo a ser mais eficaz contra os microrganismos. Assim sendo, a combinação de produtos químicos pode alcançar maiores índices de desempenho tanto para eliminação rápida, como para a eliminação em longo prazo para cargas microbianas elevadas.
Os biocidas à base de QUATs foram capazes de inibir totalmente a atividade das bactérias aeróbias produtoras de ácido no biofilme, embora na fase planctônica a sua eficácia tenha sido parcial (Figuras 2(C)-2(D)).
Note-se que as BHA foram resistentes aos três biocidas, embora comparativamente os produtos à base de QUATs tenham tido um melhor desempenho no seu controle em ambas as fases (Figuras 2(A)- 2(F)).
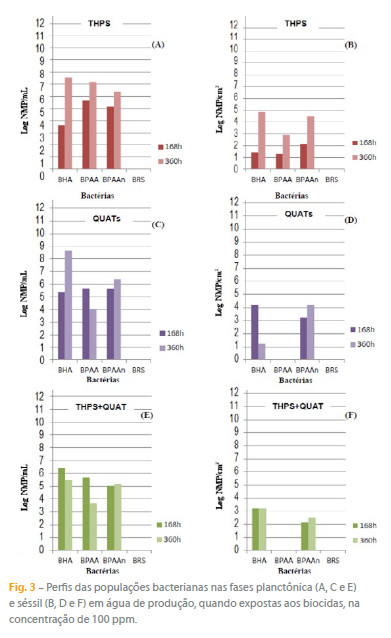
O comportamento das populações bacterianas quando expostas a concentração de 100 ppm dos biocidas é apresentado na Figura 3. Foram constatados perfis semelhantes aos obtidos quando as populações microbianas foram tratadas com menor concentração dos biocidas. Portanto, ratifica-se o melhor desempenho do biocida contendo os composto de THPS+QUATs. No entanto, o aumento da concentração dos biocidas resultou em melhor controle das populações bacterianas ao longo do tempo, uma vez que as concentrações se mantiveram inalteradas ou reduziram.
Análise comparativa do potencial em circuito aberto dos sistemas experimentais
A Figura 4 ilustra as curvas de potencial com o tempo, obtidas para os sistemas montados para estudo.
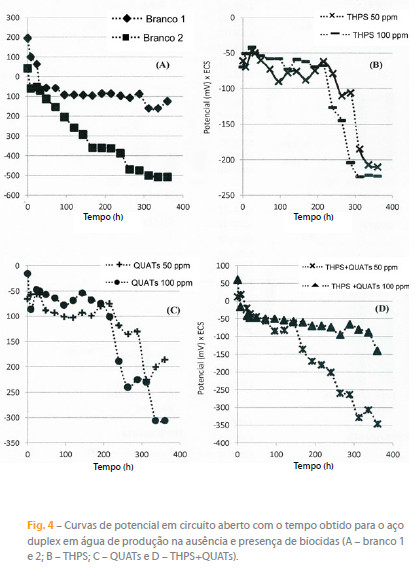
Na Figura 4(A) é apresentada a variação do potencial dos CPs do Aço Duplex quando exposto ao sistema sem biocidas e sem microrganismos (branco 1) e sem biocida e com microrganismos (branco 2). Quando o metal foi exposto ao meio na ausência tanto de biocidas quanto de microrganismos observou-se queda do potencial nas primeiras 96 horas, até atingir uma região de estabilização, a qual permaneceu até às 288 horas de exposição. A queda inicial do potencial pode estar associada à percolação de íons agressivos através da camada passiva do metal [23]. Um comportamento diferenciado pode-se observar quando o mesmo é exposto ao meio sem biocidas e com microrganismos (branco 2): o gráfico mostra uma tendência do potencial em se deslocar para valores cada vez mais negativos com o tempo, o que ocorreu desde o início da imersão dos CPs na água de produção, o que pode indicar a formação de um biofilme de maneira heterogênea na superfície metálica. Este fato associado à presença de elevada concentração de íons cloreto, pode ter favorecido as diferenças de potencial entre áreas do metal recobertas com biofilme e áreas sem recobrimento bacteriano. Fazendo uma análise comparativa deste comportamento do potencial (Figura 4(A) – branco 2) com a quantificação bacteriana mostrada na Figura 1, os metabólitos produzidos por estes microorganismos presentes, principalmente em sua fase séssil, pode alterar o potencial, contribuindo para a degradação da camada passiva. No entanto, entre 168 e 216 horas de exposição, o potencial atinge um platô em torno de -360 mV e, após esse tempo, voltou a cair, atingindo estabilização em potenciais em torno de -500 mV ao final do experimento.
Quando os CPs foram expostos na presença de microrganismos e do biocida contendo apenas THPS em concentrações de 50 e 100 ppm (Figura 4(B)) obser va-se que as cur vas do potencial nas duas concentrações têm comportamentos semelhantes inicialmente, apresentando relativa estabilidade dos potenciais nas primeiras 200 horas, o que pode inferir a uma maior homogeneidade do biofilme. Esse fato pode ser corroborado através dos resultados apresentados na Tabela 4 e Figura 2(A) e 2(B), onde é possív el observar que o biocida THPS, com exceção das BRS, causou menor impacto sobre os grupos bacterianos. Após as primeiras 200 horas observou-se queda nos valores de potencial o que pode indicar a ocorrência de ataque à superfície metálica por íons agressivos (cloretos).
No caso do biocida contendo QUATs (Figura 4(C)) nas duas concentrações estudadas (50 e 100 ppm), quando os CPs foram colocados na presença deste biocida e microrganismos também ocorreu queda do potencial nas primeiras horas de exposição à água de produção. Porém, no intervalo de 24 e 192 horas de exposição, o potencial sofreu poucas variações indicando uma certa estabilidade. Após 216 horas de exposição o potencial voltou a diminuir, fato este explicado por provável remoção parcial do biofilme concomitantemente à percolação de íons agressivos.
Já quando os CPs foram expostos na presença do biocida contendo THPS+QUATs e microrganismos (Figura 4(D)) nas concentrações de 50 e 100 ppm na água de produção, também se observa queda do potencial nas primeiras 24 horas. Analisando o gráfico, observa-se que quando exposto a 50 ppm, com o passar do tempo, o potencial é deslocado para valores cada vez mais baixos, não sendo detectada nenhuma região de estabilização. No entanto, quando exposto a 100 ppm, observa-se uma região de estabilização do potencial (em torno de -50 mV) entre 48 e 240 horas de exposição, o qual após 240 horas retornou a variar moderadamente, até o final dos experimentos. Este comportamento do potencial pode também estar relacionado com o efeito inibitório que o biocida teve contra as populações bacterianas (Tabela 4) e o impacto causado nas populações tanto nas fases planctônicas quanto séssil (Figuras 2 e (3), o que fez com que provavelmente diminuísse a produção de metabolitos que atacasse a superfície do metal. Por outro lado, esta curva também mostra comportamento semelhante à curva do potencial do branco 1 (Figura 4(A) ), o que criou uma barreira (filme) entre superfície metálica e a água de produção, levando a estabilização dos potenciais, devido ao facto de o filme formado ter sido menos degradado.
Em todos os casos analisados, observa-se evolução do potencial para valores mais ativos, devido à provável degradação da camada passiva mediante a elevada salinidade do meio. Além disso, os microrganismos produzem metabolitos que podem atacar a superfície metálica, o que ajuda na degradação desta camada passiva. A colonização da superfície formando biofilme (não homogêneo) ocasiona corrosão por arejamento diferencial, o que afeta os valores de potencial, conforme pode ser observado na Figura 4(A).
CONCLUSÕES
-Individualmente, o biocida contendo THPS foi mais efetivo no controle das BRS, planctônicas e sésseis;
-Os biocidas contendo QUATs e THPS+QUATs – mesmo na concentração de 50 ppm tiveram ação inibitória para BHA, BPAA, BPAAn, além das BRS;
-O biocida contendo THPS+QUATs causou maior impacto nas populações bacterianas promotoras da MIC;
-As análises de potencial em circuito aberto mostram uma evolução dos potenciais para valores mais ativos, devido à provável degradação da camada passiva mediante a elevada salinidade do meio e ação dos microrganismos na superfície dos CPs.
-Quando os CPs do aço duplex foram expostos na presença dos biocidas e microrganismos, o biocida contendo THPS+QUATs causou maior impacto nas populações bacterianas, e quando aplicado 100 ppm deste biocida houve menor degradação da camada passiva (o que pode ser observado pelo potencial), levando o potencial a um platô de estabilização.
REFERÊNCIAS
[1] D. S Vieira, M. C. Cammarota e E. F. C. Sérvulo (Redução de contaminantes presentes na água de produção de petróleo), in Proceedings do 2º Congresso Brasileiro de P&D em Petróleo & Gás, Joinville, Brasil (2003).
[2] K. A. Sousa (Avaliação da biogênese de sulfeto sob diferentes concentrações de bactérias redutoras de nitrato, bactérias redutoras de sulfato e nitrato), dissertação apresentada para obtenção do grau de Doutor em Tecnologia de Processos Químicos e Bioquímicos, Escola de Química, Universidade Federal do Rio de Janeiro, Rio de Janeiro, Brasil (2009). [ Links ]
[3] A. J. Dinning, D. Oliphant, E. A. Vik, and L. Bruas (Initial souring monitoring and souring-mitigation testing using an online souringmitigation cabinet (SMC) prior to live produced water reinjection (PWRI) and nitrate-based souring-mitigation treatment on Norske Shells Draugen Platform), in Proceedings of SPE International Symposium On Oilfield Chemistry, Houston (2005). [ Links ]
[4] G . Voordouw, T. Jack (Proposal for NSERC industrial research chair in petroleum microbiology: development of a competency cluster within ISEEE at the University of Calgary), Calgary, Canada (2005). [ Links ]
[5] A. J. Dinning, G. E. Jennerman, K. Voldum and E. A. VIK (The use of nitrate/nitrite on control in PWRI – experiences Ekofisk Field) in Proceedings of 15th International Oilfield Chemistry Symposium, Geilo, Norway (2004). [ Links ]
[6] G. E. Jenneman, A. J. Dinning, K. Voldum and E. A. Vik (The effect of nitrate/nitrite on control of souring in produced water at the Ekofisk Field) in Proceedings of NIF Internacional Produced Water Conference, Stavanger, Norway (2004). [ Links ]
[7] A. Gasparini (Transporte dutoviário e meio ambiente. O controle da rede de dutovias terrestres da Petrobrás operadas pela Transpetro), Instituto Militar de Engenharia IME, Agosto, Rio de Janeiro, Brasil (2006). [ Links ]
[8] V. Gentil. Corrosão, 6ª Ed., LTC-Livros Técnicos e Científicos, Rio de Janeiro, Brasil (2012). [ Links ]
[9] H. A. Videla. Biocorrosão, Biofouling e Bioterioração de materiais. 1ª Ed., Edgard Blücher Ltda, São Paulo, Brasil (2003). [ Links ]
[10] R. V. Capelleti (Avaliação da atividade de biocidas em biofilmes formados a partir de fluídos de corte utilizados em usinagem de metais), dissertação apresentada para a obtenção do grau de Mestre em Engenharia Química, Faculdade de Engenharia Química, Universidade Estadual de Campinas, Campinas, Brasil (2006). [ Links ]
[11] C. C. Gaylarde and L. H. G. Morton, Biofouling, 14, 59 (1999). [ Links ]
[12] R. W. Lutey (Process cooling water), in Handbookof Biocide and Preservative Use. (Rossmore, H. W. ed.), Blackie Academic & Professional, Glasgow, UK (1995). [ Links ]
[13] H. A. Videla, Int. Biodeter. Biodegr., 49, 259-270 (2002). [ Links ]
[14] P. M. Gaylarde and C. C. Gaylarde, Int. Biodeter. Biodegr., 29, 273-283 (1991). [ Links ]
[15] K. A. Heinzel, I. W. Sutherland and V. J. Matin, Microbiology, 144, 3039- 3047 (1998). [ Links ]
[16] A. P. Harrison, Appl. Environ. Microb., 131, 68-76 (1982). [ Links ]
[17] J. R. Postgate. The sulphate-reducing bacteria, 2ª Ed., Press Sindicate of the University of Cambridge, New York, USA (1984). [ Links ]
[18] I. B. Beech and C. C. Gaylarde, J. Appl. Bacteriol., N. 67, 201-207 (1989). [ Links ]
[19] T. M. Madigan, Martinko Jm, P. V. Dunlap and D. P. Clark. Microbiologia de Brock, 12ª Ed., Artmed, Porto Alegre, Brasil (2010). [ Links ]
[20] J. W. Costerton, Z. Lewandowski, D. E. Caldwell, D. R. Korber and H. M. Lappin-Scott, Annu. Rev. Microbiol., 49, 711-745 (1995). [ Links ]
[21] D. Takahashi, M. V. Enzien, B. Yin and S. Bottero. Aumente a produção de gás e petróleo com programas aprimorados de controle microbiano. Disponível em: http://oilandgas.dow.com/pdf/rio/de_controle_microbiano.pdf (Acesso em 14/03/2013). [ Links ]
[22] G. M. Van Der Kraan, D. Jocksch, M. Canalizo-Hernandez, B. Yin, T. Williams and P. A. Keene. Implementação de melhores soluções para o controle microbiano em processos petrolíferos. Disponível em: http://www.dow.com/microbial/la/pt/pdf/PaperPortuguese.pdf (Acesso em 14/03/2013). [ Links ]
[23] S. Wolynec. Técnicas Eletroquímicas em Corrosão, Editora USP, São Paulo, Brasil (2003). [ Links ]
AGRADECIMENTOS
Os autores agradecem a Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES) pela concessão da bolsa de doutorado, ao Laboratório de Corrosão Professor Vicente Gentil (EQ/ UFRJ) e ao Laboratório de Biocorrosão (LABIO/INT) pelo apoio no desenvolvimento deste trabalho.
Artigo submetido em Maio de 2013 e aceite em Outubro de 2013













