Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Corrosão e Protecção de Materiais
versão On-line ISSN 2182-6587
Corros. Prot. Mater. vol.31 no.3-4 Lisboa 2012
Avaliação da resistência à corrosão da liga de alumínio 6101 após diferentes tratamentos térmicos de precipitação
Evaluation of corrosion resistance of 6101 aluminum alloy after differents precipitation heat treatment
F. Abreu1, A. Sabariz1, A. Quadro1 e A. Bueno1
1 Universidade Federal de São João Del Rei. Departamento de Engenharia mecânica, Praça Frei Orlando, 170, centro, São João Del Rei - MG, Brasil
A quem a correspondência deve ser dirigida, e-mail: fernandobh@msn.com
RESUMO
Atualmente, as ligas de alumínio da série 6xxx vêm ocupando um espaço importante na produção global das ligas de alumínio. A utilização em larga escala dessa classe de ligas é consequência da melhoria de suas propriedades mecânicas quando submetidas a tratamentos térmicos. No entanto, a realização de tratamentos térmicos de solubilização e a precipitação de fases metaestáveis durante o envelhecimento podem prejudicar consideravelmente a resistência à corrosão dessa classe de ligas. O presente trabalho, objetiva avaliar a suscetibilidade à corrosão da liga de alumínio 6101 submetida a tratamentos térmicos de solubilização. Investigou-se a corrosão através da realização de ensaios de potencial ao longo do tempo e curvas anódicas de polarização. Avaliou-se qualitativamente a formação de pites através de microscopia eletrônica de varredura (MEV). As soluções de 3,5 % de NaCl e 0,1 M de Na2SO4 foram utilizadas nos ensaios para simular condições de alta agressividade.
Palavras Chave: Ligas de Alumínio, Corrosão por Pite, Tratamento Térmico de Solubilização
ABSTRACT
Currently, 6xxx series aluminum alloys have been occupying an important place in the global production of aluminum alloy. The wide use of this class of alloys is a result of improvement on mechanical properties when subjected to heat treatments. However, the thermal treatments of solubilization and precipitation of metastable phases during aging may impair the corrosion resistance of this class of alloys. The present study aims to evaluate the corrosion behavior of aluminum alloy 6101 after heat treatment of solubilization by testing over time and anodic polarization curves. The formation of pits was evaluated by scanning electron microscopy (SEM). Solutions of 3.5 % NaCl and 0,1 M Na2SO4 were used in order to simulate conditions of high aggressiveness.
Keywords: Aluminum Alloys, Pitting Corrosion, Heat Treatment of Solubilization
1. INTRODUÇÃO
A utilização em larga escala das ligas de alumínio está associada, entre outros fatores, à excelente combinação entre o baixo peso específico e a boa resistência mecânica, que em alguns casos se iguala ao aço estrutural. Essa característica é fundamental em aplicações industriais, tais como, navios, aviões, automóveis, etc [1].
Dentre as ligas de alumínio mais utilizadas, as ligas da série 6xxx se destacam, pois apresentam grande aumento de resistência mecânica e dureza quando submetidas a tratamentos térmicos de solubilização. Uma das características importantes desse grupo de ligas é a resistência à corrosão, que está associada à presença de um filme aderente de alumina (Al2O3), que se desenvolve naturalmente na superfície das ligas sob condições atmosféricas normais [2].
No entanto, a presença de poluentes específicos, em especial o SOl2 e o Cl, podem afetar a cinética de corrosão por meio da dissolução do filme passivo. Consequentemente, ataques corrosivos localizados podem provocar à perda de resistência mecânica e levar o material a falha, mesmo que este tenha boas propriedades como é o caso da liga de alumínio 6101 [3, 4].
2. REVISÃO BIBLIOGRÁFICA
As ligas de alumínio representam um importante grupo de materiais, em consequência do seu elevado valor tecnológico e da extensa gama de aplicações industriais, principalmente nas indústrias naval, aeroespacial, automotiva e doméstica [5]. As baixas densidades combinadas com características como: boa condutibilidade elétrica e térmica, elevada refletividade à luz e ao calor e excelente resistência à corrosão são fatores que contribuem para o uso e produção em larga escala dessas ligas.
Atualmente, as ligas de alumínio da série 6xxx vêm ocupando um espaço importante na produção global das ligas de alumínio. Recentemente mais de 80% das ligas empregadas na produção mundial de perfis extrudados fazem parte do sistema Al-Mg-Si [6]. A utilização em larga escala dessas ligas ocorre devido a melhoria de suas propriedades mecânicas quando submetidas a tratamentos térmicos [7]. Outra característica importante das ligas de alumínio da série 6xxx é a sua boa resistência à corrosão, que ocorre devido ao fenômeno da passivação, mas pode ser prejudicada pela realização de tratamentos térmicos e pela presença de determinados agentes corrosivos que influenciam a cinética de corrosão [4].
Do ponto de vista termodinâmico, o metal alumínio é um material instável, não existe na natureza sob a forma elementar, e a sua tendência natural é voltar à condição inicial de minério. Assim, ele seria um metal susceptível a corrosão em ambientes naturais. Contudo, o referido fenómeno de passivação, formação de uma camada de óxido ou hidróxido em sua superfície, torna o alumínio bastante resistente à corrosão na maior parte dos ambientes naturais [8].
A passivação em ligas de alumínio é um tema complexo e controverso. Alguns autores consideram que a passivação seja causada por um filme de óxido formado na superfície metálica, ou a um estado oxidado que impede o contato direto entre metal e meio corrosivo [8 -10]. Estudos recentes, consideram que a resistência a corrosão das ligas de alumínio esta associada à presença de um filme fino e compacto de óxido de alumina (Al2O3), que se desenvolve naturalmente na superfície das ligas sob condições atmosféricas normais [2,3,11]. A espessura desse filme protetor cresce muito mais rapidamente na água do que no ar, formando-se filmes mais espessos na ausência de oxigênio. A espessura normal desse tipo de filme é da ordem de 5 nanômetros [11].
A proteção contra corrosão fornecida por essa película varia, entre outros, de acordo com a composição de liga, microestrutura e meio corrosivo. A alteração de algum desses fatores influencia diretamente a velocidade e morfologia da corrosão.
Nas ligas de alumínio, a formação de pite está associada a uma divisão em pontos específicos da película de óxido, quando a liga está exposta em ambientes contendo íons haleto, dos quais o cloreto é o mais comum. A intensidade do ataque corrosivo por pite é influenciada pela concentração do haleto, temperatura, velocidade de fluido e pH. Geralmente, a formação do pite nas ligas de alumínio ocorre na presença de um eletrólito em uma faixa de pH entre 4,5 e 8,5 e tende a aumentar com o aumento da temperatura e concentração de íons agressivos [10].
Diferentemente da corrosão por pite, a corrosão intergranular se caracteriza por ocorrer em torno de contornos de grãos, visíveis somente em análises metalográficas [11]. Alguns autores consideram que a corrosão intergranular ocorre como sendo o resultado da célula galvânica criada entre o contorno anódico e o interior do grão catódico. A região do contorno de grão torna-se anódica devido a presença de uma fase ou mais fases precipitadas com potencial diferente da matriz [4, 11].
A ocorrência da corrosão intergranular está associada a mecanismos que aumentam a probabilidade de precipitação de fases nos contornos de grãos. O resfriamento rápido após o tratamento térmico de solubilização reduz a precipitação nos contornos de grãos, no entanto, maiores taxas de resfriamento não são desejáveis, pois podem introduzir tensões residuais no material. O superenvelhecimento diminui a sensibilidade da liga a corrosão intergranular, devido ao engrossamento das partículas nos contornos de grãos e na matriz proporcionando a redução nas diferenças do potencial entre a fronteira e o interior do grão [4].
Outro fator que contribui para uma mudança nas condições de corrosão em uma fenda é uma diminuição no potencial do interior para a superfície livre do metal. Para as ligas de alumínio em soluções de 0,5 M de NaCl as diferenças de potencial entre a fresta e a superfície pode alcançar 270 mV. Nesse caso o agravamento da corrosão na fenda é causado predominantemente por um contato com a superfície livre [12].
O meio corrosivo no qual o metal se encontra é determinante nas condições de corrosão. Entre os meios naturais, onde as ligas de alumínio podem ser amplamente utilizadas, a água do mar é o eletrólito mais corrosivo. Em sua composição mineral, estão presentes uma complexa composição de sais marinhos, entre eles se destacam o NaCl e o MgCl2 por sua importância no processo corrosivo [12].
O efeito do cloreto de sódio, na corrosão, deve-se ao fato de este sal ser um eletrólito forte, ocasionando, portanto, aumento de condutividade, que é fundamental no mecanismo eletroquímico de corrosão [8]. Quando exposto em meios contendo íons haletos, o filme de óxido quebra em pontos específicos, levando a formação de pequenas cavidades (pites) na superfície do alumínio [2].
3. MATERIAIS E MÉTODOS
Foi utilizada a liga 6101 fornecida pela LSM Brasil, cuja composição química é apresentada na Tabela 1.
Tabela 1
Composição química da liga de alumínio 6101.
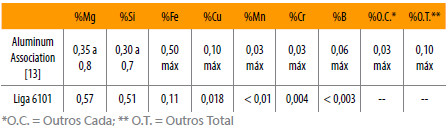
Com o intuito de avaliar o comportamento à corrosão da liga 6101 tratada termicamente em diferentes temperaturas, foram realizados os procedimentos experimentais a seguir descritos.
3.1 Tratamentos de solubilização
Os corpos de provas foram retirados de um vergalhão de 9,5 mm de diâmetro da liga 6101, e submetidas ao tratamento térmico de solubilização, que foi realizado nas temperaturas de 450 °C, 480 °C, 520 °C, 550 °C e 580 °C durante 30 minutos no forno mufla e em seguida foram resfriados em água na temperatura ambiente. A variação da temperatura obtida foi de aproximadamente 10 °C. Esse procedimento repetiu-se a cada 10 dias, por um período de 5 meses, para a obtenção das amostras solubilizadas em todas as temperaturas especificadas, com tempos que variam de 0 dias até 5 meses de envelhecimento natural.
Algumas amostras foram tratadas termicamente a 520 °C e de seguida envelhecidas durante 5 minutos à temperatura de 170 ºC, conforme apresentado na Tabela 2.
Temperaturas de solubilização das amostras.

3.2 Ensaios de corrosão
As soluções utilizadas nos ensaios de corrosão foram as seguintes:
- 3,5 % de NaCl, pH=6,81
- 0,1 M Na2SO4, pH=6,99
3.2.1 Curvas de polarização
Para a determinação das curvas de polarização, fabricaram-se seis corpos de prova, um para cada temperatura de solubilização, ambos com área exposta de 70,88 mm². Eles foram soldados a um fio e no local da solda, foram isolados com resina e esmalte, para garantir que não ocorresse contato do fio com a solução.
As curvas de polarização foram realizadas no equipamento AUTOLAB PGSTAT101, utilizando o método da voltametria linear em uma célula eletroquímica convencional de três eletrodos, sendo eles: eletrodo de trabalho(CP) , eletrodo de referência (calomelano saturado) e contra-eletrodo (platina) . Utilizou-se uma velocidade de varredura de 100 mV/min.
3.2.2 Potencial ao longo do tempo
Para a realização do ensaio de potencial ao longo do tempo, confeccionou-se 6 eletrodos da liga de alumínio 6101, para cada temperatura conforme é mostrado na Tabela 2, e para ambas soluções utilizadas, totalizando consequentemente 12 corpos de provas distintos. Os eletrodos foram imersos nas soluções de ensaio e o potencial monitorizado três vezes ao dia, durante 30 dias, com um multímetro digital, utilizando um eletrodo de calomelanos saturado como referência.
3.2.3 Análise microscópica da formação de pites
A visualização da formação de pites foi feita utilizando a microscopia eletrônica. Os corpos de provas foram lixados e polidos de forma a se obter melhores imagens da superfície da liga de alumínio 6101. Foram obtidas e comparadas as imagens da microscopia eletrônica antes e depois da realização das curvas de polarização.
4. RESULTADOS E DISCUSSÃO
4.1. Medidas de potencial a circuito aberto (Eocp) ao longo do tempo
As figuras 1 e 2 mostram o potencial de circuito aberto ao longo do tempo, para as diferentes amostras da liga 6101 com diferentes temperaturas de tratamento térmico (Tabela 2) nas soluções de 0,1 M Na2SO4 e 3,5% NaCl, respectivamente. A tabela 3 apresenta os valores dos potenciais em circuito aberto após 800 horas de imersão.
Figura 1
Curvas de potencial ao longo do tempo em solução de 0,1M Na2SO4.
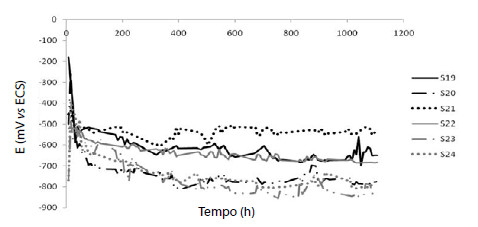
Figura 2
Curvas de potencial ao longo do tempo em solução de 3,5% NaCl.
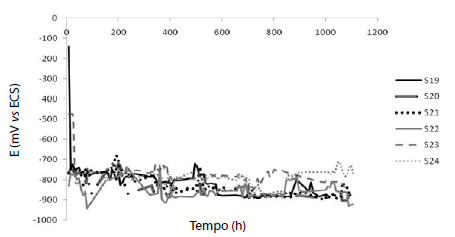
Tabela 3
Potencial em circuito aberto ao fim de 800 h.
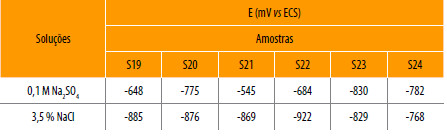
Os valores de Eocp de todas as ligas em ambas as soluções iniciaram em valores que variaram de -100 mV a - 600 mV (ECS), que estabilizaram de acordo com os potenciais apresentados na Tabela 3. O processo de estabilização do potencial ocorreu somente após uma média de 800 horas de imersão. O potencial em circuito aberto teve uma tendência catódica, ou seja, ocorreu uma queda no potencial, provavelmente devido a formação do filme passivo na superfície do corpo-de-prova.
O potencial em circuito aberto das ligas imersas em 3,5% NaCl ficaram mais negativos que na solução de 0,1M Na2SO4, o que se atribui à ação negativa dos íons cloretos em relação à estabilidade do filme passivo.
De acordo com o diagrama de equilíbrio eletroquímico para o sistema Al/H2O a 25°C (Pourbaix, 1976), os potenciais em circuito aberto de todas as ligas em ambas as soluções se estabilizaram dentro do domínio de passivação com estabilidade do óxido Al2O3.H2O e abaixo da linha de equilíbrio H2/H+. Neste caso, a reação de passivação do alumínio para o óxido ocorreu de forma termodinamicamente espontânea.
A seguir são apresentadas as curvas de polarização das ligas de Al em ambos os meios, onde é comprovado o processo de passivação na superfície do metal.
4.2. Curvas de polarização potenciostáticas
As figuras 3 a 5 apresentam as curvas de polarização anódica das ligas de Al com diferentes tratamentos térmicos, respectivamente obtidas em soluções de 0,1 M Na2SO4 e de NaCl 3,5%. Os ensaios foram realizados em condição naturalmente aerada. As tabelas 4 e 5 apresentam os potenciais de pite de cada liga respectivamente obtidas nas soluções de 0,1 M Na2SO4 e de NaCl 3,5 %. O potencial de pite foi determinado quando houve incremento significativo na densidade de corrente.
Figura 3
Curvas de polarização anódicas das amostras da liga de Al com diferentes tratamentos térmicos em solução de 0,1 M Na2SO4 naturalmente aerada.
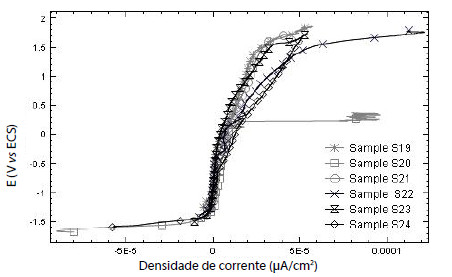
Figura 4
Curvas de polarização anódicas das amostras da liga de Al com diferentes tratamentos térmicos em solução de NaCl 3,5% naturalmente aerada.
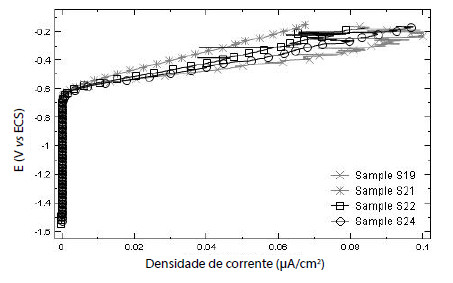
Figura 5
Curvas de polarização das amostras S20 e S23 da liga de alumínio 6101 em solução de 3,5% NaCl naturalmente aerada.
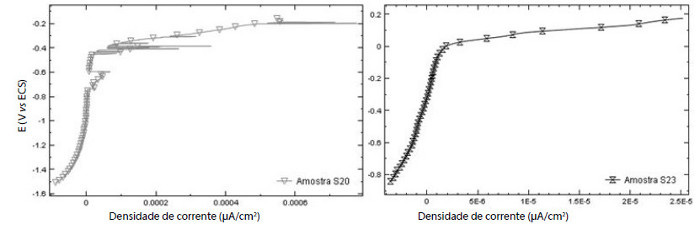
Valores do potencial e corrente de pite para as diferentes amostras da liga de alumínio 6101 em solução de Na2SO4 0,1 M, a pH 6,99.
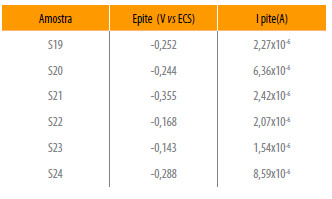
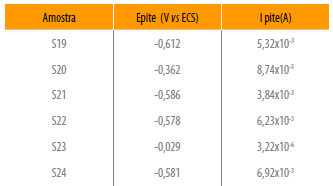
Valores do potencial e corrente de pite para as diferentes amostras da liga em solução de NaCl 3,5%, a pH 6,81.
Todas as amostras apresentaram processo de passivação em ambas as soluções testadas, ou seja, foram observados domínios de passivação numa faixa de -1150 a -1350 mV de polarização para a solução de 0,1 M Na2SO4, e de -800 a -1470 mV para a solução de 3,5 % NaCl.
Observa-se que o potencial a circuito aberto não variou de uma liga para a outra nas duas soluções testadas.
Com base no diagrama de equilíbrio eletroquímico para o sistema Al/H2O a 25 °C, todas as amostras nas duas soluções apresentaram potenciais em circuito aberto em condições naturalmente aeradas, que se situaram dentro do domínio de passivação e abaixo da linha de equilíbrio H2/H+. Neste caso, a reação de passivação anódica Al/Al2O3.H2O foi termodinamicamente espontânea.
Nas tabelas 4 e 5 são apresentados os potenciais de pite (Epite). Neste caso, nota-se que a solução NaCl foi mais agressiva que a solução de 0,1 M Na2SO4,o que era de esperar devido à presença do ião cloreto.
Ezuber et al. [2], relatam que o filme de óxido formado na superfície do alumínio é não uniforme e fino, quando exposto a ambiente agressivos, como os íons Cl-, este quebra o filme em pontos específicos gerando a corrosão por pite. Referem também que a corrosão por pite é influenciada por vários fatores, dentre eles a formação de macro defeitos como partículas de segunda fase e precipitados micro e macroscópios.
Na solução de 3,5 % de NaCl foi observado que as amostras S20 e S23 apresentaram a melhor resistência à corrosão por pite que as outras amostras. Neste caso, apresentaram maior potencial de pite e menor densidade de corrente no potencial de pite. Na solução de 0,1 M Na2SO4, as ligas S20 e S23 não se diferenciaram das outras. As outras ligas, quando testadas em NaCl, apresentaram potencial de pite que variou de -578 mV a -612 mV, sendo que a liga S24 apresentou maior densidade de corrente, podendo se considerada a mais suscetível a corrosão por pite.
As amostras apresentaram maior resistência à corrosão por pite na solução de 0,1 M Na2SO4. Isto provavelmente ocorreu porque nesta solução não ocorreu a ação dos íons Cl- que favorece a condutividade e quebra do filme passivo. O potencial de pite variou de -143 mV a -355 mV, sendo maior para a amostra S23 e menor para a amostra S21.
A amostra S23 apresentou a maior resistência à corrosão por pite entre todas as amostras em ambas as soluções. Isto provavelmente ocorreu devido esta amostra ter sido totalmente solubilizada não favorecendo a formação de pares micro-galvânicos entre o Al e os precipitados coerentes e semi-coerentes formados. .
Marioara et al. [7]., afirmam que o aumento da dureza e da resistência mecânica em consequência do tratamento térmico é resultado da nucleação e crescimento de diferentes tipos de fases metaestáveis na matriz de alumínio. Dessa forma, para que se alcance o desempenho ideal é fundamental que se investigue os parâmetros que controlam a precipitação nessa série de ligas, como: temperatura de solubilização, tempo de envelhecimento natural, temperatura e tempo de envelhecimento artificial, entre outros.
Contudo, Sinyavskii e Kalinim [12] relatam que o processo de tratamento térmico tem um complexo efeito na resistência à corrosão por esfoliação, corrosão sob tensão e corrosão intergranular. Neste caso, a corrosão intergranular é causada pelos precipitados nos contornos de grão formados durante o processo de TT. Se o potencial de corrosão destes precipitados forem diferentes da matriz poderá ocorrer a formação de micro pares galvânicos e suscetibilidade à corrosão intergranular. De acordo com Svenningsen et al. [4] os precipitados nos contornos de grão podem ser mais ou menos nobres que as zonas adjacentes, dependendo do tipo de fase precipitada. O autor ainda ressalta que a susceptibilidade ao pite pode ser associada com o engrossamento dos precipitados.
Assim sendo, a variação no potencial de pite (tabelas 4 e 5), ou seja, da resistência à corrosão de cada liga na mesma solução decorre provavelmente devido ao tipo de tratamento térmico que cada amostra foi submetida. Neste caso, no processo de TT ocorre a formação de precipitados coerentes e semi-corentes com a matriz de alumínio que apresentam diferentes tamanhos que afetam a resistência à corrosão das ligas série 6000.
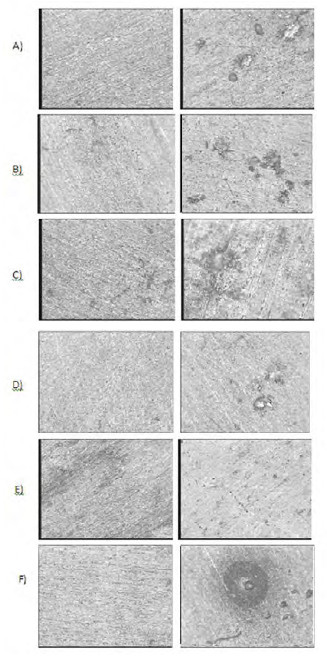
Após os ensaios de polarização os corpos de prova, ensaiados em solução de NaCl 3,5 %, foram avaliados no microscópio eletrônico para visualizar os pites (Figura 6). Nota-se que o maior pite ocorreu na amostra S24 que também apresentou maior densidade de corrente no potencial de pite (Tabela 5). A amostra S23 apresentou apenas pequenos pites confirmando a maior resistência à corrosão verificada nos ensaios de polarização.
Figura 6
Imagens obtidas por microscopia eletrônica antes e depois dos ensaios de polarização em solução de 3,5 % de NaCl, das amostras : A) S19, B) S20, C) S21, D) S22, E) S23 e F) S24 (200x).
5. CONCLUSÕES
O potencial em circuito aberto teve uma tendência de variação catódica, ou seja, ocorreu uma queda no potencial devido à formação do filme passivo na superfície do corpo-de-prova.
Os potenciais em circuito aberto de todas as amostras em ambas as soluções se estabilizaram dentro do domínio de passivação com estabilidade do óxido Al2O3.H2O e abaixo da linha de equilíbrio H2/H+. Neste caso, a reação de passivação do alumínio à forma de óxido ocorreu de forma termodinamicamente espontânea na superfície do metal.
Todas as amostras apresentaram processo de passivação em ambas as soluções testadas, ou seja, foram observados domínios de passivação numa faixa de 1150 a 1350 mV de polarização para a solução de 0,1 M Na2SO4, e de 800 a 1470 mV para a solução de 3,5 % NaCl.
A solução NaCl 3,5 % foi mais agressiva que a solução de 0,1 M Na2SO4, uma vez que os potenciais de pite foram menores para a solução de 3,5 % de NaCl que para a solução de 0,1 M Na2SO4, o que se deve à maior facilidade de quebra do filme passivo por ação do Cl-.
A amostra S23 apresentou a maior resistência à corrosão por pite entre todas as amostras em ambas as soluções. Isto provavelmente ocorreu devido esta amostra ter sido totalmente solubilizada não favorecendo a formação de micro-par galvânico entre o Al e o precipitado de Mg2Si. Contudo, para confirmar esta hipótese estão sendo realizadas as análises de Microscopia ótica, Microscopia eletrônica de varredura e Difração de raio-X para detectar estas fases e precipitados.
A variação no potencial de pite de cada amostra na mesma solução decorre provavelmente devido ao tipo de tratamento térmico que cada amostra foi submetida. Neste caso, no processo de TT ocorre a formação de precipitados coerentes e semi-coerentes com a matriz de alumínio que apresentam diferentes tamanhos que influenciam de modo diferente a resistência à corrosão das ligas série 6000.
REFERÊNCIAS
[1] W. F. Smith (Structure and Properties of Engineering Alloy), 2ª Edition, McGraw-Hill Education, New York (1992). [ Links ]
[2] H. Ezuber, A. El-Houd and F. El-Shawesh, Mater. Design, 29, 801 (2007). [ Links ]
[3] R. Vera, D. Delgado and B. M. Rosales, Corros. Sci., 48, 2882 (2006). [ Links ]
[4] G. Svenningsen, M. H. Larsen and K. N. Nordlien, Corros. Sci., 48, 258 (2005). [ Links ]
[5] W. A. Badawy, F. M. Al-Kharafi and A. S. El-Azab, Corros. Sci., 41, 709 (1998). [ Links ]
[6] M. Usta, M. E. Glicksman and R. N. Wright, Metall. Mater. Trans. A., 35, 435 (2004). [ Links ]
[7] C. D. Marioara, H. Nordmark, S. J. Andersen and R. Holmestad, J. Mater. Sci., 41, 471 (2006). [ Links ]
[8] V. Gentil, (Corrosão), 5ª Edição, Ed. Livros Técnicos e Científicos, Rio de Janeiro, Brasil (2007). [ Links ]
[9] C. B. Coutinho (Materiais Metálicos para a Engenharia), Ed. Fundação Cristiano Ottoni, Belo Horizonte, Brasil (1992). [ Links ]
[10] S. Z. Szklarska, Corros. Sci., 41,1743 (1998). [ Links ]
[11] Alumínio. Disponível em: http://www.infomet.com.br/metais-e-ligas-conteudos.php?cod_tema=10&cod_secao=11&cod_assunto=59, acesso em 13 Novembro 2010. [ Links ]
[12] V. S. Sinyavskii and V. D. KALININ, Prot. of Met+., 41, 317 (2004). [ Links ]
[13] The Aluminum Association, International Alloy Designations and Chemical Composition Limits for Wrought Aluminium and Wrought Aluminum Alloys (2007). [ Links ]
Artigo recebido em Maio de 2011 e aceite em Outubro de 2012
AGRADECIMENTOS
Agradecimentos à Fapemig pelo suporte financeiro para desenvolvimento deste trabalho e a LSM Brasil por disponibilizar o material de pesquisa.













