Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Corrosão e Protecção de Materiais
versão impressa ISSN 0870-1164
Corros. Prot. Mater. v.29 n.2 Lisboa mar. 2010
Estudo Microestrutural e Eletroquímico de Ligas Ni-Cr-Mo Usadas em Próteses Dentárias Depois de Diferentes Processos de Refundição
Lucíola Lucena de Sousa(1)(*) , Hamilton de Felipe(2), Eduardo Norberto Codaro(2) e Roberto Zenhei Nakazato(2)
(1) Instituto Unificado de Ensino Superior Objetivo – Faculdades Objetivo – IUESO, Av. T-02, nº 1.993 - Setor Bueno, Goiânia - GO – CEP 74215-010, Brasil
(2) Grupo de Corrosão e Eletroquímica - Universidade Estadual Paulista Júlio de Mesquita Filho, Av. Dr. Ariberto Pereira da Cunha, 333 Guaratinguetá-SP – CEP 12516-410, Brasil
RESUMO
Ligas Ni-Cr-Mo são amplamente utilizadas como próteses dentárias fixas, sendo utilizados diferentes procedimentos de refundição que podem alterar as propriedades mecânicas e resistência à corrosão. O objetivo desse trabalho foi analisar o comportamento eletroquímico, as microestruturas e a dureza de duas ligas refundidas pelo processo de refundição em chama aberta (maçarico oxi-GLP) e por indução em forno de alta frequência. A análise metalográfica revelou estruturas dendríticas com grãos largos e precipitados nos seus contornos. As ligas refundidas por indução apresentam menor resistência à corrosão em soro fisiológico, a 37 ºC e maiores valores de dureza.
Palavras-chave: Corrosão, Liga Dentária, Níquel-Cromo-Molibdênio
Electrochemical and Microstructural Study of Ni-Cr-Mo Alloys used in Dental Prosthesis After Different Remelting Processes
ABSTRACT
Ni-Cr-Mo alloys are widely used as fixed dental prostheses, and different procedures for remelting are used which can change the mechanical properties and corrosion resistance. The main aim of this study was to analyze the electrochemical behavior, microstructures and hardness of two remelted alloys by the open flame process (oxy-GLP torch) and by induction in high frequency furnace. Metallography analysis showed dendritic structures with large grains and precipitates in their contours. Alloys recast by induction displayed a lower corrosion resistance in physiologic serum, at 37 °C and higher hardness values.
Keywords: Corrosion, Dental Alloy, Nickel-Chrome-Molybdenum
1. INTRODUÇÃO
As ligas de metais não-nobres (básicos) para restaurações odontológicas foram introduzidas nos anos 30. Ligas não-nobres são ligas que contêm em sua composição metais ativos, isto é, metais que têm tendência a se oxidar retornando a um composto estável como o encontrado na natureza na forma de um minério. Desde essa época, as formulações de Ni-Cr têm se tornado cada vez mais populares, comparadas com as ligas de metais nobres. As vantagens em se utilizar estas ligas são seus pesos mais leves, suas propriedades mecânicas e seus custos reduzidos.
As ligas à base de níquel-cromo e cobalto-cromo, chamadas de ligas alternativas, começaram a se difundir devido ao alto custo das ligas de ouro e a partir de então foram feitos vários questionamentos com respeito às propriedades físicas e mecânicas destas ligas [1]. Esta motivação deve-se principalmente às características que apresentam, tais como: módulo de elasticidade superior, menor densidade, maior resistência, menor flexibilidade, alongamento satisfatório e custo reduzido. Suas características de expansão se assemelham com as ligas áureas e a formação de óxidos possibilita uma adequada adesão à porcelana. Estas ligas alternativas devem apresentar, dentre outras características, propriedades físicas e mecânicas adequadas a qualquer tipo de trabalho restaurador [2].
Ligas de Ni-Cr para coroas e próteses parciais fixas contêm de 60% a 80% (m/m) Ni, 16% a 27% Cr e 4% a 10% Mo.
Outros elementos podem ser adicionados em pequenas quantidades para alterar suas propriedades mecânicas, tais como: dureza e módulo de elasticidade. Estas ligas precisam exibir biocompatibilidade, facilidade de fusão, fundição, soldagem, polimento, pouca contração de solidificação, mínima reatividade com o material de revestimento, boa resistência ao desgaste e excelente resistência ao manchamento e à corrosão [3].
A resistência ao manchamento e à corrosão das ligas de Ni é de grande interesse devido ao potencial alergênico do níquel e seus compostos [4,5].
Processos corrosivos liberam íons metálicos que entram em contato com células e tecidos. Se esses íons não são biocompatíveis e se a quantidade absorvida é alta o organismo pode ser prejudicado. Estas ligas são resistentes à corrosão devido ao fenômeno de passivação, com a formação de óxidos estáveis na superfície, como o Cr2O3 [6-8]. Óxidos de Ni, Cr, Mo, Nb e de outros elementos podem ser formados na superfície, sob ação do oxigênio atmosférico após o polimento. A composição e a espessura da camada de óxidos são afetadas após refundições, podendo gerar imperfeições e ocorrer corrosão localizada principalmente em meios salinos. Além disso, em presença de outras ligas mais nobres pode ocorrer a corrosão galvânica [9,10].
Roach et al. (1998) concluíram que a liga de Ni-Cr-Mo contendo o mínimo de (16-22)% Cr e (9-14)% Mo podem formar uma camada de óxido passivo que promove resistência ao processo de corrosão [11].
Schmalz e Gardhammer (2002) relembram que a corrosão das ligas odontológicas têm como resultado a liberação de íons metálicos que podem causar efeitos biológicos locais. A corrosão na boca é um processo eletroquímico natural e espontâneo. A completa formação do filme passivo nas superfícies dos metais/ligas pode tornar a corrosão grandemente inibida, pela formação de uma camada de óxidos na superfície [12].
O conhecimento da temperatura de fusão dos metais e ligas é de grande importância no momento de sua indicação, para que se obtenha sucesso nos trabalhos realizados com estes materiais. As ligas não nobres possuem temperatura de fusão muito alta (cerca de 1400ºC) e portanto, apresentam maior contração de solidificação que as ligas de ouro, além disso, aquelas que possuem zona de fusão muito ampla são mais favoráveis à corrosão. As ligas para restauração metalocerâmica devem ter uma zona de solidificação em temperaturas elevadas, de modo que o metal permaneça sólido bem acima da temperatura de cocção da porcelana, para obter menor distorção marginal das infra-estruturas metálicas [13].
Fusão e refundição das ligas ainda representam os procedimentos laboratoriais mais amplamente usados para a fabricação de restaurações odontológicas [14,15]. Como esses procedimentos são realizados com pouco ou nenhum controle atmosférico e de temperatura, ocorrem alterações na microestrutura sendo necessários estudos mais aprofundados dos processos de refundição. Propomos nesse trabalho comparar o comportamento eletroquímico e a microestrutura de duas ligas Ni-Cr-Mo utilizadas em próteses dentárias fixas. O estudo é realizado in vitro em meio de NaCl 0,9 % em massa, pH 6 a 37 ºC simulando a agressividade do meio bucal.
2. METODOLOGIAS
Foram utilizadas duas ligas de Ni-Cr-Mo com composições de 65,0% Ni, 22,5% Cr, 9,5% Mo (Wiron 99) e 59,6% Ni, 24,0% Cr, 9,8% Mo (Wironia) que são comercializadas na condição bruta de fusão . Foram ainda utilizados tarugos de metais Cromo, Níquel e Molibdênio comercialmente puros para efeito comparativo na resistência à corrosão.
Para confecção dos corpos-de-prova foram utilizados cilindros de cera de aproximadamente 0,5 cm2 de área na seção transversal por 3 cm de comprimento, que foram revestidos com fosfato, sendo aquecido para eliminar a cera, gerando um molde. As ligas, neste trabalho, na condição bruta de fusão foram refundidas pelo método da cera perdida com dois procedimentos:
● Chama aberta (maçarico oxi-GLP) sem controle da vazão do gás e da temperatura. A chama foi incidida sobre o metal, e após a formação de uma gema, o molde foi retirado do forno, colocado perto do cadinho e por centrifugação o metal fundido penetrou no molde. O corpo-de-prova obtido por este procedimento será denominado Maçarico.
● Indução em forno de alta frequência (Forno de indução MANFREDI ALLY). Neste tipo de máquina o metal foi fundido pelo campo de indução que se desenvolveu no interior do cadinho, a 1500 ºC. Em seguida, o molde aquecido foi colocado no forno de indução próximo ao cadinho e preenchido pelo metal líquido, por centrifugação. O corpo-de-prova obtido por este procedimento será denominado Indução.
Em ambos os procedimentos os moldes foram resfriados naturalmente sem controle atmosférico. As amostras foram removidas do molde e usinadas na forma de cilindros e nesta condição utilizadas para as respectivas análises.
Na análise microestrutural as amostras foram lixadas com lixas 220 a 1500 mesh, polidas num pano de polimento com pasta de diamante de 3 mm, submetidas a um ataque eletroquímico em solução de 20% HCl e fotografadas em Microscópio Eletrônico de Varredura (MEV) LEO 1450VP, munido de um analisador por separação de energia dispersiva de raios-X, que permite a análise elementar localizada qualitativa e semi-quantitativa.
Para a confecção dos eletrodos de trabalho, as ligas Ni-Cr como recebidas e refundidas foram embutidas em resina poliéster deixando uma área exposta de 0,5 cm2. A superfície foi lixada com lixa de 220 a 1200 mesh que permitiu boa reprodutibilidade das medidas eletroquímicas.
Os ensaios eletroquímicos foram realizados utilizando as técnicas de voltametria cíclica e polarização potenciodinâmica. Para este propósito utilizou-se uma célula termostatizada de vidro, um eletrodo de referência de calomelano (SCE) adaptado a um capilar de Luggin e um contra eletrodo de platina. Como eletrólito utilizou-se solução de NaCl 0,9 % (m/m), ajustada a pH 6,0 a 37 ºC. O pH da solução foi ajustado pela adição gota a gota de ácido clorídrico ou hidróxido de sódio, com o auxílio de um agitador magnético, empregando-se um pHmetro com eletrodo de vidro combinado.
O equipamento usado foi um Potenciostato EG&G PAR 283 interfaceado a um microcomputador GS – Pentium II através de uma interface GPIB munido dos programas Softcorr III e Power Suite para o controle e processamento dos dados.
As medidas de dureza Vickers foram obtidas em um durômetro, marca Wolpert, com uma carga aplicada de 10 kgf num tempo de 15 s, seguindo a norma (ASTM E 92, 1982)[16]. Foram feitas 10 medidas em cada corpo-de-prova, em diversas regiões da amostra, tomando-se uma média que representasse, estatisticamente, o valor da dureza.
3. RESULTADOS E DISCUSSÃO
3.1 Ensaios eletroquímicos
A voltametria cíclica constitui um dos métodos mais adequados para a obtenção de informações sobre a reversibilidade de um sistema, seus potenciais formais, ocorrência ou não de reações acopladas aos processos de transferência de elétrons, bem como sobre a carga elétrica envolvida no processo e a reprodutibilidade da superfície. Na voltametria cíclica efetuou-se uma varredura no intervalo de -1,0 V a 0,8 V com uma velocidade de 33,3 mV/s e para a curva de polarização em uma faixa de potencial de –1,0 V a 1,0 V com uma velocidade de varredura de 0,333 mV/s.
Os ensaios potenciodinâmicos foram realizados iniciando-se a varredura em –1,0V, na região de desprendimento de hidrogênio. Em seguida, procedeu-se a varredura no sentido de potenciais positivos. A inversão da varredura foi feita em 0,8V, na região de dissolução do material.
As figuras 1 e 2 mostram, respectivamente, os voltamogramas cíclicos para as ligas Wiron 99 e Wironia bruta de fusão e submetidas a diferentes procedimentos de refundição. Em todos os casos observa-se uma ampla região de estabilidade entre (-0,6 e 0,6) V.
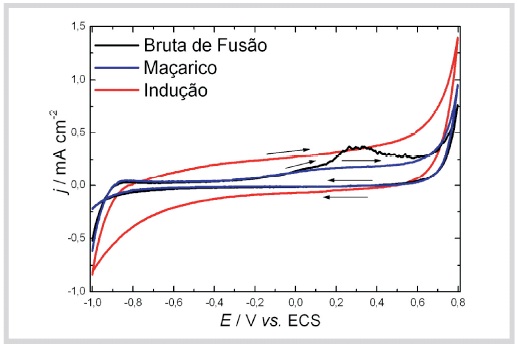
Fig. 1 - Voltamogramas cíclicos, v=33,3 mV/s, para a liga Wiron 99 em NaCl 0,9 %.
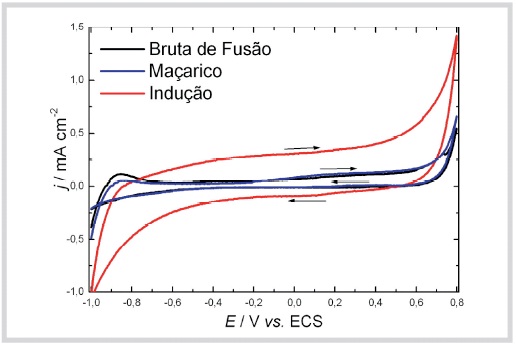
Fig. 2 – Voltamogramas cíclicos, v=33,3 mV/s, para a liga Wironia em NaCl 0,9 %.
A liga Wiron 99, Figura 1, obtida por indução, revela um aumento na densidade de corrente na região passiva comparado ao processo de refundição em chama aberta (maçarico). A liga Wiron 99 bruta de fusão apresenta um pico largo de corrente anódica cujo máximo se localiza em aproximadamente 0,3 V. Esse pico, por comparação com a Figura 3, que apresenta os resultados obtidos com metais puros utilizados como referência, foi atribuído à oxidação principalmente do níquel, presente em maior concentração na liga. Em todos os outros casos observa-se uma ampla região de estabilidade entre aproximadamente (-0,5 e 0,5) V.
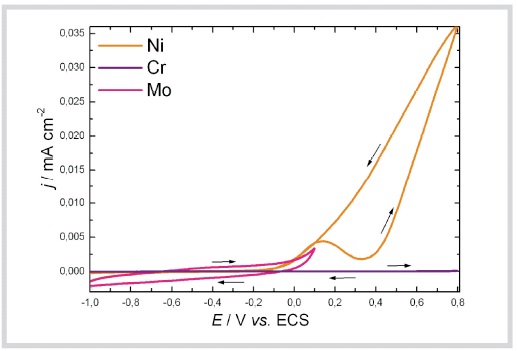
Fig. 3 - Voltamogramas cíclicos, v=33,3 mV/s dos metais puros em NaCl 0,9 %.
O efeito da refundição para a Wironia, Figura 2, é análogo ao observado para a Wiron 99. A principal diferença, no entanto, é que a liga bruta de fusão tem comportamento idêntico à liga tratada em chama aberta, sem mostrar a presença de picos de corrente de oxidação. As ligas Indução revelam uma densidade de corrente cerca de três vezes maior do que a observada para as outras ligas, o que indica um filme superficial menos resistivo.
Por meio das curvas de polarização procura-se estabelecer uma relação entre o tipo de ataque corrosivo que sofre o material e sua resistência à corrosão. As curvas de polarização para as ligas Ni-Cr brutas de fusão e maçarico em NaCl 0,9 % (m/m) mostradas nas Figuras 4 e 5 apresentaram uma região catódica, onde em pH 6,0 pode ocorrer a redução de íons H+ e/ou de oxigênio. Na região anódica observa-se uma extensa região de passivação (~1 V) que vai desde -0,3 V até aproximadamente +0,7 V. Para potenciais superiores (~0,7 V) há um acréscimo progressivo da densidade de corrente, devido à dissolução dos componentes da liga, fenômeno conhecido como transpassivação. Este comportamento é semelhante ao obtido com o Cromo, porém a densidade de corrente para o metal na região de passividade é menos elevada como visto na Figura 6. Nesta região de potenciais, as ligas refundidas por Indução apresentam um lento aumento na densidade de corrente em um amplo intervalo de potencial (~1,0 V), que pode ser interpretado como uma aparente passivação e posteriormente ocorre a transpassividade. Essa diferença de comportamento pode estar associada à maior heterogeneidade na estrutura que dificulta a formação de um filme protetor. Nas curvas do Ni e do Mo, Figura 6, não se observa uma passivação, o processo é controlado catodicamente principalmente pela velocidade de redução de oxigênio e a velocidade de corrosão é aproximadamente 100 vezes maior que no Cromo.
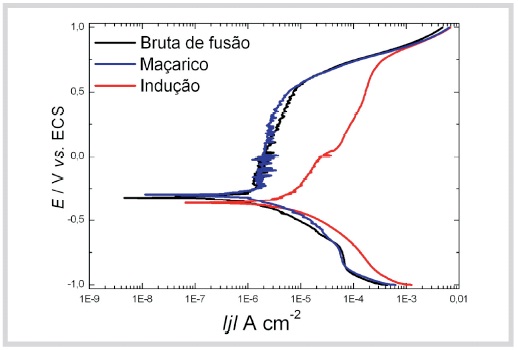
Fig. 4 - Curva de Polarização da liga Wiron 99 em NaCl 0,9 %, pH 6,0.
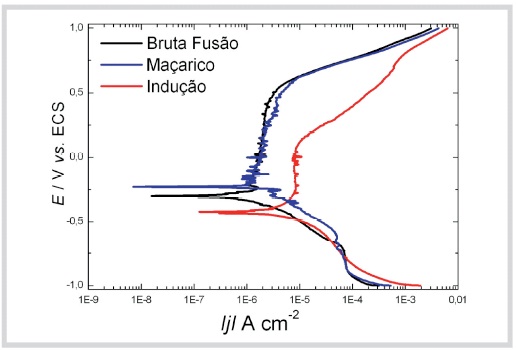
Fig.5 - Curva de Polarização da liga Wironia em NaCl 0,9 %, pH 6,0.
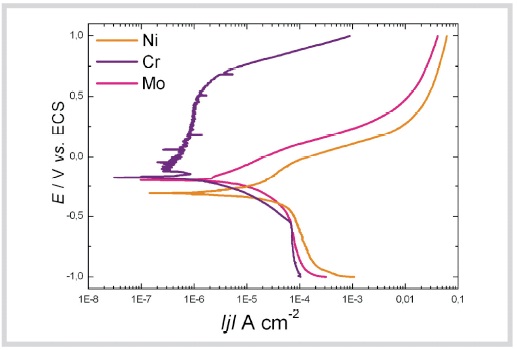
Fig. 6 - Curva de Polarização dos metais puros em NaCl 0,9 %, pH 6,0.
A passivação das ligas de Ni-Cr-Mo é frequentemente atribuída à formação de uma fina e compacta camada de óxido de cromo (Cr2O3). Huang [17,18] determinou que esta camada é constituída de óxidos e hidróxidos. Esta película é autolimitante porque age como barreira para o transporte de oxigênio e íons metálicos. A estabilidade dessa película dependerá da sua solubilidade à temperatura de trabalho.
A Tabela 1 apresenta os parâmetros, densidade de corrente de passivação (jpass), intervalo de passivação (Eruptura-Ecorr ) e potencial de ruptura (Eruptura), obtidos das curvas de polarização potenciodinâmica das ligas Wiron 99 e Wironia refundidas por diferentes processos e do Cr.
Tabela 1 - Parâmetros obtidos das curvas de polarização potenciodinâmica das ligas Ni-Cr-Mo.
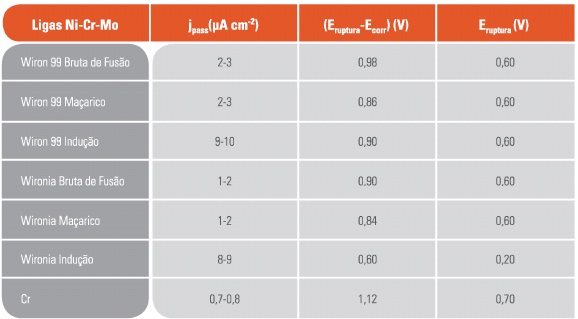
3.2 Análise metalográfica
A análise da superfície das ligas Bruta de Fusão, após revelação por ataque eletroquímico, com uma ampliação de 500x, evidencia uma estrutura constituída por uma matriz de solução sólida em disposição dendrítica (fase primária) e uma fase interdendrítica (secundária) regularmente distribuída como mostrado nas Figuras 7 e 8. Nas amostras refundidas, Figuras 10 e 12 para a amostra Wiron 99 e Figuras 9 e 11 para a Wironia são observadas duas fases: principal (solução sólida de Ni-Cr-Mo) e precipitados ricos em Mo. A Wiron 99 apresenta menor concentração de precipitado. Esses precipitados são constituídos provavelmente de carbetos de Cr e Mo, principalmente de Mo.

Fig. 7 - Micrografia eletrônica da liga Wironia Bruta de Fusão. Ampliação:500x.

Fig. 8 – Micrografia eletrônica da liga Wiron 99 Bruta de Fusão. Ampliação:500x.

Fig. 9 - Micrografia eletrônica da liga Wironia Indução. Ampliação:500x.

Fig. 10 - Micrografia eletrônica da liga Wiron 99 Indução. Ampliação:500x.

Fig. 11 - Micrografia eletrônica da liga Wironia Maçarico. Ampliação:500x.

Fig. 12 - Micrografia eletrônica da liga Wiron 99 Maçarico. Ampliação:500x.
A Wiron 99 Maçarico, Figura 12, ainda mantém caráter dendrítico, possui poros que pode ter sido adquirido na refundição, os precipitados são menores. A Wiron 99 Indução, Figura 10, possui alguns precipitados pequenos enquanto na Wironia Indução, Figura 9, percebe-se uma maior quantidade de precipitados e quantidade aproximadamente igual de precipitados que a Wironia Maçarico, Figura 11.
As ligas Wironia Maçarico e Indução apresentam precipitados maiores que a Wiron 99 e nessa liga percebe-se que não há a presença de muitos poros na amostra como visto na Wiron 99 Maçarico.
A estrutura bruta de fusão é predominantemente dendrítica e sabe-se que nesta estrutura, as dendritas têm concentração dos metais presentes, diferentes da concentração dos metais nos espaços inter-dendríticos. Isto ocorre devido ao processo de solidificação, onde as dendritas solidificam-se primeiro e, como consequência, apresentam resistências ao ataque eletroquímico e químico diferentes [19].
No processo de resfriamento e solidificação é que a microestrutura das ligas é definida [14]. Nesse processo, a precipitação de fases secundárias resulta da saturação da matriz que separa os elementos ligantes. Como resultado, formam uma nova fase [1]. A fase principal, também conhecida como homogênea é constituída de uma solução sólida de Ni-Cr-Mo que ainda mantém um caráter estrutural dendrítico e a segunda fase são precipitados eutéticos lamelares nos contornos de grãos [20]. Baran (1983) [14] trabalhou com a liga Wiron 77 e Huang [17] trabalhou com a liga Wiron 99 e obtiveram resultados parecidos. Para diversos autores que analisaram ligas com composições próximas à deste trabalho a segunda fase seriam aglomerados, provavelmente constituídos por carbetos de Cr e Mo [21].
A formação de carbetos metálicos se dá durante a solidificação da liga fundida [1]. A facilidade de reação do carbono com outros elementos metálicos resulta na formação de uma variedade de carbetos do tipo MC, M6C e M23C6, sendo M representado por vários elementos metálicos [1,14,20,22].
A diferença principal de comportamento entre a Wironia e a Wiron 99 pode estar relacionado ao fato da Wiron 99 apresentar uma quantidade muito baixa de carbono (<0,02 % C) e a presença de Nb (1,0 % Nb), que tem uma afinidade maior ao carbono levando à formação do carbeto de Nb, enquanto o Cr é mantido na solução para manter a resistência à corrosão. O carbono (C) é o elemento mais crítico, pois pequenas variações têm um efeito pronunciado na resistência mecânica, dureza e ductibilidade. A afinidade deste, por vários elementos que compõem a liga de Ni-Cr, facilita a formação de inúmeros carbetos metálicos. A precipitação destes carbetos é um fator de importância na resistência de uma liga, porém, se houver excesso uma indesejável friabilidade pode ocorrer. Os carbetos segundo Liu et al., em 2003, são ainda responsáveis pela melhoria da resistência ao creep [23]. Parece claro que o aumento da concentração de carbono tem uma influência na diminuição da resistência à corrosão, já que o carbono tem a característica de formar compostos com elementos formadores na película passivadora [24]. O nióbio (Nb) apresenta uma grande tendência à formação de óxidos com excelente resistência à corrosão. O óxido de nióbio é fortemente aderido ao substrato metálico o que contribui para uma melhor adesão à porcelana [25]. O Nb ainda tem a possibilidade de formar um composto eutético com o níquel que poderia auxiliar na fluidez da liga.
A ordem de estabilidade de óxidos em termos de energia livre é: NiO<MoO2<Cr2O3<NbO2<NbO<SiO2 e a estabilidade de carbetos por mole de carbono: NbC<SiC<Cr23C6 sendo possível a formação de uma mistura de compostos.
3.3 Ensaios de dureza
Valores de dureza Vickers são comumente fornecidos pelos fabricantes de ligas dentárias como um parâmetro útil na qualificação do material. Foram realizadas medidas de dureza, pois esta propriedade está correlacionada com a confecção da prótese (maior dureza permite a confecção de próteses mais compridas).
Medidas de dureza Vickers são mostradas na Tabela 2. Os valores representam a média de 10 medidas. As ligas bruta de fusão e as refundidas por Indução apresentam uma dureza maior do que a refundida por Maçarico.
Tabela 2 - Dureza Vickers (HV) das ligas Wironia e Wiron 99.

4. CONCLUSÕES
● Diferentes processos de refundição alteram a microestrutura, o comportamento eletroquímico e a dureza das ligas Wiron 99 e Wironia.
● A microestrutura das ligas refundidas apresenta caráter parcialmente dendrítico com o aparecimento de aglomerados, provavelmente constituídos por carbetos de Cr e Mo. O número destes precipitados nas amostras refundidas por Indução é maior indicando maior heterogeneidade.
● Ligas refundidas por Indução apresentam menor resistência à corrosão em soro fisiológico, a 37 ºC, evidenciada por não se passivarem nesse meio e por apresentarem alta densidade de carga, indicando a formação de filme protetor superficial menos resistivo.
● Refundição das ligas diminuem os valores de dureza Vickers, sendo o abaixamento mais pronunciado para a refundição com Maçarico.
REFERÊNCIAS
[1]. G. R. Baran, J. Dent. Res., 58, 196 (1979). [ Links ]
[2] D. F. Vieira (Metais e ligas metálicas; noções básicas para dentistas), 2 ed., Edgard Blucher, São Paulo, Brasil (1967).
[3] K. J. Anusavice (Phillips Materiais Dentários) 10ª ed., Ed. Guanabara Koogan, Rio de Janeiro, Brasil (1998).
[4] E. F. Huget and S. G. Vermilyea (Base metal dental and surgical alloys) in Biocompatibility of dental materials, (Smith D. C., Williams D. F., ed.), Vol. IV. Boca Raton, F.L: CRC Press, USA, p. 37-50 (1982).
[5] S. P. Kedici, A. A. Aksul, M. A. Kilicarlan, G. Bayramoglu and K. Gokdemir, J. Oral Rehabil., 25, 800 (1998).
[6] M. D. Roach, J. T. Wolan, D. E. Parsell and J. D. Bumgardner, J. Prosthet. Dent., 4, 623 (2000).
[7] S. Winkler, H. F. Morris and J. M. Monteiro, J. Prosthet. Dent., 52, 821 (1984).
[8] Y. Okazaki, T. Tateishi and Y. Ito, Mater. T. Jim, 38, 78 (1997).
[9] C. A. Elbert and G. Ryge, J. Prosthet. Dent., 15, 873 (1965).
[10] H. J. Harcout and W. Cotterill, Brit. Dent. J., 118, 323 (1965).
[11] M. Roach, D. Parsell, S. Gardner and J. D. Bumgardner, Crit. Rev. Biomed. Eng., 26, 391 (1998).
[12] G. Schmalz and P. Garhammer, Dent. Mater., 18, 396 (2002).
[13] V. F. Milagres, K. N. Olivieri et al., Revista Gaúcha de Odontologia, 53, 2, P. Alegre, Brasil, 164 (2005).
[14] G. R. Baran, J. Prosthet. Dent., 50, 5, 639 (1983).
[15] K. F. Leinfelder, J. Am. Dent. Assoc., 128, 37 (1997).
[16] ASTM E 92:1982 (Standard test method for vickers hardness of metallic materials), American Society For Testing And Materials, Philadelphia (1982).
[17] H. H. Huang, J. Biomed. Mater. Res., 60, 3, 465 (2002).
[18] H. H. Huang, Biomaterials, 24, 9, 1582 (2003).
[19] J. C. Gomes (Ataque eletroquímico em ligas de Ni-Cr e Co-Cr, efeito de soluções, tempos e densidades de corrente), Dissertação para a otenção do grau de Mestre (em Dentística) – Faculdade de Odontologia, Universidade Estadual Paulista, Araraquara, Brasil (1986).
[20] A. J. Lewis, Aust. Dent. J., 20, 5, 303, (1975).
[21] M. Leonhardt, W. Loser, H. G. Lindenkreuz, Acta Mater., 47, 10, 2968 (1999).
[22] A. J. Lewis, Aust. Dent. J., 20, 6, 383 (1975).
[23] L. R. Liu et al., Mater. Sci. Eng. A, 361, 1-2, 197 (2003).
[24] M. Oliveira, (Estudo comparativo entre cinco ligas de níquel-cromo no tocante a fluidez e consequente reprodutibilidade), Dissertação para a obtenção do grau de Mestre (em Prótese Dentária) – Universidade de Taubaté, Taubaté, Brasil (2004).
[25] O. L. Bezzon et al., J. Prosthet. Dent., 80, 5, 574 (1998).
(*) A quem a correspondência deve ser dirigida, e-mail: luciolalucena@yahoo.com.br
Artigo submetido em Maio de 2009 e aceite em Julho de 2009













